В конце декабря 2019 года в городе Ухань была выявлена вспышка заболеваемости пневмонией неясной этиологии, которая быстро распространилась по Китаю, а затем и по всему миру. Всемирная организация здравоохранения (ВОЗ) объявила о пандемии этого заболевания уже в марте 2020 года [1]. Оказалось, заболевание связано с новым вирусом из группы коронавирусов, который получил название SARS-CoV-2 (Severe acute respiratory syndrome-related coronavirus 2). В феврале 2020 года ВОЗ дала официальное название этой инфекции – Coronavirus disease 2019, или сокращённо COVID-19 [1].
Коронавирусы – РНК-содержащие вирусы, которые поражают различные виды животных, в особенности птиц и летучих мышей. На данный момент существует 7 штаммов коронавирусов, патогенных для человека (табл.). У коронавирусов, циркулирующих в природе, есть особенность: они могут преодолевать межвидовые различия, тем самым становясь патогенными для человека. Именно это произошло со штаммами SARS-CoV и MERS-CoV [2] (таблица).
Штаммы коронавируса, патогенные для человека
|
Штамм |
Год выявления |
Рецепторы для адгезии |
Путь передачи |
Клинические проявления |
|
HCoV-229E |
1960-е |
ANP |
Воздушно-капельный, контактный через слизистые |
Бронхит, реже бронхиолит, пневмония. Возможно поражение ЦНС |
|
HCoV-OC43 |
1967 |
|
Воздушно-капельный, контактный через слизистые |
Бронхит, реже бронхиолит, пневмония. Возможно поражение ЦНС |
|
HCoV-NL63 |
2004 |
ACE2 |
Воздушно-капельный, контактный, фекально-оральный |
Бронхит, бронхиолит, круп, пневмония. Возможен энтерит |
|
HCoV-HKU1 |
2005 |
|
Воздушно-капельный, контактный, фекально-оральный |
Бронхит, реже пневмония. Возможен энтерит |
|
SARS-CoV-1 |
2002 |
ACE2 |
Воздушно-капельный, контактный через слизистые |
Бронхит и бронхиолит, пневмония, ТОРС* |
|
SARS-CoV-2 |
2019 |
ACE2 |
Воздушно-капельный, контактный, фекально-оральный |
Бронхит и бронхиолит, пневмония, ТОРС*, энетрит. Поражение ЦНС? |
|
MERS-HCoV |
2015 |
CD-25 |
Воздушно-капельный, контактный через слизистые |
Бронхит и бронхиолит, пневмония, ближневосточный респираторный синдром |
Примечание. * – тяжёлый острый респираторный синдром.
ANP – аминопептидаза N; ACE2 – ангиотензин-превращающий фермент 2.
Типичная картина COVID-19 характеризуется тремя симптомами: одышка, кашель, лихорадка. Изначально считалось, что этот вирус поражает только лёгочную ткань, вызывая тяжёлый острый респираторный синдром (ТОРС). Однако, помимо системных и респираторных заболеваний, вирус обладает и нейротропностью, вследствие чего поражает и нервную систему [3].
Вирус проникает в клетки посредством адгезии на рецепторы к ангиотензин-превращающему ферменту 2 (angiotensin-converting enzyme (ACE2)). ACE2 находится на мембранах: клеток дыхательных путей и паренхимы лёгких (пневмоциты II типа), эндотелиальных клеток артерий и вен, энтероцитов тонкого кишечника, почек [4; 5]. Рассматривается существование генетической предрасположенности неврологических осложнений COVID-19, которая, вероятно, связана с полиморфизмом ACE2 [6; 7].
Наличие рецепторов к ACE2 не всегда свидетельствует об успешном проникновении SARS-CoV-2 в клетки-мишени. Например, энтероциты продемонстрировали свою устойчивость к возбудителю инфекции. В то же время клетки печени (гепатоциты), не имеющие на своей поверхности данные рецепторы, в большой степени подвержены проникновению вируса [8].
Последнее время всё чаще описываются неврологические осложнения COVID-19, к которым относятся: острое нарушение мозгового кровообращения, тяжелый вирусный геморрагический энцефалит, острые демиелинизирующие поражения, в том числе и синдром Гийена-Барре (СГБ).
Цель исследования: изучить, каким образом вирус SARS-CoV-2 поражает нервную систему на примере синдрома Гийена-Барре.
Материалы и методы исследования: был проведён анализ отечественной и зарубежной литературы, на основании чего нами были выделены основные пути проникновения SARS-CoV-2 в клетки нервной системы. Мы описали этиопатогенез классического синдрома Гийена-Барре, сущность которого заключается в аутоиммунном поражении периферической нервной системы (ПНС). Для того чтобы описать этиопатогенез синдрома Гийена-Барре, ассоциированного с COVID-19, мы разобрали несколько клинических случаев, описанных российскими и зарубежными авторами, а также описали основные теории поражения нервной системы.
Этиопатогенез синдрома Гийена-Барре
СГБ – острая воспалительная демиелинизирующая полирадикулоневропатия (ОВДП) аутоиммунной природы. Данное заболевание впервые было описано O. Landry в 1859 году, когда он опубликовал 10 случаев «острого восходящего паралича», сопровождающегося бульбарным синдромом и дыхательной недостаточностью [9]. Однако этот синдром стал известен позднее, в 1916 году, после работ G. Cilliain и J.A. Barre [9].
Этиология и патогенез СГБ на данный момент до конца не изучены. Известно, что 2/3 пациентов за 2-3 недели до развития неврологической симптоматики перенесли инфекционные заболевания (желудочно-кишечные или респираторные инфекции), вызванные Campylobacter jejuni, цитомегаловирусом, вирусами Эпштейна-Барр, гриппа А, ECHO, Коксаки и т. д. [9].
СГБ проявляется аутоиммунным поражением ПНС, приводящим к деструкции миелиновой оболочки со вторичной аксональной деструкцией нервных волокон (рис.). Инфекция запускает выработку в организме аутоантиген-специфических Т-лимфоцитов, стимулирует выработку аутоантител В-клетками против ганглиозидов [10]. Учитывая обширный спектр ганглиозидов, каждый из которых локализуется в строго специфическом участке ПНС, определены паттерны заболевания (рис.).
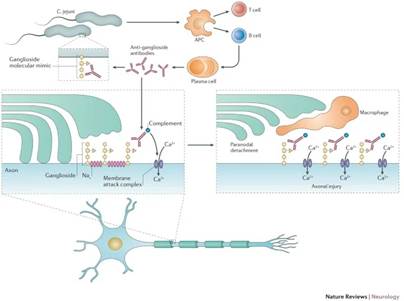
Патогенез синдрома Гийена-Барре
Установлено, что при инфекции, вызванной цитомегаловирусом, вырабатываются аутоантитела к ганглиозиду GM2 и развивается острая воспалительная демиелинизирующая полинейропатия (ОВДП) [11]. Острая моторно-сенсорная аксональная нейропатия (ОМСАН) развивается после перенесённой инфекции, вызванной Campylobacter jejuni, и ассоциирована с аутоантителами к ганглиозидам GM1, GM1b и GD1a [11]. Синдром Миллера-Фишера (СМФ), являющийся одной из форм СГБ, характеризуется триадой признаков: офтальмоплегия, атаксия и арефлексия. Диагностическим критерием для постановки диагноза СМФ является выявление антител к ганглиозидам GQ1b, GT1a [11].
При поражении ПНС, ассоциированном с SARS-CoV-2 или с вирусом Зика, аутоантитела к ганглиозидам определяются редко [12].
СГБ, ассоциированный с COVID-19
Существует ряд путей проникновения SARS-CoV-2 в клетки нервной ткани: интраназальная инокуляция (т. е. через обонятельные нервы), транссинаптическая передача посредством периферических нервов, эндотелиальные клетки гематоэнцефалического барьера и клеточная инвазия [13]. Так как ни у одного больного с СГБ в цереброспинальной жидкости не было выявлено SARS-CoV-2, можно исключить прямое повреждающее действие вируса на ПНС [8].
Считается, что СГБ является неврологическим осложнением COVID-19, поскольку основной путь заражения инфекцией воздушно-капельный и большинство пациентов первично описывают симптомы острой респираторной вирусной инфекции, а неврологическая симптоматика присоединяется вторично [14].
Zhao H. и соавт. [15] описали сочетание СГБ и COVID-19 у женщины в возрасте 61 года. Пациентка поступила в стационар с жалобами на острую слабость в обеих руках и ногах. Из анамнеза известно, что она вернулась из г. Ухань в конце января 2020 года, однако симптомов инфекционного процесса выявлено не было. В анализе крови лимфоцитопения (0,52·109 /л, n=1,1 – 3,2·109 /л). Во время проведения неврологического обследования была выявлена симметричная слабость и арефлексия в обеих руках и ногах. Сила мышц составляла 4/5 на верхних конечностях, 3/5 – на нижних. Чувствительность к прикосновениям и уколам снижена дистально. На основании клинических данных, результатов электронейромиографии (ЭНМГ) был поставлен диагноз «синдром Гийена-Барре» и начата терапия внутривенным введением иммуноглобулина. Во время пребывания в стационаре с больными новой коронавирусной инфекцией не контактировала, однако на 8-е сутки у неё повысилась температура тела до 38,2 °С, появился сухой кашель. На компьютерной томографии органов грудной клетки (КТ ОГК) выявлены затемнения по типу «матовых» стёкол, в мазке из ротоглотки выявлен SARS-CoV-2. После этого был поставлен диагноз COVID-19 и назначена противовирусная терапия, состоящая из препаратов: арбидол, лопинавир и ритонавир. При выписке на 30-й день респираторные симптомы исчезли вместе с неврологической симптоматикой. Zhao H. и соавт. [15] не исключают, что пациентка заразилась вирусом SARS-CoV-2 во время пребывания в г. Ухань, и COVID-19 способствовал развитию СГБ.
Приведённый в качестве примера клинический случай не является единичным. В Российской Федерации Е.В. Ширшова и соавт. [16] описывают пациента 72 лет, поступившего на лечение в ФНКЦ ФМБА России в конце февраля 2021 года. Больной обратился с жалобами на онемение и слабость в руках и ногах, жалоб на симптомы инфекционного процесса не предъявлял. Со слов пациента, с больными COVID-19 не контактировал, коронавирусной инфекцией не болел. При поступлении ПЦР-тест на SARS-CoV-2 отрицательный. Во время проведения неврологического обследования выявлено снижение мышечной силы верхней конечности до 2/5 баллов, нижней конечности – до 1,5/5. Тонус мышц был снижен диффузно на верхних и нижних конечностях, арефлексия. Вялый тетрапарез. На основании клинических данных и результатов ЭНМГ был диагностирован синдром Гийена-Барре и начата терапия внутривенным вливанием иммуноглобулина человека Октагам. На 18-й день состояние пациента ухудшилось в связи с появлением кашля и снижением сатурации SpO2 до 74%. В анализе крови лимфоцитоз (17,16×109 /л, n=1,1 – 3,2·109 /л). После этого была проведена КТ ОГК, по результатам которой выявлена двусторонняя полисегментарная пневмония, выявлены Ig M и G к S-белку SARS-CoV-2 методом иммуноферментного анализа. На основании проведённых исследований был выставлен диагноз COVID-19. Е.В. Ширшова и соавт. [16] не исключают, что описанный клинический случай также является примером СГБ, ассоциированного с COVID-19.
Патогенез ОВДП, возникшей на фоне новой коронавирусной инфекции, до конца не ясен. Однако на сегодняшний день в зарубежной литературе можно найти несколько предположений, способных объяснить этот феномен.
По мнению многих авторов, СГБ, ассоциированный с COVID-19, в отличие от классической ОВДП представляет собой «острую параинфекцию». Это предположение основывается на том, что у значительного количества больных разгар аутоиммунной полирадикулопатии отмечался через несколько дней после начала острой респираторной вирусной инфекции [17; 18].
Кроме того, значительное количество авторов высказывают мнение о том, что параинфекционный механизм развития СГБ может опосредоваться генерализованным гипериммунным ответом, который возникает на новый вирус SARS-CoV-2 [17; 18]. Это может объяснить отсутствие аутоантител к ганглиозидам в случаях, когда проявление симптоматики СГБ возникает в первые дни развития симптомов новой коронавирусной инфекции [19].
Мнение о параинфекционном механизме развития СГБ, ассоциированного с COVID-19, подкрепляется тем, что стандартная терапия ОВДП, заключающаяся во внутривенном введении иммуноглобулина человеческого и плазмаферезе, оказалась терапевтически несостоятельной [17].
Caress J.B. и соавт. высказали предположение о том, что развитие СГБ, ассоциированного с COVID-19, связано с развитием перекрёстной реактивности между ганглиозидами нервной ткани и вирусными белками, возникшей как результат молекулярной мимикрии [20]. Кроме того, Caress J.B. и соавт. выдвинули и альтернативную точку зрения, согласно которой ключевая роль в поражении клеток ПНС принадлежит активации Т-лимфоцитов и высвобождению медиаторов воспаления макрофагами [20].
Заключение
Таким образом, новая коронавирусная инфекция COVID-19, вызванная вирусом SARS-CoV-2, проявляется не только симптоматикой острой респираторной вирусной инфекции, но и поражением периферической нервной системы. Последнее время синдром Гийена-Барре всё чаще описывается в качестве осложнения COVID-19.
По сравнению с классическим синдромом Гийена-Барре, при котором на фоне инфекционного процесса вырабатываются аутоантитела к ганглиозидам GM2, GM1, GM1b, GD1a, GQ1b, GT1a нервной ткани, при ОВДП, протекающей на фоне COVID-19, аутоантитела выявляются крайне редко.
В результате анализа зарубежной литературы мы определили несколько механизмов развития синдрома Гийена-Барре, ассоциированного с COVID-19:
1. Параинфекционный механизм.
2. Механизм развития перекрёстной мимикрии между белками SARS-CoV-2 и ганглиозидами нервной ткани.
3. Механизм активации Т-лимфоцитов и высвобождения медиаторов воспаления макрофагами.



