Колоректальный рак (КРР) является актуальной проблемой современной онкологии, занимает одно из лидирующих мест в структуре заболеваемости и смертности от онкологических заболеваний во всем мире. Ежегодно выявляются более 1 млн новых случаев КРР приблизительно с одинаковой частотой распространения у мужчин и женщин [1, 2].
Сегодня разработано большое количество современных методов визуализации. Но, несмотря на значительные диагностические возможности, показатели запущенности КРР остаются высокими. На момент обращения больного, как правило, онкопроцесс имеет местно-распространенный характер с наличием лимфогенных и отдаленных гематогенных метастазов [3, 4].
Больше половины случаев КРР приходится на рак ободочной кишки (РОК), который занимает 4-е место в структуре общей онкологической заболеваемости (оба пола), 5-е место в структуре онкологической заболеваемости у мужского населения и 4-е место – у женского [5].
В последнее время актуальным предметом исследований в современной онкологии является изучение роли различных звеньев иммунной системы в развитии, клиническом течении, прогрессировании опухолевого процесса [6]. Эффекторные и регуляторные механизмы системы врожденного и приобретенного иммунитета, взаимодействуя с опухолевыми клетками, определяют биологические особенности последних и влияют на процессы возникновения опухолей, их метастазирования, а также устойчивость к радио- и химиотерапевтическому лечению опухоли. Доказана двузначная роль иммунной системы в канцерогенезе: как противоопухолевых эффектов, так и опухоль-стимулирующих. В сложившейся ситуации особую актуальность приобретает изучение роли отдельных компонентов как адаптивного, так и врожденного иммунитета.
Иммунная система пищеварительного тракта играет важную роль в защите организма от действия инфекционных агентов, токсинов, осуществляет их инактивацию и элиминацию.
Сегодня доказано, что местные и системные воспалительные реакции имеют большое значение в прогрессировании опухолевого процесса, влияя на исход заболевания. Опухоли толстой кишки инфильтрированы различными иммунными и воспалительными клетками. Ряд исследований показал, что наибольшее значение имеет число Т-лимфоцитов, которые инфильтрируют опухоль [7]. Как известно, ткань опухолей толстой кишки содержит небольшое количество Т-лимфоцитов с рецепторами CD4+ и CD8+ [8].
Ряд авторов рассматривают макрофагальную инфильтрацию опухоли и перитуморальной зоны как прогностический фактор: низкая плотность инфильтрации связана с более высокими инвазивными свойствами опухоли [9–10].
В зарубежной литературе имеется ряд исследований по изучению опухоль-инфильтрирующих иммунокомпетентных клеток и их прогностической значимости при КРР, но на сегодняшний день остается много спорных и нерешенных вопросов [11–13]. В литературе отсутствуют данные, посвященные изучению локального клеточного иммунитета при РОК в зависимости от локализации опухолевого процесса, что и определяет актуальность нашего исследования.
Цель исследования: выявить особенности локального популяционного и субпопуляционного состава иммунокомпетентных клеток при раке ободочной кишки различной локализации опухоли.
Материал и методы исследования
В исследование включены 50 пациентов с РОК, которые проходили лечение в отделениях абдоминальной онкологии № 1 с группой рентгенэндоваскулярных методов диагностики и лечения и абдоминальной онкологии № 2 ФГБУ «НМИЦ онкологии» Минздрава России.
Критерии включения в работу:
1) наличие гистологически верифицированной аденокарциномы ободочной кишки;
2) TNM –сT1-4N0-2 M0;
3) статус ECOG – 0–2;
4) возраст более 18 лет;
5) подписанное информированное согласие.
Критерии исключения: наличие терапевтических или психиатрических заболеваний; беременность или период лактации; наличие синхронных злокачественных опухолей; наличие острой хирургической патологии.
В выборку вошли 26 женщин (52%), средний возраст которых составил 67±0,4 года, и 24 мужчины (48%) со средним возрастом 66±0,3 года. Преобладали пациенты, имеющие II стадию онкопроцесса, – 25 (50%) (рис. 1).
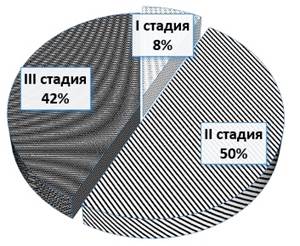
Рис. 1. Распределение больных по стадии заболевания: I cтадия – 8%, II стадия – 50%, III стадия – 42%
В зависимости от локализации опухолевого процесса (правая половина и левая половина ободочной кишки) пациенты были разделены на 2 равные группы по 25 человек в каждой.
На первом этапе лечения всем пациентам было проведено стандартное хирургическое вмешательство с забором материала для проведения дальнейших исследований. Из фрагмента опухоли, перифокальной зоны (1–3 см от опухоли), линии резекции (~10 см от опухоли) получали суспензии клеток, которые обрабатывали панелью антител в соответствии с указаниями фирмы-производителя (Becton Dickinson, USA) для идентификации основных популяций и субпопуляций лейкоцитов и лимфоцитов с использованием проточного цитометра BD FACSCanto (Becton Dickinson, USA). Результаты выражали в относительном количестве основных популяций и субпопуляций лимфоцитов (CD3+, CD4+, CD8+, ДП (CD3+CD4+CD8+), ДН (CD3+CD4-CD8-), NK, TNK, CD19+) по отношению к общему числу лимфоцитов, имеющих вышеобозначенные рецепторы. Формировали базу полученных данных с использованием Microcoft Excel. Формирование первичной базы данных, содержащей количественные значения определяемых параметров, осуществляли с использованием пакета программ MS Office Excel 2016.
Статистическую обработку полученных результатов проводили с использованием пакета STATISTICA 13,3 (StatSoft Inc., США), что предполагало расчет основных статистических характеристик выборок, определение характера распределения определяемых показателей с использованием критерия Шапиро–Уилка. Достоверность отличий между выборками оценивалась с использованием непараметрического критерия Манна–Уитни. Результаты считались статистически значимыми при p<0,05.
Результаты исследования и их обсуждение
Полученные данные субпопуляций лимфоцитов в опухолевой ткани, перитуморальной зоне (1–3 см) и линии резекции (~10 см) в правой и левой половинах ободочной кишки представлены в таблице и на рисунках 2, 3, 4.
Субпопуляционный клеточный состав иммунокомпетентных клеток в тканях опухоли, Me, %
|
|
Опухоль n=50 |
|
|
Субпопуляция лимфоцитов |
Правая половина ободочной кишки n=25 |
Левая половина ободочной кишки n=25 |
|
Лимфоциты |
3,9 |
2,05* |
|
CD3+ |
86,75 |
78,8 |
|
CD4+ |
49,15 |
53,7 |
|
CD8+ |
43,55 |
39,1 |
|
ДП (CD3+CD4+CD8+) |
0,6 |
0,5 |
|
ДН (CD3+CD4-CD8-) |
5,55 |
4,25 |
|
NK |
2,35 |
3 |
|
NKT |
5,45 |
6,05 |
|
CD19+ |
5,5 |
11,4* |
Примечание: * – статистически значимые различия по критерию Стьюдента (р<0,05)
Отмечено снижение лимфоцитарной инфильтрации в тканях опухоли левой половины ободочной кишки по сравнению с правой половиной на 47% (p<0,05). При этом процентное содержание CD3+-, CD4+-, CD8+-клеток было практически одинаково независимо от локализации опухоли. Отличительной особенностью опухолей левосторонней локализации является инфильтрация опухоли NK-клетками, которая больше на 28%, чем при правосторонней локализации (p<0,05). Для опухолей левой половины ободочной кишки характерно увеличение содержание CD19+ до 107%, чем при опухолях правой половины (p<0,05) (рис. 2).
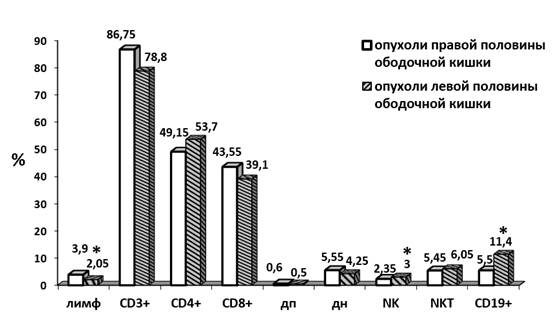
Рис. 2. Субпопуляционный состав в тканях опухоли группы пациентов с РОК различной локализации (правой и левой половины ободочной кишки), * p<0,05, статистически значимые различия
В перифокальной зоне опухолей левой половины ободочной кишки выявлено снижение на 59%, 26%, 34% и 30% относительного количества лимфоцитов, NK-, NKT- и CD19+ соответственно по сравнению с перифокальной зоной опухолей правой половины ободочной кишки (p<0,05). Также отмечено значимое повышение содержания CD8+- и ДП клеток на 107% и 425% соответственно при левосторонней локализации процесса в отсутствие изменений CD3+-, CD4+-клеток (p<0,05) (рис. 3).
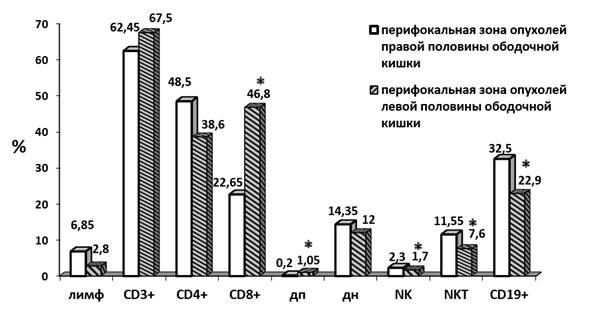
Рис. 3. Субпопуляционный состав в тканях перифокальной зоны группы пациентов с РОК различной локализации (правой и левой половины ободочной кишки), * p<0,05, статистически значимые различия
В отдаленном участке при опухолях левосторонней локализации отмечено повышение лимфоцитарной инфильтрации, процентного содержания лимфоцитов, CD8+-клеток, ДП по сравнению с правосторонней локализацией на 25%, 34% и 50% соответственно (рис. 4).
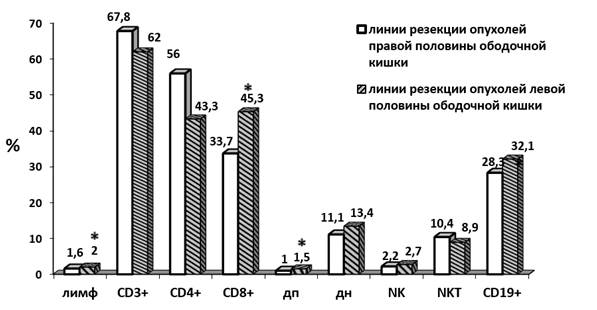
Рис. 4. Субпопуляционный состав в тканях отдаленного участка кишки группы пациентов с РОК различной локализации (правой и левой половины кишки), * p<0,05, статистически значимые различия
Результаты исследования и их обсуждение. В литературе существуют данные, свидетельствующие о том, что ткань колоректальной опухоли инфильтрирована малым количеством Т-лимфоцитов. J.R. Jass et al. (1987) доказали, что выраженная лимфоцитарная инфильтрация вокруг опухолевой ткани является прогностическим фактором более длительной выживаемости пациентов КРР [11–13]. С одной стороны, большее скопление CD8+ Т-клеток в опухолевой ткани достоверно коррелировало с более длительной выживаемостью пациентов, а с другой – значительное количество CD8+ Т-клеток в строме опухоли и вдоль ее инвазивного края не являлось важным прогностическим фактором выживаемости [14, 15]. Данные результаты позволили сделать вывод, что значение имеет не только количественный и качественный состав иммунокомпетентных клеток, которые присутствуют в опухоли.
A.C. Diederichsen et al. доказали следующий факт: низкое соотношение опухоль-инфильтрирующих лимфоцитов CD4+/CD8+ является прогностическим фактором более длительной выживаемости пациентов с КРР [16].
В исследовании Е.А. Никипеловой и соавт. показано, что содержание СD3+, СD4+ в ткани опухоли было статистически достоверно выше на 45,0%. В 1,8 раза и на 52,0% был выше индекс CD4+/CD8+ в сравнении с показателями условно здоровой ткани и ткани перитуморальной зоны (р<0,05), а также на 19% снижено количество СD8+-клеток и В-лимфоцитов на 22,0% по сравнению с условно здоровой тканью и на 43,0% относительно перитуморальной зоны (р<0,05).
Полученные Е.А. Никипеловой и соавт. данные о тканевом составе иммунокомпетентных клеток в опухоли и непораженной ткани толстой кишки обусловили разработку критериев для прогноза потенциально возможного развития метастазов КРР [17].
Выводы
При изучении локального иммунного статуса пациентов с РОК в нашем исследовании отмечается ряд следующих особенностей.
1. В опухолях правой половины ободочной кишки отмечается более высокая Т-лимфоцитарная инфильтрация по сравнению с опухолями левой половины, для которых характерна повышенная В-лимфоцитарная инфильтрация.
2. В тканях перифокальной зоны при опухолях левосторонней локализации наблюдаются снижение относительного количества лимфоцитов, NK-, NKT- и В-лимфоцитов и значительное повышение содержания CD8+- и ДП клеток.
3. При изучении популяционного состава линий резекции при опухолях левосторонней локализации отмечено повышение лимфоцитарной инфильтрации, процентного содержания CD8+-клеток, ДП лимфоцитов.
4. Таким образом, выявленные особенности локального популяционного и субпопуляционного состава иммунокомпетентных клеток при РОК в зависимости от локализации опухолевого процесса могут определить клиническое течение заболевания и способствовать выбору тактики дальнейшего лечения.



