Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
INFLUENCE OF STEREOTAXIC RADIOSURGERY ON MICRORNA EXPRESSION IN THE BLOOD PLASMA OF PATIENTS WITH METASTATIC BRAIN LESION BY NON-SMALL CELL LUNG CANCER
Рак легкого в Российской Федерации занимает третье место по заболеваемости злокачественными новообразованиями среди всего населения (9,4%) и первое место среди мужчин (16,3%) [1], а также является самой частой причиной метастатического поражения головного мозга (40% случаев) [2, 3].
Лучевая терапия представляет собой наиболее эффективный нехирургический метод радикального лечения злокачественных опухолей. Приблизительно 50% всех больных раком на различных этапах лечения получают лучевую терапию – отдельно или в сочетании с хирургическим вмешательством и/или химиотерапией. Несмотря на то что в последние годы радиационная терапия была значительно технически усовершенствована, что позволило более точно доставлять дозу, у огромного числа пациентов все еще наблюдаются рецидивы заболевания [4].
Лучевая терапия является одним из основных методов терапии больных с метастатическим поражением головного мозга (МПГМ) [5]. Стереотаксическая радиохирургия (SRS) – это высокоточное локальное облучение, проводимое за одну фракцию с использованием комбинации жесткой иммобилизации и визуального контроля, что обеспечивает высокую точность облучения опухоли с низким риском повреждения окружающей ткани мозга.
Ионизирующее излучение (ИИ) повреждает клетки, высвобождая промежуточные ионы и свободные радикалы, которые вызывают одноцепочечные или двухцепочечные разрывы ДНК [6]. Индуцированные ионизирующим излучением повреждения ДНК запускают реакцию каскада белков, влияющих на репарацию ДНК и сигнализирующих об остановке клеточного цикла. Это позволяет клетке определить, способна ли она восстановить повреждение ДНК или, когда произошло слишком большое повреждение, погибнуть в результате апоптоза или отсроченной митотической гибели клетки [7].
Известно, что основной характеристикой опухоли, влияющей на исход после лучевой терапии, является врожденная радиорезистентность опухолевых клеток, на которую влияют внутренние генетические и эпигенетические факторы. В этом контексте нарушение регуляции ДНК и других клеточных сигнальных путей при раке играет основную роль в обеспечении устойчивости к ионизирующему излучению [8, 9]. Поэтому в последние годы активно ведется разработка ингибиторов ключевых компонентов этих путей с целью разработки стратегий лечения для преодоления резистентности к лучевой терапии.
МикроРНК представляют собой эндогенные малые некодирующие молекулы РНК, которые регулируют экспрессию различных генов [10–14]. Представление о том, что микроРНК играет одну из ведущих в развитии опухоли, вместе с представлением о способности одной микроРНК контролировать несколько генов-мишеней одновременно, привело к увеличению интереса к определению функциональной связи между экспрессией микроРНК и радиочувствительностью [15–17]. В этом аспекте в некоторых исследованиях было продемонстрировано, что микроРНК принимают участие в ответе на ионизирующее излучение, потому что многие из них непосредственно регулируют экспрессию генов, участвующих в клеточных путях, имеющих отношение к ответу на облучение [18]. Однако понимание причинной роли отдельных микроРНК в детерминации радиорезистентности опухоли все еще находится на начальной стадии.
В экспериментальных исследованиях было продемонстрировано влияние ионизирующего излучения на экспрессию микроРНК hsa-miR-16-5p, hsa-miR-21-5p и hsa-miR-663 при воздействии ионизирующего излучения высокой мощности [19]. С учетом имеющихся экспериментальных данных было решено оценить влияние терапии на паттерны экспрессии микроРНК у пациентов с метастатическим поражением головного мозга немелкоклеточным раком легкого.
Цель исследования: оценить влияние терапии на паттерны экспрессии микроРНК у пациентов с метастатическим поражением головного мозга немелкоклеточным раком легкого с определением возможных закономерностей.
Материалы и методы исследования
В исследование включены 90 пациентов с метастатическим поражением головного мозга немелкоклеточным раком легкого, которым была проведена лучевая терапия в отделении радиотерапии ФГБУ «НМИЦ онкологии» МЗ РФ в 2018–2021 гг. Пациенты были разделены на 3 группы по методике проводимой терапии: 1-я группа – облучение всего головного мозга (ОВГМ); 2-я группа – стереотаксическая радиохирургия; 3-я группа – стереотаксическая радиохирургия с однократной внутривенной инфузией бевацизумаба в дозе 5 мг/м2 за сутки до проведения сеанса стереотаксической лучевой терапии. Оценка эффективности лечения оценивалась по критериям RANO BM (Response Assessment in Neuro-Oncology Brain Metastases). В таблице 1 обобщены клинические характеристики непосредственно перед началом лечения для трех исследуемых групп.
Таблица 1
Клиническая характеристика пациентов
|
Группы пациентов
Параметры |
1-я группа (ОВГМ) |
2-я группа (SRS) |
3-я группа (SRS + бевацизумаб) |
|
|
Количество пациентов |
30 |
30 |
30 |
|
|
Кумулятивный объем образований, см3 |
Среднее |
8,03 |
3,14 |
4,06 |
|
Диапазон |
1,6–17,5 |
0,2–10,628 |
0,14–16,4 |
|
|
Количество очагов в головном мозге |
1 очаг |
0 |
16 |
10 |
|
2–4 очага |
4 |
10 |
9 |
|
|
5 и более |
26 |
4 |
11 |
|
|
Возраст пациентов |
Среднее |
60,1 |
58,6 |
60,9 |
|
Диапазон |
45–73 |
33–78 |
36–73 |
|
|
Старше 65 лет |
8 |
9 |
13 |
|
|
Пол |
Мужчины |
12 |
18 |
19 |
|
Женщины |
18 |
12 |
11 |
|
Пациентам всех групп производился забор венозной крови непосредственно перед сеансом лучевого лечения и через 1 месяц после завершения лечения. Из венозной крови путем центрифугирования выделялась плазма, в которой производилась оценка уровня экспрессии микро-РНК: hsa-miR-15a-5p, hsa- miR-16a-5p, hsa-miR-17-3p, hsa-miR-21-5p, hsa-miR-145-5p, hsa-miR-663.
Суммарную РНК из 0,2 мл плазмы экстрагировали с использованием реагента TRIzol® LS и набора для выделения miRNeasy Serum/Plasma Kit (Qiagen, Германия) с использованием автоматической станции выделения QIAcube Connect. Использовали syn-cel-miR-39 в качестве дополнительного контроля для некоторых технических вариаций экстракции РНК из плазмы. Рассчитывали медианное значение CT syn-cel-miR-39, полученное для всех образцов. Все образцы РНК хранили при –80°C. Для получения кДНК микроРНК подвергали полиаденелированию и обратной транскрипции с использованием E. coli polyA-полимеразы (NEB, США) и MMLV-ревертазы (Евроген, Россия), а также универсального праймера для обратной транскрипции, как описано в статье I. Balcells et al. [20]. ПЦР проводили с использованием набора HS Taq ДНК-полимераза (Евроген, Россия) в присутствии интеркалирующего красителя EvaGreen и специфичных праймеров для амплификации исследуемых микроРНК. Для непарных сравнений двух групп использовали критерий Вилкоксона. Различия экспрессии рассчитывали с помощью ANOVA. Значение p<0,05 указывает на статистическую значимость.
Результаты исследования и их обсуждение
Среди исследуемых микроРНК – hsa-miR-15a-5p, hsa- miR-16a-5p, hsa-miR-17-3p, hsa-miR-21-5p, hsa-miR-145-5p, hsa-miR-663 – относительная экспрессия во всех трех группах после проведенной лучевой терапии достоверно изменялась у четырех микроРНК: hsa-miR-15a-5p, hsa- miR-16a-5p, hsa-miR-21-5p, hsa-miR-663 (рис. 1–3). Достоверное изменение относительной экспрессии наблюдалось только в 1-й группе пациентов hsa-miR-15a-5p после проведенного облучения всего головного мозга (p=0,0079). МикроРНК miR-16a-5p демонстрирует изменения относительной экспрессии во всех трех исследуемых группах, однако только в 1-й группе пациентов, после проведенного облучения всего головного мозга, изменения оказались статистически достоверными (p=0,0076) и характеризовались увеличением экспрессии в среднем в 1,16 раза. Уровень Hsa-miR-21-5p снижается только у пациентов 2-й группы после проведенной стереотаксической радиохирургии в самостоятельном варианте (p=0,0096). Во всех 3 группах пациентов после терапии наблюдалось достоверное снижение содержания микроРНК hsa-miR-663 (p=0,0079; 0,0095; 0,0076 соответственно). Наглядно описанные изменения представлены на рисунках 1, 2 и 3 соответственно.
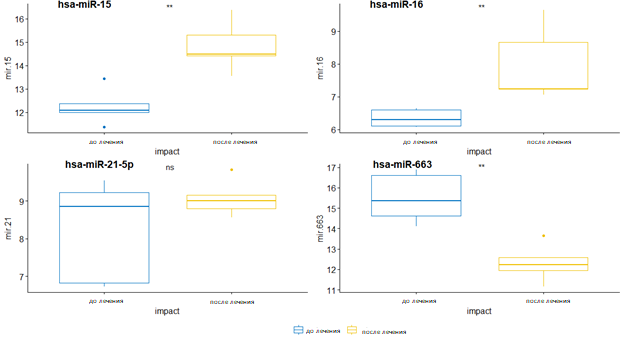
Рис. 1. Изменения уровней экспрессии микроРНК в плазме после лучевой терапии пациентов 1-й группы после ОВГМ. Уровни микроРНК в плазме крови определялись с помощью RT-PCR с использованием syn-cel-miR-39 в качестве контроля. Ось Y предоставляет уровень экспрессии (ΔCt). Критерий Вилкоксона: * значение p<0,05; ** значение p<0,01
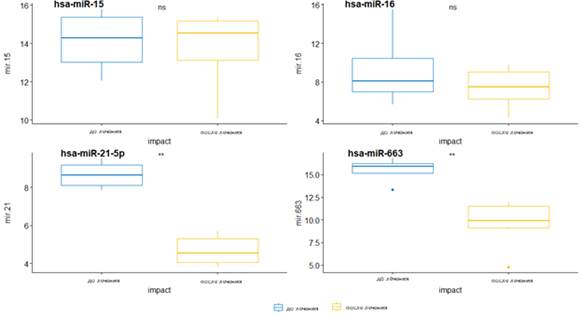
Рис. 2. Изменения уровней экспрессии микроРНК в плазме после лучевой терапии пациентов 2-й группы после SRS в самостоятельном варианте. Уровни микроРНК в плазме крови определялись с помощью RT-PCR с использованием syn-cel-miR-39 в качестве контроля.
Ось Y предоставляет уровень экспрессии (ΔCt).
Критерий Вилкоксона: * значение p<0,05; ** значение p<0,01
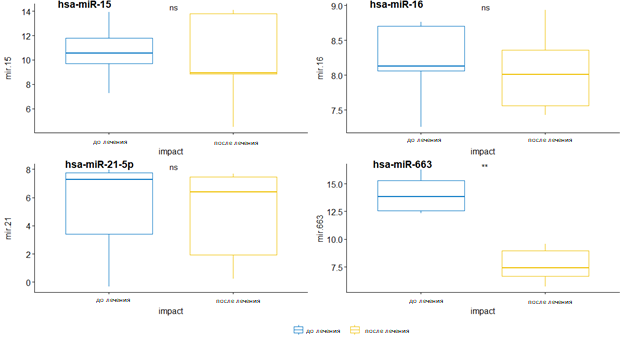
Рис. 3. Изменения уровней экспрессии микроРНК в плазме после лучевой терапии пациентов 3-й группы после SRS в комбинации с бевацизумабом. Уровни микроРНК в плазме крови определялись с помощью RT-PCR с использованием syn-cel-miR-39 в качестве контроля.
Ось Y предоставляет уровень экспрессии (ΔCt).
Критерий Вилкоксона: * значение p<0,05; ** значение p<0,01
Было проанализировано, связаны ли уровни экспрессии микроРНК в плазме крови с ответом на лучевую терапию. Для выявления микроРНК-кандидатов для прогностического классификатора были проведено сравнение уровней экспрессии исследуемых микроРНК в плазме крови пациентов до лечения внутри групп пациентов с положительным ответом (частичный ответ и стабилизация) на лечение и прогрессированием интракраниального процесса согласно критериям RANO, так как данные варианты ответа встречаются в исследовании в подавляющем большинстве.
В группе после проведенного ОВГМ при сравнении уровней экспрессии микроРНК у пациентов с положительным ответом (частичный ответ и стабилизация) на лечение и прогрессированием интракраниального процесса после проведенной лучевой терапии были выявлены отличия в уровнях экспрессии в плазме крови до лечения для микроРНК hsa-miR-15 (p=0,015) и hsa-miR-16 (p=0,013), также были отмечены статистически значимые изменения уровней микроРНК hsa-miR-21 и hsa-miR-663 (p=0,0103; 0,0097) после лечения. На основании этих данных можно предположить, что более низкие уровни микроРНК hsa-miR-15 (ΔCt ≤12,38) (p=0,015) и hsa-miR-16 (ΔCt ≤6,64) (p=0,016) могут быть связаны с положительным ответом на лечение в 1-й группе пациентов.
Для группы пациентов после стереотаксической радиохирургии в самостоятельном варианте производилось сравнение уровней экспрессии микроРНК у пациентов с положительным ответом (частичный ответ и стабилизация) на лечение и прогрессированием интракраниального процесса после проведенной стереотаксической радиохирургии. Была выявлена достоверная разница в уровне экспрессии для микроРНК hsa-miR-21 при исследовании до лечения (p=0,021) и для микроРНК hsa-miR-663 при исследовании как до лечения (p=0,027), так и после лечения (p=0,048). На основании этих данных можно предположить, что более высокий уровень микроРНК hsa-miR-21 (ΔCt ≥ 8,06) и низкий уровень hsa-miR-663 (ΔCt ≤16,06) перед лечением могут выступать прогностическими факторами частичного ответа на терапию.
При исследовании экспрессии у пациентов группы после стереотаксической радиохирургии с предварительным введением бевацизумаба производилось сравнение уровней экспрессии микроРНК у пациентов с положительным ответом (частичный ответ и стабилизация) на лечение и прогрессированием интракраниального процесса после проведенной комплексной терапии. Выявлено, что в случаях с положительным ответом до начала терапии отмечались достоверно более высокий уровень микроРНК hsa-miR-15 ΔCt ≥11,77 (p=0,0128), более высокий уровень hsa-miR-21 ΔCt ≥ 7,75 (p=0,013) и более низкий уровень микроРНК hsa-miR-663 ΔCt ≤13,82 (p=0,01). Данные микроРНК могут выступать потенциальными кандидатами для классификации пациентов 3-й группы лечения.
Заключение
Таким образом, в нашем исследовании выявлены характерные изменения экспрессии микроРНК hsa-miR-15a-5p, hsa- miR-16a-5p, hsa-miR-21-5p, hsa-miR-663, которые могут быть использованы в качестве биомаркеров прогноза ответа на различные варианты лучевой терапии метастатического поражения головного мозга немелкоклеточным раком легкого.
Библиографическая ссылка
Вошедский В.И., Дженкова Е.А., Сакун П.Г., Росторгуев Э.Е., Розенко Л.Я., Зброилова Е.С., Власов С.Г., Командиров М.А., Родионова О.Г., Карнаухова Е.А., Рогова Т.С. ВЛИЯНИЕ СТЕРЕОТАКСИЧЕСКОЙ РАДИОХИРУРГИИ НА ЭКСПРЕССИЮ МИКРОРНК В ПЛАЗМЕ КРОВИ ПАЦИЕНТОВ С МЕТАСТАТИЧЕСКИМ ПОРАЖЕНИЕМ ГОЛОВНОГО МОЗГА НЕМЕЛКОКЛЕТОЧНЫМ РАКОМ ЛЕГКОГО // Современные проблемы науки и образования. 2022. № 2. ;URL: https://science-education.ru/en/article/view?id=31636 (дата обращения: 18.05.2026).
DOI: https://doi.org/10.17513/spno.31636



