На фармацевтическом рынке России в мае 2018 г. импортные лекарственные препараты в натуральных единицах измерения составляли 40,5%, а в стоимостном выражении – 71% продаж [1, с. 5]. Средневзвешенная стоимость упаковки лекарства отечественного производства в мае 2018 г. составила 89,3 руб., а импортного – 320,7 руб. [1, с. 5]. Следовательно, расширение ассортимента лекарственных средств отечественного производства сделает лечение более доступным для населения в 3,5 раза.
По итогам 2017 г. на препараты для лечения заболеваний костно-мышечной системы (КМС) в коммерческом сегменте, который составляет 68% фармацевтического рынка, приходилось 109 млн упаковок натурального и 78,7 млрд руб. стоимостного объемов продаж [2, с. 11]. Таким образом, лекарственные препараты, направленные на лечение заболеваний костно-мышечной системы, являются одними из лидеров фармацевтического рынка, для которых характерен рост потребления. Актуальность данного направления на территории России видна и по статистике поисковых запросов на интернет-ресурсах Яндекс и Google в категории: «Заболевания. Проблемы со Здоровьем». Уровень интереса населения к таким проблемам, как боль и воспаление, достаточно высок, характеризуется большим количеством поисковых запросов. Динамика частотности данных запросов достаточно стабильна [3, 4].
Следует также отметить прогнозируемое различными организациями по всему миру дальнейшее увеличение числа людей с заболеваниями костно-мышечной системы в связи с увеличением среднего возраста населения [5, c. 628; 6, c. 2415], что также свидетельствует о возрастающей потребности в лекарственных препаратах этой группы.
Более 50% объема рынка препаратов для лечения заболеваний КМС как в натуральном, так и в стоимостном выражении занимают НПВП [3, c. 628; 7, с. 17]. На современном фармацевтическом рынке НПВП России преобладают дженерики. Оригинальные препараты занимают всего 1/4 сегмента. Десятка лидеров продаж НПВП представлена исключительно зарубежными производителями. Почти половина продаж ЛС изучаемого сегмента в денежном выражении приходится на препараты, производимые в странах Западной Европы, прежде всего, в Германии. Однако в натуральном выражении основной объем реализации приходится на препараты стран Азии, в частности Индии. Российские препараты обеспечивают всего 18,2% продаж в натуральном и 12,5% в стоимостном выражении [5, c. 628; 7, с. 17].
Для нашей разработки был выбран пироксикам, который показан для лечения воспалительных и дегенеративных заболеваний опорно-двигательного аппарата. Он является востребованным лекарственным средством и широко применяется в различных странах [6, с. 2415]. На сегодняшний день на российском фармацевтическом рынке широкого выбора этот препарат не имеет, что в какой-то мере может снижать его востребованность. Сравнительный анализ лекарственных форм свидетельствует об ограниченном применении жидких лекарственных форм, которые предпочтительнее для больных в некоторых возрастных группах [6, с. 2415]. В связи с этим нами была разработана суспензия пироксикама 0,5%-ная [8, c. 2036; 9, с. 155]. В качестве дисперсионной среды была взята вода очищенная.
Цель исследования. Анализ противовоспалительного, анальгетического и жаропонижающего действий суспензии пироксикама в эксперименте.
Материал и методы исследования. Исследование проводилось на 144 крысах – половозрелых самцах линии Wistar массой 220–240 г, полученных из вивария Пятигорского медико-фармацевтического института – филиала ФГБОУ ВО ВолгГМУ МЗ РФ, в соответствии с международными нормами экспериментальной этики. На каждом этапе оценки эффективности применения изучаемой суспензии пироксикама формировались равные экспериментальные группы по 6 особей в каждой. Дозы были выбраны с учетом межвидового коэффициента пересчета и составляли для капсул пироксикама 120 мг/кг. Суспензия пироксикама исследовалась в дозе из расчета 50 мг/кг. Препарат сравнения и изучаемая лекарственная форма пироксикама вводились интрагастрально через атравматический зонд. Группа животных негативного контроля (НК) не получала фармакологическую поддержку. Животным этой группы вводили 0,9%-ный натрия хлорид в эквиобъемном количестве [10, с 1267].
Острое воспаление у крыс воспроизводили путем субплантарного введения 0,1 мл 2%-ного раствора формалина. Исследуемая суспензия пироксикама и препараты сравнения вводились интрагастрально за 1 ч до введения формалина. Выраженность воспалительной реакции (отечность конечности) оценивали онкометрически по истечении 3 ч. На первом этапе исследования проводили определение концентрации С-реактивного белка (СРБ) как одного из маркеров воспалительного процесса. СРБ определяли полуколичественным методом с использованием стандартного набора реактивов производства компании «Арбис+» (Санкт-Петербург, Россия). Принцип метода основан на реакции взаимодействия СРБ сыворотки крови с фиксированными на поверхности латекс-частиц специфическими антителами к СРБ с образованием агглютинатов [10, с. 1267].
Хроническое пролиферативное воспаление (ХПВ) оценивали с использованием модели фетровой гранулемы. Крыс вводили в состояние наркоза хлоралгидратом (350 мг/кг) и имплантировали им под кожу живота 4 стерильных фетровых диска массой 10 мг каждый. Операция выполнялась с соблюдениями правил асептики. Исследуемую суспензию пироксикама и препараты сравнения вводили на протяжении 7 дней после воспроизведения ХПВ. На 8-е сутки определяли содержание лейкоцитов в крови с использованием системы ветеринарного автоматического гематологического анализатора BC – 2400 vet (Minray, КНР). Принцип определения основан на методе импеданса, который заключается в определении количества и размера клеток в зависимости от изменения электрического сопротивления при прохождении частицы (клетки) через маленькую апертуру [10, с. 1267]. После определения содержания лейкоцитов в асептических условиях под хлоралгидратной анестезией (350 мг/кг) у крыс извлекали фетровые диски с образовавшейся вокруг них грануляционной тканью и взвешивали. Затем диски высушивали до постоянной массы при 600С и снова взвешивали. Пролиферацию оценивали по разнице между массами высушенной гранулемы и исходного фетрового диска. Экссудативную реакцию оценивали по разнице между массой сырой и высушенной гранулемы [10, с. 1267].
Анальгетические свойства изучаемой суспензии пироксикама оценивали на модели формалиновой гиперальгезии у крыс. Экспериментальным животным субплантарно вводили 0,1 мл 2%-ного раствора формалина. Изменение порога болевой чувствительности оценивали по изменению максимального переносимого механического раздражения (давление на лапу животного – анальгезиметрия по типу Randall–Selitto) спустя 3 ч с момента введения альгогена. Критерием появления болевой реакции служила вокализация животного. Исследуемая суспензия и препараты сравнения вводились per os через 2 ч после введения формалина [10, с. 317].
Антипиретическую активность изучаемой суспензии пироксикама производили на модели дрожжевой лихорадки у крыс. Лихорадочную реакцию вызывали подкожным введением 20%-ной суспензии пекарских дрожжей. Ректальную температуру измеряли электротермометром до введения пирогена и далее ежечасно на протяжении суток. Исследуемая суспензия и препараты сравнения вводились на пике гипертермической реакции. Жаропонижающее действие оценивали по уменьшению ректальной температуры через 2 ч после введения изучаемой суспензии пироксикама и препаратов сравнения (дозы см. выше) [10, с. 1267].
Полученные в исследовании данные анализировали с использованием методов вариационной статистики и пакета прикладных программ STATISTICA 6.0 и Microsoft Excel 10-й версии. Нормальность распределения полученных данных оценивали при помощи критерия Шапиро–Уилка. Поскольку распределение данных было нормальным, для сравнения средних значений использовали t-критерий Стьюдента [10, с. 1512].
Результаты исследования и их обсуждение. В ходе оценки противовоспалительной активности 0,5%-ной суспензии пироксикама на модели острой воспалительной реакции установлено, что субплантарное введение формалина вызывает у крыс выраженную отечность конечности, о чем свидетельствует повышение объема воды, вытесняемого при погружении в емкость лапы животных, не получавших фармакологическую поддержку, на 59,6% (p<0,05) по сравнению с интактными крысами (рис. 1). Применение капсул пироксикама значимого влияния на течение острого воспалительного процесса не оказало (рис. 2) (статистически значимых отличий по сравнению с НК группой крыс не установлено), в то время как на фоне введения изучаемой суспензии пироксикама величина отечности конечности крыс по сравнению с группой животных негативного контроля уменьшилась на 30,4% (p<0,05).

Рис. 1. Влияние исследуемой 0,5%-ной суспензии пироксикама и препарата сравнения на течение острой воспалительной реакции у крыс
В условиях хронического пролиферативного воспаления у крыс группы негативного контроля показатели экссудации и пролиферации составляли 0,758±0,146 ед. и 0,278±0,033 ед. соответственно, что статистически значимо относительно интактных животных (t-критерий Стьюдента с поправкой Бонферрони, p<0,05).
При этом у НК группы животных концентрации С-реактивного белка (рис. 2) и лейкоцитов (рис. 3) в крови превышали аналогичные показатели интактных животных в 14,2 раза (p<0,05) и 3,5 раза (p<0,05) соответственно.
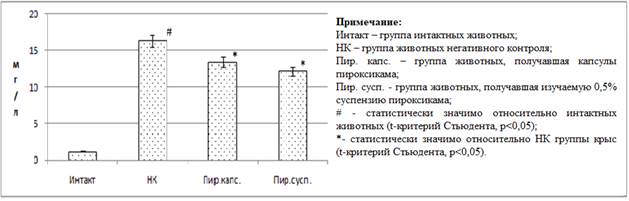
Рис. 2. Изменение концентрации СРБ в плазме крови крыс в условиях коррекции хронического воспалительного процесса изучаемой суспензией пироксикама и препаратами сравнения
Применение суспензии пироксикама на фоне хронического воспаления способствовало уменьшению выраженности экссудативного процесса на 77,9% и пролиферативного процесса в 2,4 раза по сравнению с НК группой крыс (t-критерий Стьюдента с поправкой Бонферрони, p<0,05). Показатели экссудации и пролиферации на фоне приема суспензии составляли 0,426±0,122 ед. и 0,117±0,05 ед.
Кроме того, у животных при введении суспензии пироксикама концентрация СРБ уменьшилась относительно НК группы крыс на 34% (p<0,05), при этом содержание лейкоцитов в крови снизилось на 61,9% (p<0,05).
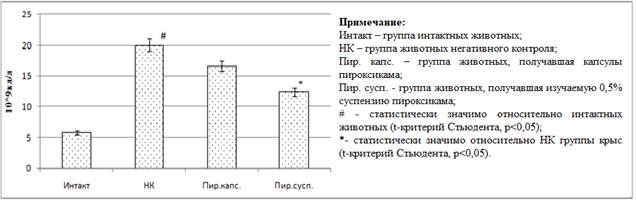
Рис. 3. Влияние изучаемой суспензии пироксикама и препаратов сравнения на выраженность лейкоцитоза в условиях хронического воспаления
Применение капсул пироксикама способствовало уменьшению показателя экссудации до 0,488±0,059. Полученный результат статистически значим относительно НК группы крыс согласно t-критерию Стьюдента с поправкой Бонферрони, p<0,05. Пролиферация составила 0,278±0,033 ед., однако по сравнению с НК группой крыс статистической значимости этого показателя не установлено. Концентрация С-реактивного белка на фоне применения капсул пироксикама по сравнению с НК группой животных снизилась на 21,8% (p<0,05).
Исследование анальгетической активности разработанной суспензии пироксикама показало, что порог болевой чувствительности (рис. 4) у интактных крыс составлял 229,8±4,11 г. У группы животных негативного контроля данный показатель был ниже на 174,7% (p<0,05).

Рис. 4. Изменение порога болевой чувствительности при коррекции ноцицептивной реакции изучаемой суспензией пироксикама и препаратами сравнения
На фоне введения капсул пироксикама в условиях острой болевой реакции ноцицепция у крыс снизилась по сравнению с НК группой животных на 109,4% (p<0,05). При применении исследуемой суспензии пироксикама отмечено уменьшение болевой реакции относительно группы животных негативного контроля на 184,2% (p<0,05).
При исследовании жаропонижающей активности разработанной суспензии пироксикама было установлено, что температура тела (рис. 5) у группы интактных животных составляла 36,97±0,0670С.
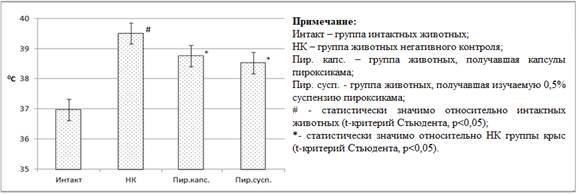
Рис. 5. Влияние изучаемой суспензии пироксикама и препаратов сравнения на изменение температуры тела крыс в условиях гиперпиретической реакции
При введении пиретического агента у группы животных негативного контроля пик подъема температуры отмечен спустя 3 ч от момента введения пирогена, температура тела при этом составила 39,5±0,110С, таким образом, рост температуры тела у животных НК группы составил +2,530С (p<0,05). В то же время при коррекции гипертермии посредством введения капсул пироксикама и изучаемой суспензии пироксикама температура тела крыс составила 38,75±0,1260С и 38,52±0,0870С, что было ниже аналогичного показателя групп животных негативного контроля на 0,750С (p<0,05) и 0,980С (p<0,05) соответственно.
Заключение. Проведенная сравнительная оценка суспензии пироксикама в отношении ее фармакологических свойств показала, что по величине противовоспалительной активности изучаемая 0,5%-ная суспензия пироксикама превосходит существующий, взятый в качестве сравнительного объекта, препарат «Пироксикам капсулы». Аналогичная тенденция изменений была отмечена и при оценке влияния изучаемой суспензии пироксикама на течение хронического воспалительного процесса, а также при исследовании анальгетических и жаропонижающих свойств 0,5%-ной суспензии пироксикама.
Библиографическая ссылка
Илькевич Е.В., Воронков А.В., Степанова Э.Ф., Поздняков Д.И., Кулешова С.А. ФАРМАКОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА ОРИГИНАЛЬНОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ ПИРОКСИКАМА В ЭКСПЕРИМЕНТЕ // Современные проблемы науки и образования. 2021. № 3. ;URL: https://science-education.ru/en/article/view?id=30813 (дата обращения: 21.04.2026).
DOI: https://doi.org/10.17513/spno.30813



