Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
COMPARATIVE ANALYSIS OF LEFT VENTRICULAR SEGMENTAL CONTRACTILITY USING ECHOCARDIOGRAPHY AND SINGLE-PHOTON EMISSION COMPUTED TOMOGRAPHY IN SILENT MYOCARDIAL ISCHEMIA
Наличие безболевой ишемии миокарда (ББИМ) повышает риск внезапной сердечной смерти, нарушений ритма сердца, инфаркта миокарда и застойной сердечной недостаточности [1, 2]. Важной функциональной характеристикой сердца является региональная сократимость левого желудочка (ЛЖ), ее определение уточняет характер и возможные причины поражения миокарда, помогает спланировать тактику ведения пациента [3–4]. Обнаружено, что у пациентов с ББИМ по сравнению с больными с безболевыми эпизодами нарушения локальной сократимости более выражены: они выявлялись чаще, захватывали большее количество сегментов [5]. Для оценки регионарной сократимости ЛЖ обычно используются эхокардиография (ЭХОКГ) или однофотонная эмиссионная компьютерная томография (ОЭКТ). Сравнение результатов ЭХОКГ и ОЭКТ помогает понять сопоставимость получаемых с их помощью данных [6].
Цель исследования. Определить возможность сопоставления методов ЭХОКС и ОЭКТ в определении регионарной сократимости миокарда ЛЖ у пациентов с ББИМ, выявить наличие различий при использовании этих методов. На основе анализа полученных результатов предложить вариант сравнения данных ЭХОКС и ОЭКТ.
Материал и методы исследования. Среди пациентов с ББИМ выделена группа из 27 пациентов с подтвержденной БББИМ, которым в одну госпитализацию проводились ЭХОКС и ОЭКТ (покой/нагрузка) и по данным ЭХОКС не было обнаружено нарушений региональной сократимости. Средний возраст больных составил 57,7±6,16 года, из них 4 женщины (14,8%) и 23 (85,2%) мужчины. У 18 пациентов (66,7%) была полностью ББИМ (I тип), у 9 (33,3%) пациентов – сочетание болевых и безболевых эпизодов (II тип). 10 (37%) пациентов имели в анамнезе перенесенный ИМ, 20 (74%) – артериальную гипертензию, 3 (11,1%) пациентов страдали СД II типа.
При проведении ОЭКТ использовалась 19-сегментная модель ЛЖ, при проведении ЭХОКГ – 16-сегментная модель. По шкале оценки сегментарной сократимости ЛЖ выделяют следующие варианты: нормальная сократимость или гиперкинез – 1 балл, гипокинез – 2 балла, акинез или минимальное утолщение – 3 балла, дискинез (парадоксальное систолическое движение) – 4 балла, аневризма (диастолическая деформация) – 5 баллов [7]. При суммировании баллов для всех сегментов и делении на число визуализированных сегментов можно получить индекс регионарной сократимости (ИРС) миокарда.
С целью прямого сопоставления результатов анализа сегментарной сократимости по данным ОЭКТ и ЭХОКГ нами предложен перевод 19-сегментной модели ЛЖ в объединенную 16-сегментную модель (рис. 1). Выбор 16-сегментной модели в качестве основной определяется следующими причинами: 1) деление апикального уровня миокарда на 6 сегментов приводит к резкой несопоставимости анатомических размеров сегментов базального и апикального уровня, при этом теряется практический смысл расчета индекса сегментарной сократимости; 2) деление апикального уровня миокарда в 16-сегментной модели в целом соответствует распределению кровоснабжения от коронарных артерий; 3) исключение верхушки (19-го сегмента) связано с его полной функциональной зависимостью от смежных апикальных сегментов; 4) отсутствие выхода верхушки (19-го сегмента) на эндокардиальную поверхность ЛЖ делает в принципе невозможной оценку его подвижности в баллах. Выделение верхушки в самостоятельный сегмент нецелесообразно, поскольку ее кровоснабжение и сократимость определяются смежными апикальными сегментами. Как правило, сократимость верхушки определяется передним, септальным и боковым апикальными сегментами. Изолированных нарушений сократимости верхушки при сохранении сократимости перечисленных смежных сегментов нами выявлено не было. Таким образом, сегменты с 1-го по 12-й и их баллы по оценке сократимостипереводятся из 19-сегментной модели в объединенную 16-сегментную модель без изменений. Сегменты 14 и 15 из 19-сегментной модели объединяются в сегмент 14 в 16-сегментной модели, а сегменты 16 и 17 из 19-сегментной модели объединяются в сегмент 16 в 16-сегментной модели. При расчете индекса сократимости баллы сегментов 14 и 15 из 19-сегментной модели переводятся как среднее арифметическое в баллы сегмента 14 в 16-сегментной модели, а баллы сегментов 16 и 17 из 19-сегментной модели переводятся как среднее арифметическое в баллы сегмента 16 в 16-сегментной модели.
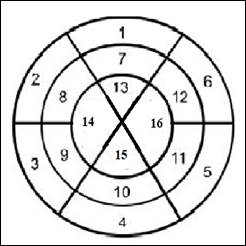
Рис. 1. Объединенная 16-сегментарная модель ЛЖ. Базальные сегменты: 1 – передней; 2 – передне-септальный; 3 – нижне-септальный; 4 – нижний; 5 – нижнебоковой; 6 – переднебоковой. Медиальные сегменты: 7 – передний; 8 – передне-септальный; 9 – нижне-септальный; 10 – нижний; 11 – нижнебоковой; 12 – переднебоковой. Апикальные сегменты: 13 – передний; 14 – септальный; 15 – нижний; 16 – боковой
Следует подчеркнуть, что предлагаемая модель позволяет сохранить в рамках одного объединенного сегмента характер кровоснабжения двух объединяемых сегментов. В объединенной 16-сегментной модели сегменты ЛЖ верно соотносятся с бассейном кровоснабжения коронарных артерий в зависимости от вариантов коронарного кровообращения (рис. 2). При этом возникает возможность прямого сопоставления различных инструментальных показателей, связанных с сегментарной сократимостью ЛЖ.
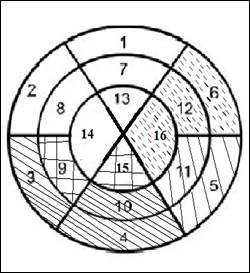
Рис. 2. Распределение коронарного кровообращения в объединенной 16-сегментной модели. Сегменты 1, 2, 7, 8, 13, 14 – ПНА; 6,12,16 – ОА или ПНА; 5,11 – ОА или ПКА; 3, 4, 10 – ПКА; 9, 15 – ПКА или ПНА
Вместе с тем объединенная 16-сегментная модель имеет свои особенности, требующие учета. В частности, апикальные сегменты 14 и 16 превосходят по размерам сегменты 13 и 15. Кроме того, перевод баллов сократимости из двух сегментов в один в форме среднего арифметического создает дробность получаемых значений. Практическое применение модели показало, что разница между объединяемыми сегментами (14-м и 15-м; 17-м и 18-м) никогда не превышала 1 балла, составляя пары значений: 1–1 (76%), 2–2 (9,2%), 1–2 (14,8%). Следовательно, разница между результирующим баллом объединенного сегмента (среднее арифметическое по двум объединяемым сегментам) и исходным баллом каждого из объединяемых сегментов никогда не превышала 0,5 балла. Иначе говоря, объединение сегментов по такому принципу не приводит к необоснованному завышению или занижению сократимости объединенного сегмента по сравнению с каждым из исходных сегментов. Это позволяет использовать балл объединенного сегмента наряду с баллами других сегментов для расчета ИРС как среднего арифметического по всем сегментам.
Нарушения региональной сократимости в заключениях по ОЭКТ и ЭХОКГ часто имеют описательный характер, поэтому нами предложена и была использована следующая система оценки нарушений сократимости: нормокинезия и гиперкинезия – 1 балл; умеренная гипокинезия – 2 балла, выраженная гипокинезия и гипо-акинезия – 3 балла, акинезия – 4 балла, парадоксальное систолическое движение (дискинезия) – 5 баллов. Из полученных значений в баллах рассчитывался ИРС, эквивалентный классическому ИРС, как среднее арифметическое по объединенной 16-сегментной модели, однако имеющий больший разброс значений с учетом введения дополнительной градации в 5 баллов. Статистическая обработка проведена с использованием лицензионного программного обеспечения «Statistica» (StatSoft, Inc.), различия считались достоверными при p<0,05.
Результаты исследования и их обсуждение. Метод ЭХОКГ у части пациентов с подтвержденной ББИМ может давать ложноотрицательные результаты в 51,8% случаев по сравнению с более углубленной ОЭКТ. У 13 из 27 пациентов с нормальной регионарной сократимостью по ЭХОКГ на ОЭКТ в покое были выявлены нарушения. Эти случаи включали 11 мужчин и 2 женщин в возрасте51–71 лет (средний возраст 59 лет), у 9 из которых была ББИМ 1-го типа и у 4 – ББИМ 2-го типа. В 8 случаях имелся ПИКС, в 10 случаях – артериальная гипертония, в 3 – случаях сахарный диабет.
Средние значения ИРС по объединенной 16-сегментной модели в группе составили: по ЭХОКС – 1, по ОЭКТ – 1,28±0,32 (от 1,06 до 2,00). Доля сегментов со сниженной сократимостью на ОЭКТ варьировала в отдельных случаях от 6,25% до 100%, составляя в среднем 18,58±24,97%. Расхождение значений ИРС по ЭХОКГ (1,00) и ОЭКТ варьировало от 1,75 до 2,67, составляя в среднем 2,23±0,56. Расхождения встречались во всех сегментах, но чаще в 14-м (апикальном септальном) и в 16-м (апикальном боковом) – по 38,46%.
В группе из 13 человек оценка сократимости по отдельным сегментам в баллах показала следующее. В базальных сегментах среднее расхождение варьировало от 1,08±0,28балла (сегменты 1, 6) до 1,61±1,16 балла (сегмент 3), составив в среднем по базальным сегментам1,28±0,34 балла. В сегментах, имевших расхождения, оценка в баллах по ОЭКТ варьировала от2(умеренный гипокинез – сегменты 1, 5, 6) до3баллов (выраженный гипокинез – сегмент 2), в среднем составив 2,36±0,36балла. В медиальных сегментах среднее расхождение варьировало от 1,08±0,28 балла (сегмент 7) до 1,54±0,97балла (сегмент 9), составив в среднем по медиальным сегментам1,24±0,30 балла. В сегментах, имевших расхождения, оценка в баллах по ОЭКТ варьировала от2(умеренный гипокинез – сегменты 7, 10, 11, 12) до3баллов (выраженный гипокинез – сегмент 8), составив в среднем 2,29±0,45балла. В апикальных сегментах среднее расхождение варьировало от 1,23±0,60(сегмент 15) до 1,42±0,64балла (сегмент 14), составив в среднем по апикальным сегментам 1,34±0,36 балла. В сегментах, имевших расхождения, оценка в баллах по ОЭКТ варьировала от1,80±0,36 балла (сегмент 16) до2,67±0,34балла (сегмент 13), составив в среднем 2,26±0,39балла.
Также проводился анализ сегментарной сократимости и перфузии по результатам ОЭКТ (табл. 1).
Таблица 1
Сопоставление сократимости и перфузии по сегментам у пациентов с ББИМ
|
Варианты сочетаний* |
Сегменты |
n |
|||||||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
||
|
1 |
4 |
5 |
5 |
5 |
6 |
8 |
9 |
10 |
8 |
8 |
9 |
10 |
6 |
7 |
7 |
7 |
114 |
|
2 |
– |
– |
3 |
3 |
1 |
– |
– |
1 |
– |
1 |
– |
– |
1 |
– |
– |
– |
10 |
|
3 |
8 |
6 |
4 |
4 |
5 |
4 |
3 |
1 |
1 |
2 |
2 |
1 |
4 |
1 |
4 |
1 |
51 |
|
4 |
1 |
2 |
1 |
1 |
1 |
1 |
1 |
1 |
4 |
2 |
2 |
2 |
2 |
5 |
2 |
5 |
33 |
Примечание: * 1 – нормальная сократимость и нормальная перфузия, 2 – нарушенная сократимость и нарушенная перфузия, 3 – нарушение сократимости при нормальной перфузии, 4 – нормальная сократимость при нарушенной перфузии.
Несовпадения сократимости и перфузии миокарда ЛЖ были обнаружены у всех пациентов. Число сегментов с расхождениями от 2 до 16 в среднем составило 2,62±1,31сегмента. Из 208 сегментов у 13 пациентов чаще всего встречалось совпадение нормальной сократимости и нормальной перфузии (54,8% случаев), совпадение нарушенной сократимости с нарушенной перфузией – в 4,8% случаев, нарушение сократимости при нормальной перфузии – в 24,5% случаев, нормальная сократимость при нарушенной перфузии – в 15,9% сегментов (рис. 3). Разница в группах с различными вариантами сочетаний сократимости и перфузии, определенная по методу Хи-квадрат, была достоверна, p<0,05.
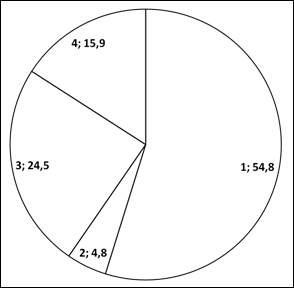
Рис. 3. Показатели сегментарной сократимости и перфузии по ОЭКТ: 1 – совпадение нормальной сократимости и перфузии (%); 2 – совпадение сниженной сократимости и перфузии (%); 3 – снижение сократимости при нормальной перфузии (%); 4 – нормальная сократимость при сниженной перфузии (%)
Расхождение оценок сократимости и перфузии, выявленное более чем в 1/3 сегментов (35,4%), не может быть случайным. Нормальная сократимость при сниженной перфузии (26,6%) может быть связана с тем, что исследование проводилось в состоянии покоя, без нагрузки на миокард. Сегменты со сниженной сократимостью при нормальной перфузии (8,9%) могут иметь некоронарную природу выявленных нарушений.
Сегменты с совпадением нормальной сократимости и перфузии выявлялись у всех пациентов, но их доля варьировала от 87,5% (14 сегментов) до 25,0% (4 сегмента). Из них пациенты, имевшие такое совпадение не менее чем в половине всех сегментов, составили 58,3%. Сегменты со сниженной сократимостью при нормальной перфузии имелись у 83,3% пациентов. Сегменты с сохраненной сократимостью при сниженной перфузии имелись в 75,0% случаев. Совпадение сниженной сократимости и перфузии выявлено у 42,7% больных (рис. 4).
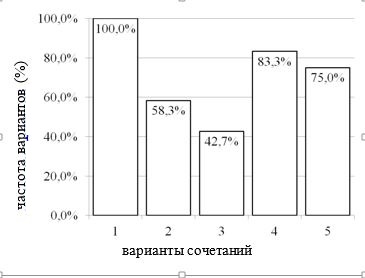
Рис. 4. Частота вариантов сочетаний сократимости и перфузии по ОЭКТ.
1 – совпадение нормальной сократимости и перфузии; 2 – совпадение нормальной сократимости и перфузии не менее чем в половине всех сегментов; 3 – совпадение сниженной сократимости и перфузии; 4 – сниженная сократимость при нормальной перфузии; 5 – нормальная сократимость при сниженной перфузии
Нами разработана и успешно применена для сопоставления данных ЭХОКГ и ОЭКТ объединенная 16-сегментная модель, которая позволила провести сопоставление данных локальной сократимости ЛЖ и предложить методику проведения исследования. Мы учитывали, что нет необходимости выделения верхушки как отдельного сегмента, учитывая особенности ее кровоснабжения и сократимости.
У пациентов с ББИМ метод ЭХОКГ может давать ложноотрицательные результаты локальной сократимости ЛЖ в более чем половине случаев по сравнению с данными ОЭКТ. Доля сегментов со сниженной сократимостью на ОЭКТ варьировала в широких пределах, при этом расхождения в апикальных септальном и боковом сегментах были наиболее частыми. В базальных, средних и апикальных сегментах максимальное среднее расхождение было в 3-м и 9-м нижне-септальных и в 14-м септальном сегментах; в сегментах, имевших расхождения, выраженный гипокинез обнаружен во 2-м и 8-м сегментах (передне-септальных) и в 13-м переднем сегменте. Таким образом, обнаружено, что данные локальной сократимости по результатам ЭХОКС и ОЭКТ в большей мере различаются в перегородочной области (2-й, 3-й, 8-й ,9-й, 14-й сегменты) с захватом 13-го переднего апикального сегмента.
Проведенное сопоставление данных локальной сократимости и перфузии по объединенной 16-сегментной модели в виде числа сегментов со следующими признаками: совпадение нормальной сократимости и перфузии, нарушение сократимости при нормальной перфузии, нормальная сократимость при нарушении перфузии, совпадение нарушений сократимости и перфузии – показало, что те или иные изменения в разной мере выявляются у всех пациентов. Обнаружены несовпадения сократимости и перфузии миокарда ЛЖ от 2-го до 16-го сегментов. Несовпадение данных ЭХОКС и ОЭКТ выявлено в виде нарушение сократимости при нормальной перфузии в 24,5% сегментов, нормальная сократимость при нарушенной перфузии – в 15,9% сегментов.
Обоснованное исключение данного случая изменило распределение вариантов нарушения изучаемых показателей в форме перевеса в сторону группы с нормальной сократимостью при нарушенной перфузии – в 26,6% сегментов и уменьшения в группе с нарушением сократимости при нормальной перфузии – в 8,9% сегментов.
Существует необходимость продолжения нашего исследования, следующим этапом планируются использование предложенной нами методики сопоставления методов ЭХОКС и ОЭКТ у пациентов с ББИМ на большей группе, сопоставление данных ЭХОКС и ОЭКТ с результатами других методов исследования.
Выводы. Разработана и успешно опробована объединенная 16-сегментная модель деления миокарда ЛЖ, которая может быть использована для прямого сопоставления результатов ЭХОКГ, ОЭКТ и КАГ. Она может позволить, при невозможности проведения всех трех исследований, с высокой долей вероятности предвидеть изменения на недостающих методах исследования. У пациентов с ББИМ метод ЭХОКГ может давать ложноотрицательные результаты по сравнению с более углубленным исследованием ОЭКТ более чем у половины больных. С использованием предложенной модели установлено расхождение сократимости по ЭХОКГ и ОЭКТ по всем сегментам, чаще в 14-м (апикальном септальном) и в 16-м (апикальным боковом).В базальных, медиальных и апикальных сегментах средние значения максимального расхождения были в септальных сегментах. В сегментах, имевших расхождения, более выраженный гипокинез обнаружен в базальном и медиальном передне-септальных сегментах и в переднем апикальном сегменте.
На ОЭКТ обнаружено расхождение сократимости и перфузии миокарда по 2 и более сегментам (до 16 сегментов) у всех пациентов группы. Сегменты, имевшие снижение сократимости при нормальной перфузии, составили 24,5%, а имевшие нормальную сократимость при сниженной перфузии – 15,9%. Анализ обоих показателей позволяет расширить возможности дифференциальной диагностики некоронарных поражений.
Библиографическая ссылка
Абдрахманова А.И., Амиров Н.Б., Цибулькин Н.А., Сайфуллина Г.Б. СРАВНИТЕЛЬНЫЙ АНАЛИЗ СЕГМЕНТАРНОЙ СОКРАТИМОСТИ ЛЕВОГО ЖЕЛУДОЧКА ПО ДАННЫМ ЭХОКАРДИОГРАФИИ И ОДНОФОТОННОЙ ЭМИССИОННОЙ КОМПЬЮТЕРНОЙ ТОМОГРАФИИ ПРИ БЕЗБОЛЕВОЙ ИШЕМИИ МИОКАРДА // Современные проблемы науки и образования. 2021. № 2. ;URL: https://science-education.ru/en/article/view?id=30748 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.30748



