Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
EFFECT MOLECULAR OSMOLYTES WEIGHT ON OSMOTIC DECREASE OF CORNEAL MATRIX
Роговица образует переднюю часть внешней оболочки глаза и выполняет двойную функцию защиты внутреннего содержимого глаза, а также является основным преломляющим оптическим элементом глаза, который обеспечивает фокусировку видимого света на сетчатке. Роговица состоит в основном из трех слоев: наружного слоя, содержащего эпителий, среднего стромального слоя и внутреннего слоя эндотелиальных клеток. Строма, или матрикс, образует основную часть структурного каркаса роговицы и составляет примерно 80-85% ее толщины. Она состоит из кератоцитов, регулярно расположенных коллагеновых фибрилл и межфибриллярного пространства, содержащего гликозаминогликаны.
Нарушение содержания воды в строме (в норме ∼78% от веса) изменяет диаметр и расположение коллагеновых волокон, что является критическим для прозрачности роговицы [1; 2]. При нарушении светопроводимости роговицы наиболее распространенным методом восстановления способности видеть является кератопластика. В настоящее время усилия исследователей направлены на уменьшение риска отторжения трансплантата. Развиваются новые способы высокоточных разрезов тканей донора и реципиента с помощью фемтолазеров, усовершенствуются методы хранения и консервации ткани.
В глазу осмотический баланс матрикса роговицы определяется динамическим равновесием выведения и поступления воды и осмолитов в строму. Эти процессы часто описывают с помощью так называемого механизма Pump-Leak транспорта осмолитов и воды. Поступление воды в матрикс (leak) происходит пассивно согласно проницаемости эндотелия для воды и осмолитов и градиенту осмотического давления между матриксом и жидкостью в передней камере глаза. Удаление воды из матрикса (pump) обусловлено Na, K-ATФазой и системой, включающей транспорт HCO3-, Cl-, а также активность карбоангидраз клеток эндотелия [3]. Оба процесса определяются функцией клеток эндотелия роговицы. Эндотелий (задний эпителий) роговицы представляет собой монослой гексагональных клеток на внутренней поверхности роговицы и является одной из наиболее метаболически активных тканей организма. Показано, что клетки эндотелия роговицы человека заблокированы в G1 фазе клеточного цикла и по этой причине не проходят митотическое деление. Клетки эндотелия роговицы поляризованы, апикальная и базолатеральная плазматические мембраны имеют свою специализацию. Апикальная поверхность обращена в переднюю камеру глаза и участвует в оттоке жидкости из стромы роговицы. Базальная поверхность обращена к десцеметовой мембране. В глазу поступление воды в матрикс зависит от водной проницаемости монослоя клеток эндотелия, а формирование градиента осмотического давления определяется интенсивностью энергозависимого транспорта в этих клетках [4].
В качестве материала для трансплантации используют препараты донорской роговицы из глазных банков, где они исследуются на пригодность к трансплантации и затем хранятся в консервационной среде при пониженной температуре (холодовая консервация) [5-7]. Нарушение осмотического баланса роговицы ведет к изменению характеристик донорской роговицы, что влияет на возможность ее использования при разных видах кератопластики. При холодовой консервации водно-электролитный обмен в роговице остановлен, поскольку определяется транспортными механизмами клеток эндотелия, которые подавлены при пониженной температуре. Остановка насосной функции эндотелия приводит к установлению осмотического равновесия ткани со средой консервации и сопровождается набуханием препарата. В этой связи для улучшения результатов трансплантации становится важным восстановление нормального объема донорской роговицы (десвеллинг).
Цель исследования. В настоящей работе была поставлена цель исследовать возможность осмотического десвеллинга консервированных препаратов роговицы с использованием осмотических агентов разного молекулярного веса.
Материал и методы исследования. Исследование проводилось на дисках роговицы свиньи диаметром 8,0 мм. Иссечение сквозных дисков осуществлялось трепаном 8,0 мм через 6-8 часов после забоя животных. Иссеченные диски роговицы сохраняли 7-14 суток при температуре 4 °С в консервационной среде Eusol-C (Alchimia, Италия).
В качестве осмотических агентов для создания градиента осмотического давления использовали хлорид натрия, маннитол, сахарозу и декстран 500 (молекулярный вес 500 000). В экспериментах диск роговицы инкубировали в гипертоническом растворе, который создавали на основе PBS (табл. 1).
Таблица 1
Состав раствора PBS
|
Компоненты |
NaCl |
Na2HPO4 |
KCl |
KH2PO4 |
MgCl2 |
Глюкоза |
CaCl2 |
|
mM |
137,0 |
4,7 |
2,7 |
1,5 |
0,5 |
5,5 |
1,0 |
Для создания осмотического градиента в PBS вносили: NaCl – 400 mM, что дает осмотическую концентрацию 800 mOsm/kg, маннитол – 200 mM (200 mOsm/kg), сахарозу – 200 mM (200 mOsm/kg), декстран 500 – 0,08 mM (0,08 mOsm/kg) (табл. 2).
Таблица 2
Молекулярные веса используемых осмотических агентов
|
Осмотический агент |
Молекулярный вес (г/М) |
|
NaCl |
58,44 |
|
Маннитол |
182,18 |
|
Сахароза |
342,3 |
|
Декстран 500 |
500 000 |
Определение скорости изменения толщины диска роговицы проводили по методу, описанному ранее [8]. В основе метода лежит изменение освещенности, которое коррелирует с длиной оптического пути в окрашенной среде. Иссеченный диск роговицы помещается в инкубационную камеру, его положение фиксируется. В инкубационную среду вносится гемоглобин до оптической плотности 2,0 OU на длине волны 540 nm. В процессе инкубации измеряется оптическая плотность системы: диск роговицы и среда на фиксированном оптическом пути (рис. 1).
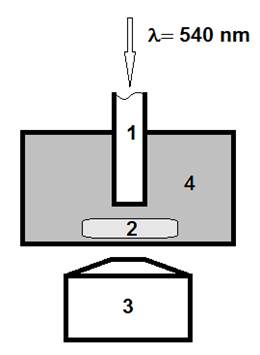
Рис. 1. Измерительная камера. 1 – световод, 2 – препарат роговицы, 3 – микроскоп, 4 – окрашенная гипертоническая среда
При внесении осмотического агента в инкубационную камеру происходит изменение толщины роговицы. При снижении толщины диска роговицы увеличивается длина оптического пути в окрашенной среде, что приводит к изменению освещенности. Свет регистрировали с помощью фотоприемника на основе ФЭУ-71, оборудованного полевой диафрагмой для измерения интенсивности проходящего света в центральной области роговичного диска. Измерения производили с помощью цифрового осциллографа АСК-3102 («Актаком»®, Россия) с записью на компьютер.
Для оценки достоверности различий независимых выборок применяли t-критерий Стьюдента. Все величины выражены как M±SEM, n – количество препаратов роговицы.
Процедура исследования соответствовала стандартам Этического комитета Хельсинкской декларации 1975 г. и ее пересмотру в 1983 г.
Результаты исследования и их обсуждение. Результаты экспериментов по осмотическому снижению объема матрикса роговицы показали значительное влияние молекулярной массы использованных в работе агентов на начальную скорость десвеллинга. Эффективность осмотического агента, если ее определять по начальной скорости снижения толщины матрикса, значительно возрастает с увеличением его молекулярной массы (рис. 2).
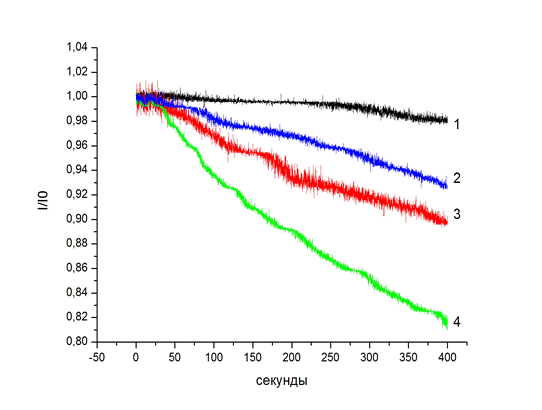
Рис. 2. Динамика снижения толщины роговицы в гипертонической среде. Типичный график, (условные единицы). Оси: абсцисс – время (секунды), ординат – I/I0 относительная интенсивность проходящего света. 1 – NaCl 800 mOsm/kg; 2 – декстран 500 – 0,08 mM (0,08 mOsm/kg); 3 – маннитол – 200 mM (200 mOsm/kg); 4 – сахароза – 200 mM (200 mOsm/kg)
В наших экспериментах время записи процесса снижения объема матрикса роговицы было ограничено 400 секундами. На протяжении этого периода вид экспериментальных кривых позволяет принять характер динамики снижения линейным. Коэффициенты регрессии при линейной аппроксимации экспериментальных кривых были использованы для оценки начальной скорости осмотического снижения объема матрикса роговицы (µ/s): NaCl (800 mOsm/kg) R=0,25±0,02; маннитол (200 mOsm/kg) R=0,97±0,01; сахароза (200 mOsm/kg) R=1,49±0,02; декстран 500 (0,08 mOsm/kg) R = 0,77±0,01 (n=4). Различия между любыми двумя коэффициентами достоверны с уровнем p <0,05.
Приведенные результаты указывают на то, что молекулярный вес осмотического агента имеет исключительно большое значение для эффективности процесса осмотического снижения объема. Скорость снижения объема матрикса роговицы в среде декстрана 500 при градиенте 0,08 mOsm/kg выше примерно в 3 раза по сравнению со скоростью снижения в среде, где хлоридом натрия создана значительно более высокая концентрация осмотического агента. Скорость осмотического снижения объема определяется скоростью диффузионного выхода воды из матрикса роговицы, который по своей структуре ближе к гелю и не имеет ограничивающей полупроницаемой мембраны, на которой может формироваться ступенчатый градиент осмотического давления, как это происходит на плазматической мембране клетки. В случае с матриксом роговицы осмотический градиент формируется в свободной среде и подвержен диффузионному размыванию во времени. Повышение эффективности осмотического агента, связанное с повышением его молекулярного веса, можно объяснить тем, что молекулярный вес органических соединений коррелирует с размерами молекулы, что в сферическом приближении определяет ее коэффициент диффузии согласно формуле D= kT (6πhr)-1, где k – постоянная Больцмана, Т – температура, h – вязкость среды, r – радиус молекулы.
Подвижность молекул осмотического агента влияет на величину осмотического градиента и, соответственно, величину движущей силы, определяющей выход воды из матрикса. С точки зрения диффузионных процессов матрикс роговицы можно представить гелем, что означает то, что градиент формируется в жидкости и находится в обратной зависимости от подвижности молекул осмолита. В наших экспериментах влияние осмотического размывания градиента можно видеть, если сравнить скорости снижения толщины роговичных дисков (µ/s) относительно концентраций осмотических агентов (mOsm/kg): NaCl – 3,13E-04; маннитол – 4,85E-03; сахароза – 7,45E-03; декстран 500 – 9,63E+00. Из приведенных оценок можно видеть, что повышение эффективности декстрана как осмотического агента по сравнению с хлоридом натрия составляет 4 порядка, что пропорционально соотношению их молекулярных весов.
Заключение. При гипотермической консервации роговицы происходит ее значительное утолщение преимущественно за счет отека стромы. Это приводит к существенному различию по толщине между роговицей реципиента и донора. Возникающая разница по толщине накладывает ограничения на использование отечной роговицы при некоторых видах кератопластики (кератопластика с профильными разрезами), при выполнении разрезов отечной донорской роговицы с помощью фемтолазеров. Кроме того, значительная разница по толщине затрудняет адаптацию края трансплантата и края роговицы реципиента, что в свою очередь приводит к усложнению хирургических манипуляций, к ранним и поздним послеоперационным осложнениям. Десвеллинг консервированной донорской роговицы способен в значительной степени устранить эти проблемы. Анализируя результаты наших экспериментов, можно сказать, что повышение молекулярного веса и, соответственно, размера молекул осмотического агента эффективно повышает осмотический градиент даже при более низких концентрациях в среде. Осмотическое снижение объема препарата роговицы несет в себе риск повреждения клеток эндотелия, т.к. воздействие гипертонической среды на клетки может вызывать их апоптоз [9]. В этой связи следует отметить, что предпочтительнее выбор осмотического агента для десвеллинга с возможно более высоким молекулярным весом, что снизит риск апоптоза, поскольку позволит использовать среду с более низкой осмотической концентрацией.
Резюмируя, можно отметить, что полученные в работе результаты кинетики десвеллинга консервированной донорской роговицы могут быть полезны для разработки методов осмотического восстановления объема препарата, повышая его пригодность для трансплантации.
Работа поддержана бюджетным проектом № 0259-2021-0016 и грантами Российского фонда фундаментальных исследований № 20-015-00147; № 19-08-00874.
Библиографическая ссылка
Батурина Г.С., Каткова Л.Е., Кузовлева М.А., Кузеина И.М., Смирнов Е.С., Соленов Е.И., Пальчикова И.Г., Искаков И.А. ВЛИЯНИЕ МОЛЕКУЛЯРНОГО ВЕСА ОСМОЛИТОВ НА ОСМОТИЧЕСКОЕ СНИЖЕНИЕ ОБЪЕМА МАТРИКСА РОГОВИЦЫ // Современные проблемы науки и образования. 2021. № 2. ;URL: https://science-education.ru/en/article/view?id=30705 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.30705



