Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
A CLINICAL CASE OF TREATMENT OF A PATIENT WITH BOWMAN'S REIS-BUCKLERS MEMBRANE DYSTROPHY BY INVERTED TOPOGRAPHY-GUIDED PHOTOREFRACTIVE KERATECTOMY
Общеизвестно, что дистрофия боуменовой мембраны 1-го типа связана с мутацией в гене TGFB1 короткого плеча 5-й хромосомы, кодирующего кератоэпителин, и наследуется по аутосомно-доминантному типу [1–3]. Впервые это наследственное заболевание роговицы было описано в 1917 г. В. Рейсом, а в 1949 г. – М. Бюклерсом [4]. Оба доктора при биомикроскопии переднего отрезка глаз своих пациентов отметили нарушение прозрачности роговицы в виде отложений белесовато-серого цвета в поверхностных слоях роговицы, а также задумались о семейном наследовании этой патологии, так как была выявлена закономерность встречаемости аналогичной клинической картины у близких родственников пациентов [5]. Дальнейшее изучение данного заболевания установило причину его возникновения, характер наследования, клинические особенности его течения, диагностические критерии в постановке диагноза и определило сложность его лечения [6].
В связи с этим при встрече с пациентом, страдающим дистрофией Рейса–Бюклерса, перед офтальмологом стоит трудная задача – поиск рационального решения в устранении помутнения роговицы, повлекшего за собой снижение остроты и качества зрения, как правило, у трудоспособного и социально активного пациента, с целью получения максимально возможных высоких зрительных функций.
На сегодняшний день наиболее оптимальными способами хирургического лечения дистрофии боуменовой мембраны Рейса–Бюклерса являются проведение фоторефрактивной кератэктомии (ФРК), выполнение послойной или сквозной кератопластики в зависимости от выраженности помутнения роговицы [3, 7, 8, 9]. Основной целью используемых методов является удаление зоны помутнения с формированием гладкой роговичной поверхности с получением хороших зрительных функций [7, 10]. Однако при использовании представленных способов хирургического лечения существует нерешенная проблема – отсутствие воздействия на этиопатогенетическое звено развития дистрофии боуменовой мембраны Рейса–Бюклерса. Следовательно, не исключается возможность рецидивирующего характера данного заболевания, что требует повторного хирургического лечения или поиска нового способа борьбы с ним. Также весьма вероятно возникновение и других послеоперационных проблем, например высокого риска отторжения роговичного трансплантата, низкой некорригированной остроты зрения, обусловленной посткератопластической аметропией [11, 12, 13]. При попытке выполнения операции ФРК хирурги сталкиваются с рядом проблем, обусловленных наличием иррегулярности, асимметрии и помутнения роговой оболочки, а также с тем, что эпителий роговицы при нарушении прозрачности в ее поверхностных слоях скрывает иррегулярность стромы и боуменовой мембраны. Следовательно, выполнение стандартного сферического алгоритма абляции при данных изменениях роговицы не всегда эффективно. В связи с этим наиболее оправданным методом устранения иррегулярности роговицы является проведение топографически ориентированной ФРК (ТОФРК) [14]. Вместе с тем традиционный метод выполнения ТОФРК подразумевает получение кератотопографического снимка, расчет параметров операции, механическую скарификацию эпителия с обнажением боуменовой мембраны и выполнение абляции по заранее рассчитанному алгоритму. При дистрофии Рейса–Бюклерса отмечается иррегулярность боуменовой мембраны, частично компенсированная неравномерным нарастанием эпителия. В связи с этим традиционный алгоритм выполнения ТОФРК может привести к низкой прогнозируемости рефракционного результата. В отделе лазерной хирургии ФГАУ НМИЦ «МНТК “Микрохирургия глаза им. акад. С.Н. Федорова”» МЗ РФ накоплен богатый опыт выполнения инвертированной ТОФРК у пациентов с иррегулярностью роговицы различной этиологии [15], позволяющей успешно решать задачи ремоделирования роговицы у пациентов со стромальной иррегулярностью, компенсированной эпителием, за счет замены последовательности проведения этапов операции (сначала проводится топографически-ориентированный этап ФРК с абляцией по данным кератотопограммы, затем – абляция роговицы «плоским фронтом», конгруэнтным поверхности роговицы, без рефракционного эффекта на глубину ранее измеренной средней толщины эпителия). Технология получила название инвертированной ТОФРК (ИТОФРК), она позволяет достичь высокой зрительно-функциональной реабилитации пациентов после проведения хирургической коррекции рефракционных нарушений за счет использования дифференцированного подхода в два этапа [16].
В данном контексте интерес представляет следующий клинический случай лечения пациента с дистрофией боуменовой мембраны Рейса–Блюкерса при помощи ИТОФРК.
Цель исследования. Оценить клинико-функциональные результаты проведения ИТОФРК у пациента с дистрофией боуменовой мембраны Рейса–Блюкерса.
Материал и методы исследования. Под наблюдением находился пациент Б. 33 лет с диагнозом «билатеральная дистрофия боуменовой мембраны Рейса–Блюкерса». Со слов пациента, основной его жалобой являлось снижение остроты зрения на оба глаза в течение последних 10 лет, что и послужило поводом для обращения в отдел рефракционной лазерной хирургии МНТК «Микрохирургия глаза», где на основании семейного анамнеза и типичной клинической картины и был установлен диагноз. Для устранения рефракционных нарушений и помутнения роговицы было принято решение о проведении ИТОФРК сначала на левом глазу, а потом – на правом (с учетом более низкой остроты зрения левого глаза).
Для определения возможности проведения хирургического лечения пациента Б. ему был выполнен комплекс общеофтальмологических (проверка остроты зрения вблизи и вдали в естественных условиях и в условиях медикаментозного мидриаза, измерение ВГД, авторефрактометрия, исследование полей зрения, А- и В-сканирование, офтальмоскопия с исследованием центральных и периферических областей глазного дна), а также специальных (кератопография и исследование на Шеймпфлюг-камере, оптическая когерентная томография (ОКТ) переднего отрезка глаза с анализом эпителиальной карты, оценка количественной (тест Ширмера-1) и качественной (неинвазивное время разрыва слезной пленки) слезопродукции, инфракрасная мейбография и оценка состояния эпителия при окрашивании витальными красителями) методов исследования.
Операция проводилась на эксимерлазерной установке «Микроскан-Визум» (ООО «Оптосистемы», Россия). Для расчета параметров операции использовали программу «КераСкан» (ООО «Оптосистемы», Россия). Первым этапом проводили топографически ориентированную абляцию, затем абляцию плоским фронтом до полного удаления остатков эпителия в пределах центральной и парацентральной зон диаметром 7,5 мм. После завершения операции инстиллировали антисептик и накладывали бандажную контактную линзу. Медикаментозная коррекция включала инстилляции антисептика до завершения эпителизации (на 4-е сутки), а в дальнейшем – применение стероидных противовоспалительных средств по убывающей схеме с 6 до 1 раза в течение 2,5 месяца с профилактическим назначением гипотензивного препарата и слезозаместителей.
Результаты исследования и их обсуждение. На момент дооперационного обследования были получены следующие данные: Vis OD= 0.2 н/к; Vis OS= 0.08 sph + 3.75 D cyl – 8.0 D ax 10 ° = 0.2.
При биомикроскопии на оба глаза визуализировалось диффузное мелкоточечное помутнение роговицы белесоватого цвета (рис. 1), видимая влага передней камеры прозрачна, передняя камера средней глубины, глубжележащие среды без видимой патологии. Тест Ширмера-1 до 15 мм на OD и до 16 мм на OS, время разрыва слезной пленки на OU до 5–6 с. При окрашивании витальными красителями определили точечное прокрашивание эпителия в центральной зоне роговицы. Инфракрасная мейбография свидетельствовала об отсутствии активности 30–35% мейбомиевых желез.
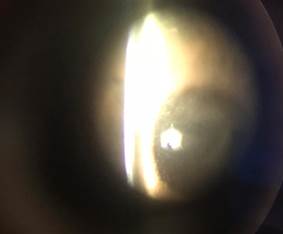
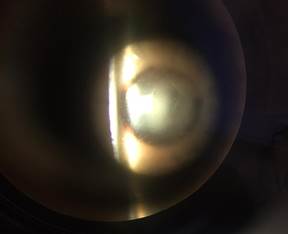
Рис. 1. Биомикроскопия переднего отрезка OU: диффузное мелкоточечное помутнение роговицы белесоватого цвета
Наличие синдрома сухого глаза испарительного типа и эпителиопатии не позволило провести корректное исследование кератотопографических данных, необходимых для расчета параметров ИТОФРК, поскольку известно, что состояние слезной пленки и эпителия роговицы критически важно для проведения кератотопографии на приборах, основанных на анализе колец Плачидо, что потребовало проведения предоперационной подготовки пациента с коррекцией состояния глазной поверхности (рис. 2).
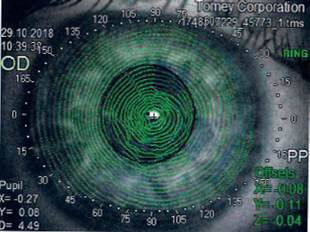
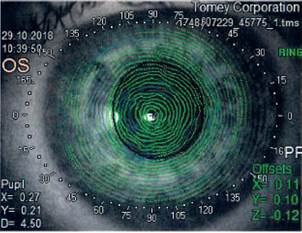
Рис.2. Кератотопограмма OU: оценка состояния слезной пленки
В качестве подготовки к хирургическому лечению пациенту был рекомендован курс терапевтической гигиены век с гелем Теагель, содержащим вещество полоксамер 188, растворяющим пробки в устьях мейбомиевых желез и удаляющим корочки, остатки липидов и эпителиальных клеток с оснований ресниц, а также инстилляции слезозаместителей на основе трегалозы – вещества, обеспечивающего наряду с увлажнением осмокоррекцию и биопротекцию эпителиальных клеток (Теалоз 4 раза в день) в течение месяца. Повторное исследование состояния функционального слезного комплекса позволило подтвердить благотворное влияние предшествующей терапии на ранее исследованные параметры – неинвазивное время разрыва слезной пленки составило более 14 сек, количество нефункционирующих мейбомиевых желез уменьшилось до 10%, а прокрашивания эпителия роговицы не отмечалось, что позволило провести кератотопографическое исследование и в дальнейшем рассчитать параметры ИТОФРК. Кроме того, известно, что синдром сухого глаза является неблагоприятным фоном для проведения операции на роговице по технологии ФРК в силу потенциального усугубления ситуации в послеоперационном периоде, что подтверждает необходимость предоперационной фармакологической подготовки при планировании хирургии.
Данные кератотопограммы (рис. 3), полученные после нормализации состояния глазной поверхности, свидетельствовали об асимметрии роговицы (индекс асимметрии – 4.02 на OD и 3.32 на OS). На ОКТ переднего отрезка глаз (рис. 4) была видна зона диффузного утолщения роговицы 646 мкм на OD и 634 мкм на OS, отмечалась неравномерность переднего эпителия в центральной зоне.
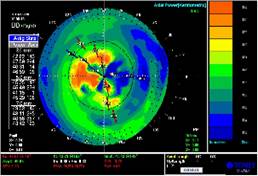
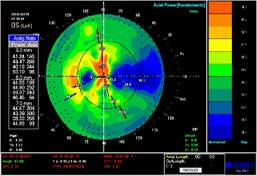
Рис.3. Кератотопограмма : индекс асимметрии – 4.02 на OD и 3.32 на OS
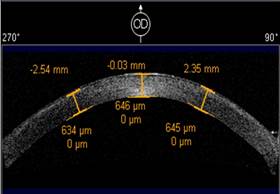
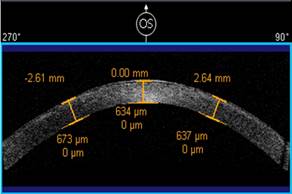
Рис. 4. ОКТ переднего отрезка OU: зона диффузного утолщения роговицы 646 мкм на OD и 634 мкм на OS
Для достижения оптимальных зрительно-функциональных результатов на OS была проведена ИТОФРК. Фармакологическое сопровождение операции было стандартным и включало назначение местного антисептика – р-ра пиклоксидина 0,05% (Витабакт), обладающего широкой противомикробной, а также противогрибковой и противовирусной активностью, с целью профилактики инфекционных осложнений 4 раза в день на 1 неделю. Стероидный противовоспалительный препарат (р-р дексаметазона 0,1%) был назначен начиная с 4-х суток послеоперационного периода после завершения реэпителизации на 10 недель по нисходящей схеме, начиная с 6 раз в день; слезозаместители с учетом дооперационного нарушения состояния глазной поверхности и хронического течения дистрофии были рекомендованы для постоянного применения в виде инстилляций р-ра трегалозы (Теалоз) 3–6 раз в сутки.
Результаты диагностических исследований через 1 месяц после операции: Vis OS=0,5. При биомикроскопии OS, представленной на рисунке 5А, роговица и влага передней камеры прозрачны, в зоне проведенной операции отмечена регуляризованная реэпителизация, передняя камера средней глубины, радужка структурна, зрачок правильной формы, хрусталик и стекловидное тело прозрачны, диск зрительного нерва бледно-розовый, границы четкие, сосуды нормального калибра, макулярная зона и периферия без особенностей. Данные кератотопограммы (рис. 5В) показали уменьшение асимметрии роговицы после выполнения ИТОФРК (индекс асимметрии – 1.44 на OS). Согласно данным ОКТ, было отмечено практически полное устранение помутнения роговицы и регуляризации эпителия роговицы (рис. 5С).
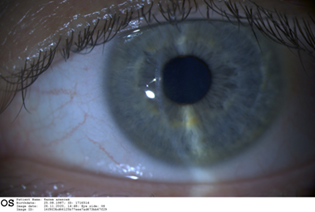
Рис. 5А. Биомикроскопия переднего отрезка OS
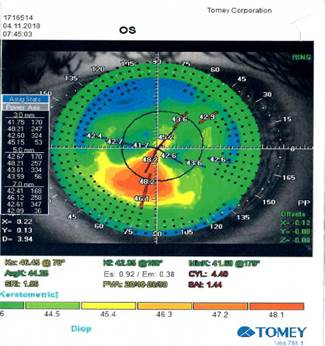
Рис. 5В. Кератотопограмма OS: индекс асимметрии – 1.44 на OS
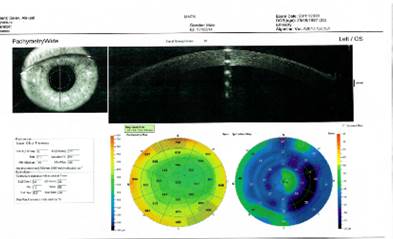
Рис .5 С. ОКТ переднего отрезка, эпителиальная карта OS
Заключение. Таким образом, проведение дооперационной фармакологической коррекции состояния глазной поверхности улучшило состояние слезной пленки и эпителия роговицы, что повысило качество кератотопографического исследования и дало возможность рассчитать параметры топографически-ориентированной кератоабляции. Выполнение ИТОФРК позволило достичь высокого зрительно-функционального результата с устранением помутнения и иррегулярности роговицы, а также провести коррекцию сопутствующих рефракционных нарушений. Однако, поскольку не исключен рецидивирующий характер течения дистрофии, требуются динамическое наблюдение за состоянием левого глаза и выполнение аналогичной рефракционной операции на правом глазу.
Библиографическая ссылка
Мушкова И.А., Майчук Н.В., Образцова М.Р. КЛИНИЧЕСКИЙ СЛУЧАЙ ЛЕЧЕНИЯ ПАЦИЕНТА С ДИСТРОФИЕЙ БОУМЕНОВОЙ МЕМБРАНЫ РЕЙСА–БЮКЛЕРСА С ПОМОЩЬЮ ИНВЕРТИРОВАННОЙ ТОПОГРАФИЧЕСКИ ОРИЕНТИРОВАННОЙ ФОТОРЕФРАКТИВНОЙ КЕРАТЭКТОМИИ // Современные проблемы науки и образования. 2021. № 1. ;URL: https://science-education.ru/en/article/view?id=30538 (дата обращения: 21.05.2026).
DOI: https://doi.org/10.17513/spno.30538



