Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
CONTROL OF JUSTIFICATION FOR PHARMACOTHERAPY IN PSYCHIATRIC HOSPITAL PATIENTS WITH FRAILTY SYNDROME
Старческая астения представляет собой синдром, сопровождающийся снижением функциональной активности организма пожилого человека, связанным с возрастными изменениями. Особую актуальность имеет тот факт, что в результате старческой астении снижается сопротивляемость организма различным факторам, приводящим к неблагоприятным событиям [1]. К таким факторам можно отнести нерациональную лекарственную терапию, которая может не только не принести пользу пожилому пациенту, но и значительно повысить риски неблагоприятных лекарственных реакций в пожилом возрасте. В то же время подобная терапия способна приводить к прогрессированию гериатрических синдромов, что может иметь приоритетное значение для больных с синдромом старческой астении.
Осуществление лекарственной терапии пожилым пациентам должно проводиться с учетом всех особенностей данной возрастной группы. Имеющаяся мультиморбидность диктует необходимость назначения большого количества лекарственных препаратов и ведет к полипрагмазии. Физиологические изменения стареющего организма также могут приводить к повышению риска развития побочных эффектов фармакотерапии, а повышение количества потенциальных межлекарственных взаимодействий – к снижению безопасности лечения. Особую осторожность следует соблюдать у пожилых людей с психической патологией. Соматическая и психическая коморбидность усложняет лечение [2], а само наличие хронической психической патологии увеличивает риск неблагоприятных лекарственных явлений [3]. Некоторые психические заболевания у пациентов пожилого возраста, такие как деменция, могут быть предиктором назначения потенциально не рекомендованных лекарственных препаратов [4], в то время как при психотропной терапии увеличивается частота таких назначений [5]. Учитывая вышеперечисленные аспекты, а также длительность лечения психических заболеваний, представляется актуальным контроль рациональности фармакотерапии у пациентов психиатрического стационара с синдромом старческой астении.
Цель исследования – оценка возможностей контроля рациональности фармакотерапии у пациентов психиатрического стационара с синдромом старческой астении.
Материалы и методы исследования
В исследование были включены 52 пациента психиатрического стационара старше 65 лет, имеющие в листах назначений 5 и более лекарственных препаратов, один из которых относится к категориям «Психолептики» или «Психоаналептики» в соответствии с международной АТХ-классификацией. Для выявления синдрома старческой астении был произведен скрининг включенных в исследование пациентов с использованием опросника «Возраст не помеха», рекомендуемый для первичной диагностики обсуждаемого синдрома методическими рекомендациями МР103 «Фармакотерапия у лиц пожилого и старческого возраста» и клиническими рекомендациями «Старческая астения» [1]. Подобный подход в диагностике считается эффективным инструментом в зарубежном здравоохранении [6].
Для оценки рациональности лекарственной терапии было использовано несколько инструментов. Одной из задач исследования явилась оценка риска развития неблагоприятных лекарственных реакций с помощью шкалы The GerontoNet ADR Risk Score [7, 8] ввиду того, что наличие пожилого возраста, а также имеющаяся у больных полипрагмазия являются важными факторами риска возникновения побочных эффектов фармакотерапии. С этой же целью был применен и другой инструмент – ADRROP (Adverse Drug Reaction Risk in Older Persons), также рекомендуемый для прогнозирования лекарственных осложнений у пожилых [9, 10].
С целью оценки рациональности фармакотерапии и выявления потенциально не рекомендованных назначений нами был применен инструмент «STOPP/START критерии» (Screening Tool of Older People’s Prescriptions/Screening Tool to Alert to Right Treatment) [11, 12], рекомендуемый к применению у пациентов со старческой астенией для борьбы с полипрагмазией и повышения безопасности лечения [1].
Ввиду возраст-ассоциированного снижения холинергической передачи и наличия у значительного числа нейротропных препаратов антихолинергических свойств, что может привести к развитию побочных эффектов, нами был проведен анализ антихолинергической нагрузки с помощью шкалы Anticholinergic Cognitive Burden Scale [13, 14] и перечня «Лекарственные средства с высоким антихолинергическим потенциалом», представленного в критериях Бирса – инструмента по борьбе с полипрагмазией, утвержденного в 2019 г. Американской гериатрической ассоциацией [15].
Статистическая обработка проводилась с оценкой нормальности распределения с помощью критерия Колмогорова–Смирнова–Лиллиефорса, а также критерия Манна–Уитни и непараметрического критерия Хи-квадрат Пирсона при использовании программного обеспечения AnalystSoft Inc., StatPlus:mac, версия 7.3.3.0.
Результаты исследования и их обсуждение
Для проведения исследования были проанализированы медицинские карты пациентов психиатрического стационара старше 65 лет. Средний возраст пациентов исследуемой группы – 76,27 (±7,28) года, 30 женщин (71,2%) и 22 мужчины (28,8%). Диагноз «Другие психические расстройства, обусловленные повреждением и дисфункцией головного мозга или соматической болезнью» был поставлен 20 пациентам (38,46%), «Деменция при других болезнях, классифицированных в других рубриках» – 15 пациентам (28,85%), «Сосудистая деменция» – 12 пациентам (23,08%), «Шизофрения» – 5 пациентам (9,62%). Среднее количество назначенных лекарственных препаратов составило 8,35 (±2,53).
Все больные были разделены на 2 равные группы: 26 пациентов с синдромом старческой астении и 26 без такового. В первой группе средний возраст составил 81,12 (±5,35) года, во второй – 71,42 (±5,54) года со средним количеством лекарственных препаратов 8,38 (±2,79) и 8,31 (±2,30) соответственно.
В первую очередь у пациентов был рассчитан суммарный балл риска развития неблагоприятных лекарственных реакций с выделением факторов его развития с помощью специальной валидированной шкалы для пожилых пациентов The GerontoNet ADR Risk Score. Медиана суммарного балла для пациентов со старческой астенией составила 5,0, интерквартильный размах – от 4,0 до 7,0, для пациентов без изучаемого синдрома – 5,5, интерквартильный размах – от 3,25 до 6,75. Статистически значимой разницы суммарного балла между группами сравнения обнаружено не было. Количество пациентов и частота встречаемости определенного балла представлены в таблице 1.
Таблица 1
Частота встречаемости суммарного балла риска шкалы The GerontoNet ADR Risk Score
|
Количество баллов у пациентов по шкале GerontoNet |
Пациенты с синдромом старческой астении: n (%) |
Пациенты без синдрома старческой астении: n (%) |
Всего: n (%) |
|
0 баллов |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
1 балл |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
2 балла |
0 (0,00%) |
1 (3,85%) |
1 (1,92%) |
|
3 балла |
5 (19,23%) |
6 (23,08%) |
11 (21,15%) |
|
4 балла |
4 (15,38%) |
3 (11,54%) |
7 (13,46%) |
|
5 баллов |
5 (19,23%) |
3 (11,54%) |
8 (15,38%) |
|
6 баллов |
4 (15,38%) |
6 (23,08%) |
10 (19,23%) |
|
7 баллов |
6 (23,08%) |
5 (19,23%) |
11 (21,15%) |
|
8 баллов |
1 (3,85%) |
2 (7,69%) |
3 (5,77%) |
|
9 баллов |
1 (3,85%) |
0 (0,00%) |
1 (1,92%) |
|
10 баллов |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
Итого |
26 (100,00%) |
26 (100,00%) |
52 (100,00%) |
Анализ факторов риска, включенных разработчиками в шкалу The GerontoNet ADR Risk Score, показал следующие результаты. Переменная «4 и более заболеваний и (или) состояний» (1 балл) встретилась у всех 52 пациентов психиатрического профиля. Фактор «Хроническая сердечная недостаточность» (1 балл) был зафиксирован у 76,92% пациентов с синдромом старческой астении и у 84,62% больных без указанного синдрома. «Количество назначенных лекарственных средств: 8 и более» (4 балла) – у 53,85% и 57,69% пациентов соответственно, «Количество назначенных лекарственных средств: 5–7» – у 46,15% и 42,31%, «Заболевания печени» – у 26,92% и 15,38%, «Неблагоприятная лекарственная реакция в анамнезе» – у 3,85% и 7,69% пациентов соответственно. Фактор «Количество назначенных лекарственных средств: менее 5» не мог быть зафиксирован ввиду дизайна исследования. Статистически значимую разницу между пациентами со старческой астенией и без нее удалось обнаружить при выявлении фактора «Почечная дисфункция», который оценивался с помощью расчета скорости клубочковой фильтрации с применением формулы Chronic Kidney Disease Epidemiology Collaboration equation (CKD-EPI). Пациентов с синдромом старческой астении, у которых была нарушена функция почек, было в 2 раза больше, чем больных без синдрома: 53,85% против 26,92% (p<0,05).
Оценка риска развития неблагоприятных лекарственных реакций также была проведена с помощью другого инструмента – ADRROP (Adverse Drug Reaction Risk in Older Persons). Медиана балла по шкале ADRROP у пациентов с синдромом старческой астении составила 14,0, интерквартильный размах – от 11,25 до 14,0, у пациентов без старческой астении – 11,0, интерквартильный размах – от 8,25 до 12,0. Разница между группами оказалась статистически значимой (p<0,05). Количество пациентов и соответствующая частота суммарного балла представлены в таблице 2.
Таблица 2
Частота встречаемости суммарного балла риска шкалы ADRROP
|
Количество баллов у пациентов по шкале ADRROP |
Пациенты с синдромом старческой астении: n (%) |
Пациенты без синдрома старческой астении: n (%) |
Всего: n (%) |
|
0 баллов |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
1 балл |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
2 балла |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
3 балла |
0 (0,00%) |
1 (3,85%) |
1 (1,92%) |
|
4 балла |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
5 баллов |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
6 баллов |
0 (0,00%) |
1 (3,85%) |
1 (1,92%) |
|
7 баллов |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
8 баллов |
1 (3,85%) |
5 (19,23%) |
6 (11,54%) |
|
9 баллов |
4 (15,38%) |
4 (15,38%) |
8 (15,38%) |
|
10 баллов |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
11 баллов |
2 (7,69%) |
7 (26,92%) |
9 (17,31%) |
|
12 баллов |
3 (11,54%) |
3 (11,54%) |
6 (11,54%) |
|
13 баллов |
0 (0,00%) |
1 (3,85%) |
1 (1,92%) |
|
14 баллов |
11 (42,31%) |
2 (7,69%) |
13 (25,00%) |
|
15 баллов |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
16 баллов |
0 (0,00%) |
1 (3,85%) |
1 (1,92%) |
|
17 баллов |
2 (7,69%) |
1 (3,85%) |
3 (5,77%) |
|
18 баллов |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
19 баллов |
2 (7,69%) |
0 (0,00%) |
2 (3,85%) |
|
20 баллов |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
21 балл |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
22 балла |
1 (3,85%) |
0 (0,00%) |
1 (1,92%) |
|
23 балла |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
24 балла |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
25 баллов |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
26 баллов |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
27 баллов |
0 (0,00%) |
0 (0,00%) |
0 (0,00%) |
|
Итого |
26 (100,00%) |
26 (100,00%) |
52 (100,00%) |
Изучение частоты встречаемости факторов риска осложнений фармакотерапии, предложенных разработчиками шкалы ADRROP, выявило следующее. «Возраст старше 70 лет», указанный в валидированной шкале в качестве одного из предикторов нежелательных побочных реакций лекарственных средств у пожилых пациентов, был обнаружен у всех пациентов с синдромом старческой астении и только у половины без такового (p<0,05). Среди пациентов с указанным гериатрическим синдромом 88,46% имели фактор «Необходимость в помощи ≥ 1 раз для осуществления повседневной активности», в то время как среди больных без синдрома данная переменная встретилась у 30,77% (p<0,05). Однако пожилым пациентам указанной группы чаще назначались 2 и более лекарственных препарата, потенциально не рекомендованных пожилым пациентам в соответствии с критериями STOPP/START: 65,38% против 42,31%, тогда как фактор «Наличие в листе назначений одного потенциально не рекомендованного лекарственного препарата из перечня STOPP/START критериев» чаще наблюдался у пациентов с синдромом старческой астении – 46,15% и 26,92% соответственно. Также обнаружилось незначительное преобладание у пациентов с изучаемым синдромом таких переменных риска, как «≥ 4 сопутствующих заболеваний», «Нарушения функции печени» и «Расчетная скорость клубочковой фильтрации <30 мл/мин/1,73 м2». Фактор «Женский пол» распределился между группами поровну, что составило 57,69% для каждой.
На основании данных, представленных разработчиками шкалы ADRROP, нами все пациенты были распределены на 4 подгруппы в зависимости от риска развития нежелательной побочной реакции. Данное распределение представлено на рисунке.
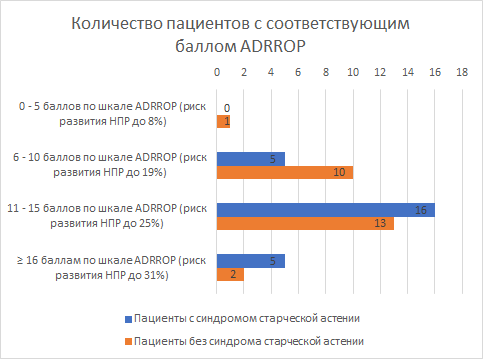
Риск развития неблагоприятных лекарственных реакций в зависимости от количества баллов по шкале ADRROP
Следующим этапом контроля рациональности фармакотерапии у стационарных больных психиатрического профиля было изучение частоты и структуры упомянутых в предыдущем инструменте потенциально не рекомендованных лекарственных препаратов в соответствии с критериями STOPP/START. Анализ показал, что 94,23% пациентов получали подобные препараты, всего было зафиксировано 99 таких назначений. Статистически значимой разницы между группой с синдромом старческой астении и контрольной группой обнаружено не было.
Инструмент по выявлению потенциально не рекомендованных лекарственных средств STOPP/START классифицирует критерии по разделам в зависимости от систем органов и тканей, фармакологических групп препаратов и последствий их воздействия. Подобное распределение в нашем исследовании выглядит следующим образом. «Раздел К. Препараты, которые предсказуемо увеличивают риск падений у пожилых людей» – 54 назначения (54,55%), «Раздел D: Центральная нервная система и психотропные препараты» – 29 назначений (29,29%), «Раздел В: Сердечно-сосудистая система» – 9 назначений (9,09%), «Раздел J. Эндокринная система» – 3 назначения (3,03%), «Раздел N: Антимускариновые/Антихолинергические препараты» – 3 назначения (3,03%), «Раздел С: Антиагреганты/Антикоагулянты» – 1 назначение (1,01%).
С точки зрения практической значимости наибольшее значение для клиницистов будет иметь информация о конкретных потенциально не рекомендованных назначениях, что должно позволить оптимизировать лекарственную терапию. Частота встречаемости STOPP-критериев представлена в таблице 3.
Таблица 3
Частота встречаемости STOPP-критериев у пожилых пациентов психиатрического стационара
|
Screening Tool of Older Persons’ Prescriptions (STOPP). Препараты, назначение которых нежелательно пациентам в возрасте 65 лет и старше |
Пациенты с синдромом старческой астении: n (%) |
Пациенты без синдрома старческой астении: n (%) |
|
Нейролептики (могут привести к нарушению ходьбы, паркинсонизму) |
18* (69,23%) |
24 (92,31%) |
|
Фенотиазины в качестве терапии первой линии, так как существуют более безопасные и эффективные альтернативы. Фенотиазины производят седативный эффект, обладают значительным антимускариновой токсичностью у пожилых людей, за исключением прохлорперазина (в настоящее время не зарегистрирован в РФ) для лечения тошноты/рвоты/головокружения, хлорпромазина для купирования стойкой икоты, левомепромазина как противорвотного препарата в паллиативной помощи |
4* (15,38%) |
12 (46,15%) |
|
Бензодиазепины (седативное действие, может привести к снижению чувствительности, ухудшать баланс) |
4 (15,38%) |
8 (30,77%) |
|
Антихолинергические/антимускариновые препараты для лечения экстрапирамидных побочных эффектов, связанных с приемом нейролептиков (риск антихолинергической токсичности) |
4 (15,38%) |
5 (19,23%) |
|
Терапия диуретиками для лечения АГ при недержании мочи (усиление симптомов недержания) |
6* (23,08%) |
0 (0,00%) |
|
Препараты сульфонилмочевины с длительной продолжительностью действия (например, глибенкламид, хлорпропамид (в настоящее время не зарегистрирован в РФ), глимепирид) при сахарном диабете 2-го типа (риск длительной гипогликемии) |
2 (7,69%) |
1 (3,85%) |
|
Одновременное применение двух или более препаратов с антимускариновыми/антихолинергическими свойствами (например, спазмолитики мочевого пузыря, кишечника, трициклические антидепрессанты, антигистаминные препараты первого поколения) (риск увеличения антимускариновой/антихолинергической токсичности) |
0 (0,00%) |
3 (11,54%) |
|
Антихолинергические/антимускариновые препараты у больных с делирием или деменцией (риск прогрессирования когнитивных нарушений) |
2 (7,69%) |
0 (0,00%) |
|
Антагонисты альдостерона (спиронолактон, эплеренон) в комбинации с калийсберегающими препаратами (например, ИАПФ, БРА, амилорид (в настоящее время не зарегистрирован в РФ), триамтерен) без контроля уровня калия в сыворотке (риск развития тяжелой гиперкалиемии> 6,0 ммоль/л; К+ в сыворотке следует контролировать регулярно, по крайней мере, каждые 6 месяцев) |
2 (7,69%) |
0 (0,00%) |
|
Антигистаминные препараты первого поколения (широко доступны менее токсичные и более безопасные антигистаминные препараты) |
0 (0,00%) |
2 (7,69%) |
|
НПВС в комбинации с антитромбоцитарными препаратами без профилактического назначения ингибиторов протонной помпы (риск развития язвы желудка) |
1 (3,85%) |
0 (0,00%) |
|
Бета-адреноблокатор при брадикардии (<50 уд/мин), атриовентрикулярной блокаде II или III степени (риск полной блокады, асистолии) |
0 (0,00%) |
1 (3,85%) |
Примечания: * – p < 0,05, статистические значимые различия между исследуемыми группами.
Заключительным этапом контроля рациональности фармакотерапии у пациентов с синдромом старческой астении и без данного синдрома явился аудит лекарственных назначений на предмет антихолинергической нагрузки, которая была оценена с помощью валидированной шкалы Anticholinergic Cognitive Burden Scale и критериев Бирса. На основании первого инструмента было выявлено, что препараты с антихолинергическим потенциалом были назначены 16 из 26 пациентов со старческой астенией и 23 из 26 пациентов без изучаемого синдрома (p<0,05). В соответствии со шкалой антихолинергической нагрузки каждому пациенту был присвоен суммарный балл. Медиана балла по шкале Anticholinergic Cognitive Burden Scale у пациентов с синдромом старческой астении составила 1,0, интерквартильный размах – от 0,0 до 2,0, для пациентов без старческой астении – 3,0, интерквартильный размах – от 1,0 до 4,0. Разница между группами статистически значима (p<0,05).
Клиническую ценность, с точки зрения разработчиков шкалы антихолинергической нагрузки Anticholinergic Cognitive Burden Scale, может иметь значение суммарного балла, равное или превышающее 3. Среди больных с синдромом старческой астении таких пациентов было меньше (6), чем без синдрома (17) (p<0,05).
При использовании раздела «Лекарственные средства с высоким антихолинергическим потенциалом», входящего в состав инструмента по борьбе с полипрагмазией – критериев Бирса Американской гериатрической ассоциации, мы получили следующие результаты антихолинергической нагрузки у исследуемых больных. Пациентам со старческой астенией реже назначались подобные препараты – 23,08% против 65,38% (p<0,05), причем во второй группе были обнаружены 3 пациента, у которых в листе назначений присутствовали 2 и более лекарственных средств с обсуждаемыми свойствами.
С целью выявления роли отдельных лекарственных препаратов в формировании общей антихолинергической нагрузки нами была проанализирована структура таких назначений, представленная в таблице 4.
Таблица 4
Структура назначений лекарственных препаратов с антихолинергическими свойствами на основании шкалы Anticholinergic Cognitive Burden Scale и критериев Бирса
|
Лекарственный препарат, входящий в шкалу Anticholinergic Cognitive Burden Scale и критерии Бирса |
Пациенты с синдромом старческой астении: n (%) |
Пациенты без синдрома старческой астении: n (%) |
|
тиоридазин* |
4 (15,38%) |
7 (26,92%) |
|
метопролол |
6 (23,08%) |
4 (15,38%) |
|
рисперидон |
2 (7,69%) |
5 (19,23%) |
|
тригексифенидил* |
1 (3,85%) |
5 (19,23%) |
|
дигоксин |
3 (11,54%) |
0 (0,00%) |
|
амитриптилин* |
0 (0,00%) |
3 (11,54%) |
|
карбамазепин |
2 (7,69%) |
0 (0,00%) |
|
ранитидин |
2 (7,69%) |
0 (0,00%) |
|
трифлуоперазин* |
0 (0,00%) |
2 (7,69%) |
|
каптоприл |
0 (0,00%) |
2 (7,69%) |
|
хлорпромазин* |
0 (0,00%) |
2 (7,69%) |
|
флувоксамин |
1 (3,85%) |
0 (0,00%) |
|
оланзапин* |
1 (3,85%) |
0 (0,00%) |
|
амантадин |
1 (3,85%) |
0 (0,00%) |
|
галоперидол |
0 (0,00%) |
1 (3,85%) |
|
клозапин* |
0 (0,00%) |
1 (3,85%) |
|
нифедипин |
0 (0,00%) |
1 (3,85%) |
|
изосорбид |
0 (0,00%) |
1 (3,85%) |
|
кломипрамин* |
0 (0,00%) |
1 (3,85%) |
Примечания: * – лекарственный препарат присутствует в шкале Anticholinergic Cognitive Burden Scale и разделе «Лекарственные средства с высоким антихолинергическим потенциалом» критериев Бирса.
Полученные в ходе проведенного исследования результаты по контролю рациональности лекарственной терапии у пациентов психиатрического стационара с синдромом старческой астении и без указанного синдрома требуют некоторых пояснений. Использование шкалы The GerontoNet ADR Risk Score было направлено на выявление пациентов с высоким риском развития неблагоприятных лекарственных реакций. По мнению разработчиков данного инструмента, высоким считается риск, если его суммарный балл достигает 8. В нашем случае таких пациентов было по 2 из двух изучаемых групп. Медиана суммарного балла статистически не отличалась у пациентов с синдромом старческой астении и без него. Однако анализ переменных выявил двукратное превышение количества пациентов с изучаемым синдромом, у которых была определена почечная дисфункция. Данный факт связан с возрастным снижением скорости клубочковой фильтрации, но в то же время подчеркивает необходимость возможной корректировки дозового режима у пациентов со старческой астенией ввиду элиминирующей функции обсуждаемой системы органов.
Задача по оценке риска осложнений фармакотерапии также решалась с помощью инструмента ADRROP (Adverse Drug Reaction Risk in Older Persons). В данном случае было зафиксировано статистически значимое превышение суммарного балла у больных с синдромом старческой астении. На полученный результат могло оказать влияние превалирование следующих факторов: «Возраст старше 70 лет», «Необходимость в помощи ≥ 1 раз для осуществления повседневной активности», каждый из которых дает по 3 балла к сумме. Очевидно, что выявленные факторы имеют прямое отношение к изучаемому синдрому, и полученные результаты повышенного риска развития неблагоприятных лекарственных реакций у пациентов с синдромом старческой астении подчеркивают уязвимость данной группы.
Рекомендованное экспертами в области гериатрии использование ограничительного перечня «STOPP/START критерии» для аудита потенциально не рекомендованных лекарственных назначений не выявило статистически значимой разницы в частоте у исследуемых групп, однако были зафиксированы различия во встречаемости определенных STOPP-критериев. Пациентам без синдрома старческой астении чаще назначались нейролептики, в частности лекарственные препараты фенотиазинового ряда, в качестве терапии первой линии. Очевидно, что использование антипсихотической терапии является неотъемлемой частью лекарственного лечения в психиатрическом стационаре. Тем не менее разработчики критериев STOPP/START предостерегают о возможных нарушениях ходьбы, возникновении риска лекарственного паркинсонизма, выраженной седации и антихолинергических побочных эффектов. Выявленная тенденция, с нашей точки зрения, может свидетельствовать о большей безопасности фармакотерапии у пациентов со старческой астенией, реализуемой рациональными назначениями лечащих врачей, а также борьбой с резистентностью и антипсихотической политерапией у больных без синдрома.
По нашему мнению, с этими же причинами могут быть связаны более высокая частота назначения лекарственных препаратов с антихолинергическим потенциалом этой группе и более высокая медиана суммарного балла. Данный факт подтверждается анализом структуры таких назначений, в которой большая часть представлена антипсихотическими препаратами, антидепрессантами и центральным холиноблокатором тригексифенидилом, используемым для коррекции лекарственно-индуцированных экстрапирамидных нарушений.
Заключение
Нерациональная фармакотерапия у пациентов с синдромом старческой астении может приводить к неблагоприятным лекарственным реакциям и развитию потенциально опасных состояний. Проведенное исследование показало больший риск нежелательных побочных реакций у больных с изучаемым синдромом, который был связан скорее с возрастными изменениями организма, нежели с лекарственной терапией, оказываемой в условиях психиатрического стационара. Тем не менее использованные методы оценки назначенного лечения способны повысить безопасность фармакотерапии и качество жизни пациентов с психическими заболеваниями и синдромом старческой астении.
Библиографическая ссылка
Кирилочев О.О., Умерова А.Р. КОНТРОЛЬ РАЦИОНАЛЬНОСТИ ФАРМАКОТЕРАПИИ У ПАЦИЕНТОВ ПСИХИАТРИЧЕСКОГО СТАЦИОНАРА С СИНДРОМОМ СТАРЧЕСКОЙ АСТЕНИИ // Современные проблемы науки и образования. 2020. № 6. ;URL: https://science-education.ru/en/article/view?id=30449 (дата обращения: 18.05.2026).
DOI: https://doi.org/10.17513/spno.30449



