Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
FORECASTING OF FORMATION OF HEAVY DISTURBANCES OF MOTOR DEVELOPMENT IN CHILDREN OF EARLY AGE, TRANSFERRED PERINATAL HYPOXICALLY-ISCHEMIC DAMAGE OF THE CNS
Проблема церебрального гипоксически-ишемического поражения центральной нервной системы (ЦНС) у новорожденных и у детей в последующие возрастные периоды до настоящего времени остается одной из наиболее актуальных в неонатологии и педиатрии в связи с высокой частотой и большой значимостью перинатальной церебральной патологии для дальнейшей жизни [1, 2]. При этом неоднозначность исходов церебральной ишемии у детей раннего возраста определяется степенью функциональной зрелости головного мозга и пластичностью нервной системы [3–5].
Не до конца решенными остаются вопросы определения влияния роли отдельных неблагоприятных факторов в механизмах возникновения перинатальных гипоксически-ишемических поражений ЦНС [6–8], а также поиск достоверных критериев прогноза формирования отдаленных неврологических нарушений и оптимальных терапевтических подходов к тактике ведения данного контингента детей [9–11].
В этих условиях тяжелые формы нарушений моторного развития, возникающие вследствие церебральных мозговых катастроф, рассматриваются не только как резидуальные органические изменения, но и как проградиентный патологический процесс на фоне нейроиммунного конфликта в системе «мать – плод» и неспецифического воспаления иммунной природы [12, 13].
Цель исследования: выявление прогностических критериев формирования тяжелых нарушений произвольных двигательных функций у детей раннего возраста с последствиями перинатального гипоксически-ишемического поражения ЦНС.
Материалы и методы исследования
Мы ретроспективно проанализировали 179 историй болезни детей с различными исходами гипоксически-ишемических поражений ЦНС, находившихся на лечении в отделении детей младшего возраста НИИ акушерства и педиатрии ФГБОУ ВО РостГМУ в 2012–2016 гг. Оценивались состояние здоровья, течение беременности и родов матерей с определением роли отдельных факторов риска, а также клинические проявления церебральных нарушений, параметры мозговой гемодинамики и биоэлектрической активности головного мозга у детей первых 3 месяцев жизни.
Критериями включения в исследование являлись доношенные дети с массой тела от 2850,0 до 4100,0 г.
Критерии исключения: гестационный возраст менее 37 недель, многоплодная беременность, наличие диагностированной хромосомной или моногенной патологии, изолированных пороков и аномалий развития ЦНС, врожденных эндокринных заболеваний, внутриутробных инфекций, гнойно-септических заболеваний.
С учетом выраженности и характера неврологической симптоматики были сформированы 3 группы: 1-я группа – 81 (45,3%) ребенок с клиническими проявлениями синдрома минимальной мозговой дисфункции (ММД); 2-ю группу составили 45 детей (25,1%) со структурной эпилепсией; 3-ю группу – 53 ребенка (29,6%) с различными тяжелыми формами нарушения моторного развития.
Всем наблюдаемым детям проводилось электроэнцефалографическое исследование (ЭЭГ) с помощью программно-аппаратного комплекса ЭЭГА-21/26 «Энцефалан 131-03». ЭЭГ регистрировалась по схеме «10–20» в лобных, височных, центральных отведениях в состоянии естественного сна в течение 15–30 минут с визуальной оценкой записи и применением спектрального анализа. Проводились оценка выраженности диффузных и локальных изменений биоэлектрической активности мозга, степени формирования и характеристика основных ритмов ЭЭГ.
Мозговой кровоток оценивался методом транскраниальной допплерографии по стандартной методике при помощи ультразвукового допплерографического прибора «Multi-Dop» T2 DWL – 2.55 MDT фирмы «ElektronischeSystemeGmbH» с набором датчиков частотой 2, 4 и 8 МГц. При этом исследовались средняя скорость кровотока в систолу, индекс резистентности (IR) в русле среднемозговой артерии (СМА), скорость кровотока по прямому синусу (ПС) в см/сек.
Результаты исследования были статистически обработаны с помощью программного пакета STATISTICA 6.0. Достоверность различий между группами оценивалась с помощью параметрических и непараметрических критериев (различия в группах считались достоверными, если уровень значимости не превышал 0,05). На основе логистического регрессионного анализа данных была построена прогностическая модель, позволяющая прогнозировать возникновение тяжелых форм нарушений моторного развития.
Результаты исследования и их обсуждение
Анализ данных медицинской документации был направлен на выявление ведущих перинатальных факторов риска формирования последствий церебральной гипоксии-ишемии различной степени тяжести (табл. 1).
Таблица 1
Состояние здоровья, особенности течения беременности и родов у матерей детей обследованных групп
|
Группы
Факторы риска |
ММД (n=81) |
Структурная эпилепсия (n=45) |
Тяжелые формы нарушения моторного развития (n=53) |
|||
|
Абс / % |
Уровень статистической значимости |
Абс / % |
Уровень статистической значимости |
Абс / % |
Уровень статистической значимости |
|
|
1. Экстрагенитальная патология |
||||||
|
Патология щитовидной железы |
2/2,5* |
p=0,046 |
5/11,1*** |
p=0,3335 |
3/5,7** |
p=0,3431 |
|
Избыток массы тела 1–2-й степени |
12/14,8* |
p=0,904 |
7/15,6*** |
p=0,3532 |
5/9,4** |
p=0,3597 |
|
Нарушение функции сердечно-сосудистой системы |
1/1,2* |
p=0,094 |
3/6,7*** |
p=0,8784 |
4/7,5** |
p=0,0608 |
|
Хронические инфекции почек |
3/3,7* |
p=0,105 |
5/11,1*** |
p=0,1700 |
2/3,8** |
p=0,9762 |
|
Респираторно-вирусные инфекции во время беременности |
10/12,3* |
p=0,604 |
7/15,6*** |
p=0,8946 |
9/17** |
p=0,4468 |
|
2. Осложнения беременности |
||||||
|
Анемия |
6/7,4* |
p=0,038 |
9/20,0*** |
p=0,1255 |
18/34,0** |
p=0,0001 |
|
Преэклампсия легкой степени |
17/21* |
p=0,214 |
14/31,1*** |
p=0,6030 |
19/35,9** |
p=0,0578 |
|
Преэклампсия средне-тяжелой степени |
5/6,1* |
p=0,0003 |
15/33,3*** |
p=0,9170 |
18/34** |
p=0,0001 |
|
Фетоплацентарная недостаточность (ФПН) |
10/12,3* |
p=0,000 |
21/46,7*** |
p=0,6924 |
23/43,4** |
p=0,0001 |
|
Много- или маловодие |
5/6,2* |
p=0,0016 |
12/26,7*** |
p=0,2335 |
9/17** |
p=0,0479 |
|
Угроза прерывания |
17/21* |
p=0,0136 |
19/42,2*** |
p=0,7660 |
24/45,3** |
p=0,6834 |
|
Преждевременное созревание плаценты |
3/3,7* |
p=0,0007 |
11/24,4*** |
p=0,5078 |
16/30,2** |
p=0,0000 |
|
3. Осложнения родов |
||||||
|
Стремительные роды |
3/3,7* |
p=0,047 |
6/13,3*** |
p=0,2997 |
11/20,8** |
p=0,0018 |
|
Затяжные роды |
7/8,6* |
p=0,036 |
10/22,2*** |
p=0,5334 |
9/17** |
p=0,1447 |
|
Кесарево сечение |
18/22,2* |
p=0,1795 |
15/33,3*** |
p=0,0195 |
30/56,6** |
p=0,0001 |
|
Тугое обвитие пуповины |
0 |
0 |
5/11,1*** |
p=0,5498 |
4/7,5** |
p=0,0613 |
|
Внутримозговые кровоизлияния |
4/4,9* |
p=0,0085 |
9/20*** |
p=0,3663 |
7/13,2** |
p=0,0953 |
Примечание: проценты даны по отношению к числу детей в группе
* Отличие между группами детей с ММД и структурной эпилепсией
** Отличие между группами детей с ММД и тяжелыми формами нарушения моторного развития
*** Отличие между группами детей со структурной эпилепсией и тяжелыми формами нарушения моторного развития
Установлено, что наиболее высокая отягощенность по экстрагенитальной патологии отмечалась у матерей в группе детей со структурной эпилепсией. Вместе с тем при анализе факторов осложнений беременности и родов почти с одинаковой частотой встречались: анемия, преэклампсия легкой степени, фетоплацентарная недостаточность и угроза прерывания беременности у матерей в группах детей со структурной эпилепсией и тяжелыми формами нарушений моторного развития, что в свою очередь обусловило высокую частоту встречаемости осложнений родового акта в обследуемых группах. При анализе факторов интранатального периода обращают на себя внимание достоверные отличия – более низкий процент выявления осложнений родового акта у детей с ММД по сравнению с группой детей со структурной эпилепсией и тяжелыми формами нарушений моторного развития.
Представляет определенный интерес наличие четкой взаимосвязи между оценкой по шкале Апгар как при рождении, так и на 5-й минуте жизни с тяжестью церебральной патологии у детей обследованных групп (табл. 2). При этом установлено, что в группе детей со структурной эпилепсией и тяжелыми формами нарушения моторного развития отмечались наиболее низкие их значения в указанный временной промежуток.
Таблица 2
Оценка по шкале Апгар у новорожденных обследованных групп
|
Группы детей
Оценка по шкале Апгар |
ММД (n=81) |
Структурная эпилепсия (n=45) |
Тяжелые формы нарушения моторного развития (n=53) |
|||
|
на 1-й минуте |
на 5-й минуте абс (%) |
на 1-й минуте абс (%) |
на 5-й минуте абс (%) |
на 1-й минуте абс (%) |
на 5-й минуте абс (%) |
|
|
7–9 баллов |
72 (88,9)* p=0,0000 |
75 (93)* p=0,0000 |
8 (9,87)*** p=0,0208 |
21 (17,8)***p=0,0497 |
15 (28,3)** p=0,0000 |
19 (35,8)** p=0,0000 |
|
4–6 баллов |
9 (11,1)* p=0,0000 |
6 (7,4)* p=0,0000 |
35 (77,8)*** p=0,0594 |
24 (53,3)***p=0,3307 |
32 (60,3)** p=0,0000 |
23 (43,4)** p=0,0000 |
|
<4 баллов |
0 |
0 |
2 (4,4)*** p=0,2160 |
0 |
6 (11,3)** p=0,0654 |
11 (20,8)** p=0,0598 |
Примечание: проценты даны по отношению к числу детей в группе
* Отличие между группами детей с ММД и структурной эпилепсией
** Отличие между группами детей с ММД и тяжелыми формами нарушения моторного развития
*** Отличие между группами детей со структурной эпилепсией и тяжелыми формами нарушения моторного развития
Анализ данных ЭЭГ выявил закономерное увеличение частоты встречаемости признаков эпилептиформной активности в группе детей со структурной эпилепсией. Вместе с тем обращала на себя внимание высокая частота регистрации эпилептиформных графоэлементов у детей с тяжелыми формами нарушения моторного развития, что позволило отнести указанный контингент в группу риска возникновения эпилептических приступов в более поздние возрастные периоды детства (табл. 3).
Таблица 3
Сравнительные особенности параметров ЭЭГ в изучаемых группах
|
Группа
Параметры
|
ММД (n=81) |
Структурная эпилепсия (n=45) |
Тяжелые формы нарушения моторного развития (n=53) |
|||
|
Абс /% |
Уровень статистической значимости |
Абс /% |
Уровень статистической значимости |
Абс /% |
Уровень статистической значимости |
|
|
Вариант возрастной нормы |
31/38,3* |
p=0,0041 |
6/13,3*** |
p=0,8472 |
22,6/12** |
p=0,0012 |
|
Задержка формирования основного ритма ЭЭГ |
50/61,7* |
p=0,0393 |
36/80*** |
p=0,0001 |
73,4/39** |
p=0,0102 |
|
Фокальная медленно-волновая активность |
4/4,9* |
p=0,0000 |
18/40*** |
p=0,0324 |
37,7/20** |
p=0,0069 |
|
Генерализованная и фокальная эпилептическая активность |
0 |
0 |
21/46,7*** |
p=0,0000 |
8/15,1** |
p=0,0546 |
|
Изменения биоэлектрической активности головного мозга диффузного характера |
||||||
|
Легкие диффузные изменения |
62/76,5 |
p=0,0000 |
4/8,9*** |
p=0,3601 |
15/28,3** |
p=0,0000 |
|
Умеренные диффузные изменения |
3/3,7* |
p=0,0000 |
29/64,4*** |
p=0,0013 |
31/58,5** |
p=0,0000 |
|
Значительные диффузные изменения |
9/35,8 |
p=0,0000 |
14/31,1*** |
p=0,0067 |
7/13,2** |
p=0,0000 |
Примечание: проценты даны по отношению к числу детей в группе
* Отличие между группами детей с ММД и структурной эпилепсией
** Отличие между группами детей с ММД и тяжелыми формами нарушения моторного развития
*** Отличие между группами детей со структурной эпилепсией и тяжелыми формами нарушения моторного развития
Согласно результатам транскраниальной допплерографии (табл. 4) нарушение мозгового кровотока в той или иной степени было выявлено во всех группах обследованных детей. Однако наиболее выраженные изменения отмечены у детей с тяжелыми формами нарушения моторного развития и структурной эпилепсией, при этом наиболее часто определялся гипокинетически-гипертонический тип кровотока, характеризовавшийся снижением средней систолической скорости в совокупности с повышением параметров периферического сосудистого сопротивления (IR) в русле СМА, сочетавшийся с явлениями церебральной венозной дисгемии по интракраниально-ликвородинамическому типу с акцентом на уровень мезодиэнцефальных структур головного мозга. Вместе с тем при анализе изучаемых параметров имеют место достоверные отличия между показателями линейной скорости кровотока во всех изучаемых группах, в то время как IR и скорость кровотока по ПС имели достоверные отличия только в группах детей с ММД и тяжелыми формами нарушений моторного развития, что свидетельствует о значимости гемодинамических нарушений в патогенезе формирования тяжелых форм двигательных расстройств.
Таблица 4
Параметры мозгового кровотока у детей обследованных групп (М +m)
|
Группа Параметры |
ММД (n=81) |
Структурная эпилепсия (n=45) |
Тяжелые формы нарушения моторного развития (n=53) |
|||
|
Средняя скорость кровотока в систоле по СМА, см/с |
77, 6 ± 5,8 |
*р=0,0000 |
67 ± 8,7 |
**р=0,0000 |
59, 2 ± 5,7 |
***р=0,0000 |
|
IR-индекса резистентности в русле СМА |
0,71 ± 0,06 |
**р=0, 0000 |
0,76 ± 0,08 |
***р=0,0185 |
0,73 ± 0,04 |
*р=0,0846 **р=0,0000 |
|
Скорость кровотока по ПС, см/с |
25,6 ± 5,5 |
*р=0,0000 |
39,7 ± 7,9 |
**р=0,1237 |
38,3 ± 3,2 |
***р=0,1237 |
Примечание: * отличие между группами детей с ММД и структурной эпилепсией
** отличие между группами детей с ММД и тяжелыми формами нарушения моторного развития
*** отличие между группами детей со структурной эпилепсией и тяжелыми формами нарушения моторного развития
В настоящее время при постановке диагноза врач-невролог опирается на данные анамнеза жизни, заболевания, общего и неврологического статуса, а также результаты современных методов нейровизуализации, нейрофизиологических и лабораторных исследований, характеризующих структурно-функциональное состояние нейронов и нейроглии. Комплексное использование этих методов определяет высокую точность диагностики, однако их широкое использование затруднено из-за необходимости наличия специальной дорогостоящей аппаратуры, а существенным недостатком является отсутствие возможности спрогнозировать возникновение неврологических нарушений на раннем этапе их возникновения, что позволяет получить лишь отдельные представления об определенных патофизиологических изменениях в ЦНС в ответ на гипоксию без учета фазности, устойчивости и особенностей течения ее последствий в постнатальном онтогенезе [14].
С целью совершенствования оказания медицинской помощи детям раннего возраста с последствиями церебрального гипоксически-ишемического поражения ЦНС различной степени тяжести нами предложена модель прогнозирования возникновения тяжелых форм нарушения моторного развития у детей первых 3 месяцев жизни. Данная модель основана на логистическом регрессионном анализе с использованием ROC-анализа [15]. Результатом исследования является расчет регрессионных коэффициентов в уравнении логит-преобразования:
y = F+5,90*А-9,99*Э+0,82*С1-1,11*С2,
где F = – 60,61 – константа;
А – оценка по шкале Апгар на 5-й минуте в баллах;
Э – степень выраженности изменений биоэлектрической активности (по данным рутинной ЭЭГ, выполняемой по стандартной методике по схеме «10–20») в баллах: 0 баллов – умеренно выраженные общемозговые изменения, 1 балл – выраженные общемозговые изменения;
С1 – средняя скорость кровотока в систоле по СМА, измеряемая в см/с;
С2 – скорость кровотока по ПС, измеряемая в см/с (указанные показатели регистрируются методом транскраниальной допплерографии по стандартной методике).
Значение объяснимого признака z определяется по формуле 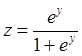 , где е – основание натурального логарифма, что при
, где е – основание натурального логарифма, что при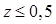 прогнозирует развитие тяжелых нарушений произвольных двигательных функций, в том числе ДЦП, у доношенного ребенка.
прогнозирует развитие тяжелых нарушений произвольных двигательных функций, в том числе ДЦП, у доношенного ребенка.
Преимуществом данного метода являются: возможность раннего прогнозирования нарушения моторного развития у детей первых 3 месяцев жизни, перенесших гипоксически-ишемическое поражение ЦНС, с использованием специфических нейрофизиологических показателей, малоинвазивных и доступных в клинической практике методов исследования, не требующих специальной подготовки ребенка, с длительностью проведения диагностического процесса около 20 минут; высокой точностью – 99 %, чувствительностью – 98% и специфичностью – 100%.
Заключение
Проведенные исследования свидетельствуют о том, что для предупреждения тяжелых исходов неврологических нарушений необходимо проводить тщательный анализ анамнестических данных, включающий учет особенностей течения беременности, родов и раннего неонатального периода, дополнительных методов исследований (ЭЭГ и УЗДГ церебральной гемодинамики), это позволит выработать персонифицированный подход к лечебно-реабилитационным мероприятиям и будет способствовать предотвращению дальнейшего прогрессирования патологического церебрального процесса с частичной редукцией или восстановлением.
Библиографическая ссылка
Созаева Д.И., Афонин А.А., Бережанская С.Б., Лебеденко А.А., Вострых Н.Н., Логинова И.Г., Бабиянц А.Я., Манукян М.Р., Афонина Т.А., Папшева Е.А. ПРОГНОЗИРОВАНИЕ ФОРМИРОВАНИЯ ТЯЖЕЛЫХ НАРУШЕНИЙ МОТОРНОГО РАЗВИТИЯ У ДЕТЕЙ РАННЕГО ВОЗРАСТА, ПЕРЕНЕСШИХ ПЕРИНАТАЛЬНЫЕ ГИПОКСИЧЕСКИ-ИШЕМИЧЕСКИЕ ПОРАЖЕНИЯ ЦНС // Современные проблемы науки и образования. 2019. № 5. ;URL: https://science-education.ru/en/article/view?id=29152 (дата обращения: 17.05.2026).



