Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
SAFETY OF USING ROPIVACAINE FOR LOCAL INFILTRATION ANESTHESIA DURING HIP REPLACEMENT
Коксартроз – тяжелое дегенеративно-дистрофическое заболевание тазобедренных суставов, развитие которого сопровождается стойким выраженным болевым синдромом, а также функциональными нарушениями. Наиболее популярным оперативным вмешательством, позволяющим облегчить жизнь таким пациентам, стало эндопротезирование тазобедренного сустава. Однако и оно не лишено недостатков, одним из которых является выраженный послеоперационный болевой синдром, препятствующий ранней функциональной реабилитации и быстрому восстановлению пациента. Проблема послеоперационной боли до сих пор остается значимой в хирургической ортопедии [1, 2]. Для ее решения предложено множество различных путей — пациент-контролируемая аналгезия, блокады периферических нервов, эпидуральная аналгезия, пролонгированное введение анестетика через установленный катетер. Также среди множества предложенных современной наукой путей решения этой проблемы выделяется локальная интраоперационная инфильтрационная анестезия (ЛИА), позволяющая адекватно уменьшить интенсивность раннего послеоперационного болевого синдрома, снизить дозу и кратность принимаемых после операции опиоидов, а также предоставить пациенту возможность заниматься лечебной физкультурой уже в первые сутки после вмешательства [3, 4]. ЛИА представляет собой интравульнарное введение раствора анестетика, часто в комбинации с адъювантами (адреналином, дексаметазоном, кеторолаком, опиоидами) в зону операционного разреза в ходе эндопротезирования крупного сустава [5, 6]. Одно из важнейших свойств локально действующих анестетиков – это обратимое угнетение нервного импульса, которое вызывает длительную сенсорную и моторную блокаду, подходящую для анестезии в различных видах хирургии [7 8], при этом снижение острого болевого синдрома достигается применением небольших доз анестетика [9].
Применение ропивакаина, имеющего структурное сходство с бупивакаином, но в отличие от последнего не являющегося рацематом, позволяет уменьшить потенциальную кардиотоксичность и улучшить отношение сенсорного и моторного блока с преобладанием первого [10].
Однако использование ропивакаина в больших дозах и объемах в сочетании с нервным блоком и методами нейраксиальной блокады может повышать токсичность и, как следствие, увеличивать риск развития судорог, глубокой гипотензии, респираторной и сердечной недостаточности. В связи с потенциальным риском летального исхода назначение препарата должно сопровождаться глубокими знаниями фармакодинамики, фармакокинетики, а также мерами предосторожности, предупреждая неблагоприятные побочные эффекты при превышении пороговой концентрации ропивакаина в сыворотке крови до 3,4–5,3 мкг/мл [11, 12].
Клинический опыт применения ЛИА за последние 20 лет доказывает ее безопасность и надежность. Тем не менее существует ряд вопросов, которые вызывают опасения при клиническом использовании данной методики. К примеру, применение высоких доз местных анестетиков, случайное внутрисосудистое введение могут повлечь за собой серьезные побочные эффекты, такие как гипо- или гипертензия, бради- или тахикардия, головная боль, головокружение, парестезия, нейропатия, нарушение функции спинного мозга (синдром передней спинной артерии, арахноидит), тошнота, рвота, озноб, повышение температуры тела, задержка мочи, аллергические реакции (в том числе анафилактический шок), вплоть до нарушения сердечной деятельности и остановки сердца. Стремление разработать безопасные безопиоидные режимы обезболивания привело к фокусировке внимания на местной инфильтрационной анестезии, частью которой является и локальная инфильтрационная анестезия. Также практически неосвещенной в отечественной и зарубежной научной литературе остается проблема безопасности сочетанного применения эпидуральной аналгезии и локальной инфильтрационной анестезии (как в целом в хирургии, так и при эндопротезировании крупных суставов в частности) ввиду ограниченного числа публикаций, освещающих уровни концентраций используемых местных анестетиков в крови.
Цель исследования: изучить безопасность сочетанного применения ропивакаина для эпидуральной и локальной инфильтрационной анестезии при эндопротезировании тазобедренного сустава.
Материал и методы исследования. В проспективное клиническое исследование был включен 21 пациент, перенесший первичное эндопротезирование тазобедренного сустава за период с 2017 по 2018 гг. в клинике РНИИТО им. Р.Р. Вредена по поводу коксартроза III–IV стадии по классификации Kellgren–Lawrence. Средний возраст больных составил 60,64±8,1 года (от 34 до 81 года). Женщин в исследовании было в 2 раза больше, чем мужчин, – 14 (66,0%) и 7 (34,0%) соответственно. Медианное значение возраста женщин составило 62 года (МКИ 52–68), у мужчин — 54 года, медианное значение МКИ 46–60. Анализ интересующих показателей концентрации ропивакаина в сыворотке крови проводился в группах по гендерному признаку.
Критерием включения был идиопатический коксартроз, критерием невключения – наличие неврологических нарушений и/или сердечно-сосудистых заболеваний в стадии декомпенсации. Всем пациентам выполняли эпидуральную анестезию 0,5%-ным раствором ропивакаина. На завершающем этапе операции применяли лекарственный коктейль, включающий 50 мл 0,5%-ного раствора ропивакаина и 2 мл 0,25%-ного раствора дексаметазона, который последовательно вводили в переднюю, нижнюю и верхнюю порции капсулы, надкостницу, сухожилие большой ягодичной мышцы, верхний глубокий слой отводящих мышц, передние участки надкостницы бедренной кости, латеральную прямую мышцу бедра, малую и среднюю ягодичные мышцы, напрягатель широкой фасции бедра, большую ягодичную мышцу, подкожную жировую клетчатку, кожу, с проведением аспирационной пробы перед каждым вколом иглы для профилактики внутрисосудистого введения раствора препаратов [13].
В последующем, через 1 час после обкалывания операционной раны, проводили взятие венозной крови для определения концентрации ропивакаина в сыворотке.
Определение ропивакаина. Концентрацию анестетика в сыворотке крови определяли методом высокоэффективной жидкостной хроматографии (ВЭЖХ) на приборе фирмы «Shimadzu» (Prominence-i). Подготовку проводили путем двукратной экстракции ропивакаина из 0,5 мл сыворотки крови в 2,5 мл хлороформа с последующим высушиванием в токе воздуха. Высушенный экстракт растворяли в 300 мкл воды и 20 мкл вводили в хроматограф. Детектирование осуществляли с помощью диодной матрицы на длине волны 230 нм. Разделение осуществляли в режиме градиентного элюирования со скоростью 450 мкл/мин. Элюент – градиент ацетонитрила в 0.01 N формиате Na, рН 3,56. Колонка Shim-pack HR-ODS 150 х 3 мм. Оценивали соответствие полученных результатов данным научной литературы, а также различия в концентрации ропивакаина у мужчин и женщин.
В раннем послеоперационном периоде проводили регистрацию нежелательных лекарственных эффектов (гипо- или гипертензия, бради- или тахикардия, головная боль, головокружение, парестезия, нейропатия, нарушение функции спинного мозга (синдром передней спинной артерии, арахноидит), тошнота, рвота, озноб, повышение температуры тела, задержка мочи, аллергические реакции (в том числе анафилактический шок).
Статистические методы обработки. Полученные статистические данные анализировались с помощью IBM SPSS Statistics for Windows (версия 24). Для средних величин определяли медиану и 25–75%-ный межквартильный интервал (МКИ). Критерием статистической значимости различий являлась величина р<0,05, определенная с помощью критерия Манна–Уитни.
Результаты исследования и их обсуждение. В исследуемой выборке пациентов на фоне эпидуральной анестезии одинаковыми для всех включенных в исследование пациентов дозами ропивакаина медиана концентрации препарата в сыворотке крови через час после его дополнительного введения в область операционной раны составила 0,82 мкг/мл (МКИ 0,57–1,45).
У женщин медианная концентрация ропивакаина в сыворотке составила 0,82 мкг/мл, что статистически не отличалось от подобного показателя в группе мужчин – 0,861 мкг/мл (р>0,05) (рис. 1).
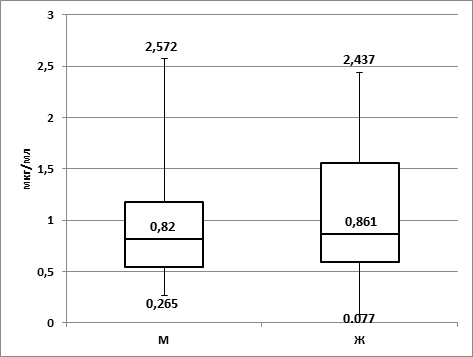
Рис.1. Разброс концентрации ропивакаина в сыворотке крови через 1 час после интравульнарного введения в 2 группах: М – мужчины (7) и Ж – женщины (14)
У 6 из 7 пациентов мужского пола концентрация препарата находилась в интервале от 0,5 до 1,5 мкг/мл (рис. 2). Наивысшая концентрация ропивакаина была у пациента 49 лет, что может быть проявлением особенности ферментных систем. У женщин (рис. 3) в 2 случаях концентрация ропивакаина была менее 0,5 мкг/мл и в 2 случаях – более 2,0 мкг/мл, что свидетельствует о несколько большей вариабельности уровня анестетика в крови.
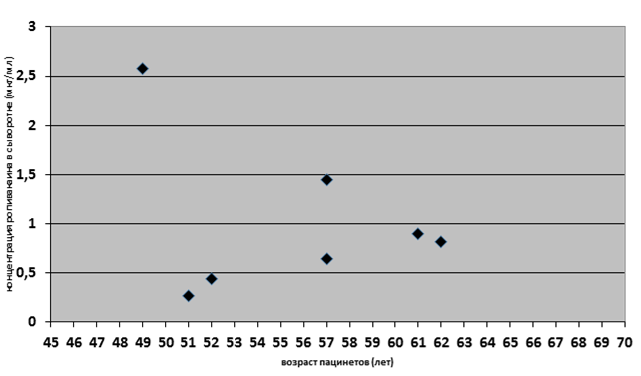
Рис. 2. Зависимость концентрации ропивакаина от возраста у мужчин
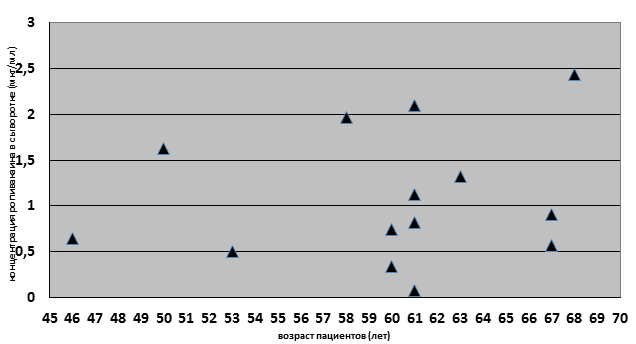 Рис.3. Зависимость концентрации ропивакаина от возраста у женщин
Рис.3. Зависимость концентрации ропивакаина от возраста у женщин
Незначительные отличия в разбросе изменений концентрации ропивакаина в сыворотке крови после одномоментного введения в зону операционного разреза, по-видимому, объяснялись различной степенью васкуляризации раны и степенью активности метаболических процессов каждого конкретного пациента. На рисунке 1 обращает на себя внимание сходство числовых значений концентраций ропивакаина в сыворотке между мужчинами и женщинами, что нивелирует индивидуальные гендерные особенности пациента, подвергающегося ЛИА. За пятидневный период наблюдения побочных эффектов использования ЛИА отмечено не было.
В аналогичном нашему исследовании A. Busch с соавторами [14] изучали анальгетическую эффективность лекарственного коктейля ропивакаина, кеторолака, эпиморфина и эпинефрина при интраоперационном локальном введении у 64 пациентов, перенесших тотальное эндопротезирование коленного сустава. В ходе своего исследования в 5 случаях авторы измерили уровень ропивакаина в сыворотке крови через 4 часа после снятия турникета. Установленная наибольшая концентрация анестетика составила 1,2 мкг/мл, что в 2,5–3 раза ниже его токсического уровня (3,4–5,3 мкг/мл). Системных токсических эффектов на центральную нервную систему и сердечно-сосудистую систему ни у кого из пациентов, включенных в исследование, авторы не выявили.
Essving и соавторы [15] в 2010 г. опубликовали статью, где проанализировали влияние на послеоперационный уровень боли сочетания 400 мг ропивакаина, 30 мг кеторолака и 0,5 мг эпинефрина, вводимых совместно периартикулярно во время операции эндопротезирования коленного сустава. При этом у 8 пациентов после 30, 60, 120, 180 минут введения лекарственной смеси забирали венозную кровь для хроматографического определения уровня ропивакаина в сыворотке крови. В результатах обращают на себя внимание вариация концентраций ропивакаина от 0,032 мкг/мл до 0,12 мкг/мл, а также отсутствие системной токсичности от вводимых препаратов.
В вышеперечисленных публикациях отсутствует информация о применяемом анестезиологическом пособии во время операции, исследуется малое количество пациентов в подгруппах с определением концентраций ропивакаина через 4 часа после снятия турникета, а не через 1 час после введения лекарственного коктейля, что может служить основанием значительной разницы в полученных результатах. Так, в нашем исследовании демонстрируются более высокие уровни ропивакаина в сыворотке крови при ЭП ТБС, нежели результаты вышеупомянутых авторов, что, возможно, связано с применением ропивакаина в более высоких дозировках для эпидуральной и локальной анестезии в сравнении с эндопротезированием коленного сустава. Однако ни в одном случае концентрация ропивакаина не достигла даже минимального порога токсичности в 3,4 мкг/мл. Применение турникета теоретически кратковременно в момент после его снятия может повлиять на уровень анестетика в сыворотке крови, так как далее при возобновлении кровотока раствор анестетика, введенный в мягкие ткани в ходе операции, устремляется в сосудистое русло, так же как это происходило бы при обкалывании без использования жгута. Однако публикаций, подтверждающих или опровергающих это мнение, пока нет.
При адаптации метода ЛИА нами была показана эффективность лекарственного коктейля, включающего 50 мл 0,5%-ного раствора ропивакаина и 2 мл 0,25%-ного раствора дексаметазона, в сравнении с уже существующими вариантами комбинаций различных лекарственных препаратов в составе вводимых коктейлей, а также дозировками и путями их введения (болюсно, установка катетера), что также подтверждается данными научных публикаций.
Заключение. Полученные нами результаты свидетельствуют, что сочетанное применение 0,5%-ного раствора ропивакаина для эпидуральной анестезии в качестве анестезиологического пособия и лекарственного коктейля, включающего 50 мл 0,5%-ного раствора ропивакаина и 2 мл 0,25%-ного раствора дексаметазона, согласно методике локальной инфильтрационной анестезии последовательно вводимого в окружающие установленные компоненты эндопротеза мягкие ткани в ходе операции первичного эндопротезирования тазобедренного сустава, не приводит к превышению пороговых концентраций анестетика в крови и развитию нежелательных лекарственных эффектов. Таким образом, при правильном применении данный метод обезболивания может быть рекомендован для широкого применения при первичном эндопротезировании тазобедренного сустава.
Библиографическая ссылка
Несинов А.А., Божкова С.А., Шубняков И.И., Королева Е.М., Гончаров М.Ю. БЕЗОПАСНОСТЬ ИСПОЛЬЗОВАНИЯ РОПИВАКАИНА ДЛЯ ЛОКАЛЬНОЙ ИНФИЛЬТРАЦИОННОЙ АНЕСТЕЗИИ ПРИ ЭНДОПРОТЕЗИРОВАНИИ ТАЗОБЕДРЕННОГО СУСТАВА // Современные проблемы науки и образования. 2019. № 3. ;URL: https://science-education.ru/en/article/view?id=28888 (дата обращения: 07.05.2026).



