Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
PREDICTION OF DEVELOPMENT OF ISCHEMIC CARDIOMYOPATHY
Кардиоваскулярная патология остается проблемой номер один в большинстве стран мира, несмотря на существенный прогресс последних десятилетий в сфере ее диагностики и лечения. В трудоспособном возрасте, на который ложится основное бремя выработки внутреннего валового продукта страны и от величины которого зависит благосостояние нации, болезни системы кровообращения составляют более 1/3 всех случаев смерти [1, 2].
Следовательно, одной из важнейших проблем современной медицины является диагностика кардиоваскулярных заболеваний на ранних стадиях. В связи с этим в настоящее время стали все чаще заниматься вопросами прогнозирования развития и течения заболеваний, а также их исходов, так как по данным прогноза можно более рационально осуществлять лечебно-профилактические мероприятия и предотвратить серьезные осложнения [3, 4].
Цель исследования – разработать алгоритм прогнозирования индивидуального риска развития ишемической кардиомиопатии у пациентов с перенесенным Q-образующим инфарктом миокарда.
Материалы и методы исследования. В контролируемое исследование были включены 58 больных мужского пола (средний возраст 54,14 [49; 60] года с перенесенным Q-образующим инфарктом миокарда (ИМ) (давность 6–12 месяцев)). Критерии включения: 1) наличие сохраненной сократительной функции миокарда левого желудочка (ЛЖ) (ФВ ЛЖ (Simpson) ≥ 50 %); 2) отсутствие признаков дилатации ЛЖ по данным эхокардиографии. Критерии исключения из исследования: возраст старше 65 лет, нестабильная стенокардия, ИМ и острые цереброваскулярные события давностью менее 6 месяцев до начала исследования, врожденные пороки сердца, острые и/или хронические заболевания в стадии обострения, аутоиммунные заболевания, злокачественные новообразования, давность хирургического вмешательства менее 6 месяцев. Контрольная группа состояла из 30 соматически здоровых лиц мужского пола (средний возраст 49,6 [41; 57] года). Клиническая характеристика пациентов представлена в таблице 1.
Таблица 1
Клиническая характеристика пациентов
|
Показатель |
Пациенты n=58 |
|
Возраст, годы
|
54,14 [49; 60] |
|
Индекс массы тела, кг/м2 |
34,0 [29,4; 53,2]
|
|
Длительность симптомов ишемической болезни сердца, годы |
5,1 [2; 14] |
|
Без стенокардии, n (%) |
7 (12 %) |
|
2, n (%) |
25 (43 %) |
|
3, n (%) |
26 (45 %) |
|
Длительность симптомов хронической сердечной недостаточности, годы |
1,3 [0,5; 4] |
|
Стадия хронической сердечной недостаточности (по NYHA) |
|
|
I-IIA, n (%)* |
40 (69 %) |
|
II Б-III, n (%) |
18 (31 %) |
|
ФК ХСН (по NYHA) |
|
|
2, n (%) |
30 (52 %) |
|
3, n (%) |
26 (44 %) |
|
4, n (%) |
2 (4 %) |
|
6-минутный тест ходьбы, м |
273 [61; 434] |
|
Шкала оценки клинического состояния, баллы |
4,84 [1; 13] |
|
Длительность артериальной гипертензии в анамнезе, годы |
14,2 [2; 30] |
|
Стадия артериальной гипертензии |
III |
|
Систолическое артериальное давление, мм рт. ст. |
146,2 [125; 170] |
|
Диастолическое артериальное давление, мм рт. ст. |
88,7 [80; 100] |
|
Отягощенный наследственный анамнез по сердечно-сосудистым заболеваниям, n (%) |
42 (72 %) |
Примечание: n – число пациентов
При включении в исследование, а затем повторно через три года всем пациентам были произведены полное клинико-диагностическое обследование согласно клиническим рекомендациям «Диагностика и лечение хронической ишемической болезни сердца» Министерства здравоохранения Российской Федерации (2013) [5] и дополнительные лабораторно-инструментальные исследования (определение уровня проадреномедуллина (MR-proADM) с использованием тест-системы «BRANMSMR-proADMKRYPTOR» (Германия); уровня предшественника натрийуретического пептида типа В (NT-proBNP) – тест-система «BiomedicaNT-proBNP» (Австрия); уровней матриксной металлопротеиназы-1 (ММП-1) и ее тканевого ингибитора (ТИМП-1), трансформирующего фактора роста-β1 (ТФР-β1) с помощью коммерческих тест-систем «BenderMedSystems» (Австрия) и расчет индекса левожелудочково-артериального взаимодействия (иЛЖАВ) [6]).
Исследование выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинской Декларации и одобрено Региональным независимым этическим комитетом (протокол № 11 от 06.11.2014 г.). Все пациенты дали информированное согласие на добровольное участие в исследовании, получив полную информацию о нем.
Статистическую обработку данных осуществляли с помощью программы «Statistica 12.0» (StatSoft, Inc., США) и «SPSS Statistica 17.0» [7, 8].
Результаты исследования и их обсуждение. Результаты специальных лабораторно-инструментальных методов обследования представлены в таблице 2.
Таблица 2
Показатели специальных лабораторно-инструментальных методов обследования в исследуемых группах
|
Показатель |
Контроль n=30 |
Пациенты n=58 |
|
Предшественник натрийуретического пептида типа В, пг/мл |
69,9 [48,9; 91]
|
246,1 [118; 430] р1<0,001 |
|
Проадреномедуллин, нмоль/л
|
0,49 [0,18; 0,58] |
0,89 [0,51; 1,35] р1=0,017 |
|
Трансформирующий фактор роста-β1, нг/мл |
5,8 [3,5; 8,5] |
32,5 [12,2; 55,7] р1<0,001 |
|
Матриксная металлопротеиназа-1, нг/мл |
3,1 [2,8; 3,9] |
4,3 [3,6; 5,4] р1=0,027 |
|
Ингибитор матриксной металлопротеиназы-1, нг/мл |
164,5 [155,8; 176,0] |
348,1 [277,3; 405] р1<0,001 |
|
Индекс левожелудочково-артериального взаимодействия |
0,64 [0,56; 1,02] |
0,78 [0,55; 1,07] р1=0,634 |
Примечание:
n – число пациентов,
р1 – уровень статистической значимости различий с группой контроля
Как показывают приведенные в таблице 2 данные, показатель иЛЖАВ не имел статистически значимых различий с группой контроля, что говорит об оптимальном сопряжении между ЛЖ и сосудистой системой в этой группе. При этом все исследуемые биохимические показатели статистически значимо отличались от контрольных значений, что можно объяснить более ранним реагированием нейрогуморальных систем, нарушения которых наблюдаются уже на ранних стадиях заболевания, предшествуя структурным изменениям органов-мишеней.
Методом логистической регрессии из клинико-анамнестических данных (возраст, индекс массы тела, длительность симптомов ИБС и артериальной гипертонии, функциональный класс стенокардии и хронической сердечной недостаточности, курение), лабораторных (уровни NT-proBNP, MR-proADM, ТФР-β1, ММП-1, ТИМП-1) и инструментальных показателей (конечный диастолический объем ЛЖ, конечный систолический объем ЛЖ, фракция выброса левого желудочка ЛЖ, иЛЖАВ) был произведен отбор переменных (предикторов) для включения в прогностический алгоритм развития ишемической кардиомиопатии (ИКМП). В качестве исходов в представленной модели использовались два варианта развития событий через три года после перенесенного Q-образующего ИМ: 1 – не развилась ИКМП (ЛЖ сохранил свои показатели структуры и функции в пределах референсных значений) и 2 – развилась ИКМП (произошли дилатация и снижение систолической функции ЛЖ).
Полученный алгоритм имел следующий вид: 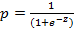 ,
,
где 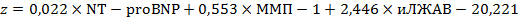 ;
;
р – вероятность развития ИКМП у пациентов ПИМ-СФВ;
NT-proBNP – уровень предшественника натрийуретического пептида типа В;
ММП-1 – уровень матриксной металлопротеиназы-1;
иЛЖАВ – значение индекса левожелудочкового артериального взаимодействия;
е – константа 2,72 (основание натурального логарифма).
Данное уравнение логит-регрессии было отобрано из десятка остальных, так как имело наиболее высокую точность предсказания. Оценка его значимости производилась с использованием Omnibus Test (χ2=51,64, df=1; р<0,001) [7].
В таблице 3 наблюдаемые показатели принадлежности к группе (1 – не развилась ИКМП, 2 – развилась ИКМП) противопоставляются предсказанным показателям на основе предложенного алгоритма.
Таблица 3
Классификационная таблица
|
Наблюдаемый показатель |
Прогнозируемый показатель |
|||
|
Развилась ИКМП |
Процент верных прогнозов |
|||
|
Нет |
Да |
|||
|
Развилась ИКМП |
Нет |
40 |
1 |
96,7 |
|
Да |
3 |
14 |
82,4 |
|
|
Суммарный процентный показатель 93,1 |
||||
Представленные в таблице 3 данные говорят о том, что из 58 (100%) больных, отобранных для прогноза, «строго положительные» результаты получены у 14 пациентов (24%), ложноотрицательные (признаны тестом здоровыми, хотя являются больными) результаты – у 3 пациентов (5%). «Строго отрицательные» результаты получены у 40 пациентов (67%), ложноположительные (признаны больными, хотя являются здоровыми) результаты получены у 1 пациента (2%). Таким образом, правильно были распознаны 54 случая, что составляет 93,1%.
Диагностическая чувствительность разработанного нами прогностического алгоритма составила 93%. Диагностическая специфичность теста составила 93%. Точность (диагностическая эффективность теста) составила 93%. Прогностическая ценность положительного результата составила 97%. Прогностическая ценность отрицательного результата составила 17,6%.
Кроме этого, была рассчитана прогностическая критериальная валидность теста (коэффициент валидности r=0,68).
Проверка значимости коэффициентов проводилась при помощи статистики Вальда [8] (табл. 4). Уровень статистической значимости коэффициентов модели меньше 0,05 указывает на статистическую значимость результатов прогнозирования при помощи данной математической модели.
Таблица 4
Уровни статистической значимости коэффициентов разработанной математической модели прогнозирования риска развития ишемической кардиомиопатии
|
Step 1 |
β-коэффициент регрессии |
Стандартная ошибка β-коэффициента |
Значение статистического критерия Вальда |
Число степеней свободы |
p |
|
NT-proBNP |
0,022 |
0,009 |
5,733 |
1 |
0,017 |
|
ММП-1 |
0,553 |
0,274 |
4,060 |
1 |
0,044 |
|
иЛЖАВ |
2,446 |
1,169 |
4,383 |
1 |
0,036 |
|
Constant |
-20,221 |
7,992 |
6,402 |
1 |
0,011 |
Следует обратить внимание на то, что при пошаговом включении отобранных предикторов (показатели NT-proBNP и ММП-1, иЛЖАВ) уравнение c одним предиктором – NT-proBNP – обеспечивало уровень конкордации в 84,5%, тогда как с двумя предикторами (NT-proBNP и ММП-1) эта величина составила уже 89,7%, то есть второй предиктор увеличил уровень конкордации на 5,2%. Включение в модель показателя иЛЖАВ также увеличивало уровень конкордации еще на 3,4%. Последующее пошаговое включение в алгоритм других предикторов не приводило к увеличению уровня конкордации и было признано нецелесообразным.
Также оценка качества разработанной модели проводилась при помощи ROC-анализа с расчетом площади под ROC-кривой (AUC) [7]. При включении в прогностическую модель одного предиктора – NT-proBNP – показатель AUC составил 0,77 с 95%-ным доверительным интервалом (ДИ) 0,616–0,923, что указывало на хорошее (AUC в диапазоне 0,7–0,8) качество данной математической модели. При включении в модель двух предикторов (NT-proBNP и ММП-1) AUC увеличивался до 0,841 (95% ДИ 0,704; 0,977). Для модели, включающей три предиктора (NT-proBNP, ММП-1, иЛЖАВ), AUC составил 0,9 (95% ДИ 0,788; 1,011), что указывало на отличное качество разработанного алгоритма.
В изученной нами литературе мы не нашли подобных моделей. Тем не менее нам встретились модели прогнозирования развития постинфарктной дилатации ЛЖ, в одной из которых в качестве предикторов выступали уровень ТИМП-1 и концентрация молекул межклеточной адгезии сосудистого эндотелия (sVCAM-1) [9], а в другой – параметры тканевой эхокардиографии, относящиеся к острому периоду ИМ (максимальная элевация ST на исходной электрокардиографии; суммарная элевация ST и число отведений с зубцом Q после тромболизиса; максимальные концентрации креатинкиназы и МВ-фракции креатинкиназы; исходные эхокардиографические показатели – индекс локальной сократимости, конечно-диастолический и конечно-систолический индексы, а также специальные параметры тканевого допплеровского исследования – индекс суммарной скорости Em непораженного миокарда ЛЖ и индекса IVC зоны дисфункции) [10].
Заключение. Учитывая высокую специфичность и чувствительность предложенного алгоритма для расчета индивидуального риска развития ИКМП, он может быть использован наряду с общепринятыми медицинскими исследованиями для определения тактики ведения пациентов после перенесенного Q-образующего ИМ и разработки индивидуальных лечебно-профилактических мероприятий для повышения их эффективности.
Библиографическая ссылка
Мясоедова Е.И., Воронина Л.П., Санджиева С.С., Полунина О.С., Шварц Ю.Г. ПРОГНОЗИРОВАНИЕ РАЗВИТИЯ ИШЕМИЧЕСКОЙ КАРДИОМИОПАТИИ // Современные проблемы науки и образования. 2019. № 2. ;URL: https://science-education.ru/en/article/view?id=28781 (дата обращения: 07.05.2026).



