Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
RETROMUSCULAR HERNIOPLASTY COMPLICATED BY NECROTIC CELLULITIS OF THE ABDOMINAL WALL
В настоящее время протезирующая пластика передней брюшной стенки является рутинной операцией. Ежегодно в Российской Федерации выполняется около 200 000 подобных оперативных вмешательств, а удельный вес этого оперативного вмешательства в общехирургических стационарах составляет 10-21% [1]. Послеоперационные осложнения не являются редкостью: частота их развития при применении сетчатых протезов составляет от 37 до 52%, превалируют серомы и гематомы, инфекция области хирургического вмешательства [2; 3]. Известно, что на фоне сахарного диабета риск развития гнойно-септических осложнений особенно высок. Одним из частных случаев гнойного осложнения после герниопластики сетчатым эндопротезом является некротический целлюлит, возникающий в 13% случаев, и который по тяжести протекания инфекционного процесса нередко приводит к летальному исходу [4]. Некротический целлюлит – это острая инфекция мягких тканей, рассматриваемая как локализованная форма септического васкулита с формированием в сосудах фибриновых тромбов при местной и генерализованной бактериальной инфекции [5]. В представленной статье рассмотрен клинический случай некротического целлюлита передней брюшной стенки после плановой ретромускулярной герниопластики на фоне сахарного диабета 2 типа.
Цель исследования: показать возможность развития некротического целлюлита передней брюшной стенки после плановой герниопластики у пациентки с сахарным диабетом 2 типа.
Клинический случай
Больная З., 67 лет, поступила 03.04.2018 года в плановом порядке по направлению хирурга поликлиники в хирургическое отделение Государственного бюджетного учреждения здравоохранения Нижегородской области «Городская клиническая больница № 30 Московского района г. Нижнего Новгорода» с жалобами на наличие грыжевого выпячивания передней брюшной стенки в области послеоперационного рубца. Из анамнеза выяснилось, что пациентка год назад перенесла нижне-срединную лапаротомию, надвлагалищную ампутацию матки по поводу фибромы. Грыжевое выпячивание заметила около полугода назад. С течением времени образование увеличивалось в размерах.
При физикальном обследовании обращал на себя внимание выраженный кожно-жировой «фартук». Локально: в области послеоперационного рубца передней брюшной стенки после нижнесрединной лапаротомии имеется грыжевое выпячивание размером 8х6 см, в брюшную полость вправляется, кашлевой толчок положительный, ущемлений не было. Дефект апоневроза 4х5 см. По данным ультразвукового исследования грыжевого выпячивания и прилежащих отделов передней брюшной стенки, в подкожной жировой клетчатке располагается грыжевой мешок, содержимое – петли кишечника, перистальтируют, грыжевых вод нет. Других дефектов апоневроза не обнаружено. Лигатурных гранулем также не было определено. Пациентке выполнена оценка функции внешнего дыхания (жизненная емкость легких – 90%, объем форсированного выдоха за 1 секунду – 85%).
Диагноз при поступлении: послеоперационная вентральная грыжа М3W2R1 (по Chevrel J.P., Rath A.M., 2000). Сопутствующие заболевания: ишемическая болезнь сердца: стенокардия напряжения, 2 ФК, ХСН 2 ст.; гипертоническая болезнь 2 степени, риск 4. Сахарный диабет II типа, вторичноинсулинпотребный. Ожирение 3 степени.
Пациентке планово выполнена ретромускулярная пластика по Rives и Stoppa сетчатым эндопротезом Эсфил стандартный (производитель ООО «Линтекс», Россия), однако с созданием моста между передними листками прямых мышц живота. Оперативное вмешательство выполнено без технических особенностей: без вскрытия грыжевого мешка выполнено рассечение переднего листка апоневроза прямых мышц живота, трансплантат фиксирован в позадимышечном пространстве узловыми швами к заднему листку апоневроза. На микробиологическое исследование направлены лигатуры апоневроза с окружающими тканями (гранулемы) после ранее выполненной операции. Передний листок апоневроза фиксирован к сетчатому эндопротезу без натяжения, оставляя свободную поверхность эндопротеза общей площадью около 3 см2. Рана ушита узловыми швами, выполнено дренирование ретромускулярного пространства и подкожной жировой клетчатки по Редону.
Ранний послеоперационный период протекал без осложнений: после операции пациентка переведена в палату, через сутки активизирована (по рекомендациям анестезиологов ввиду выполненной спинномозговой анестезии). По дренажу Редона на 1-е и 2-е сутки после операции 50 и 20 мл геморрагического отделяемого соответственно, на 3-и сутки после операции дренаж удален ввиду отсутствия отделяемого по нему. Через 4 суток после операции вечером зафиксировано повышение температуры тела до 38,2 °С. Пациентка предъявляла жалобы на потливость, озноб. Местно: рана заживала первичным натяжением, швы – состоятельные, отека, гиперемии на момент осмотра не было. Назначена антибактериальная терапия (цефтриаксон 1 грамм 1 раз в сутки). На следующий день выполнено ультразвуковое исследование послеоперационной раны, с помощью которого визуализирована послеоперационная гематома, располагавшаяся в нижней трети послеоперационного рубца в подкожной жировой клетчатке над эндопротезом (объем жидкости до 50 мл). Под контролем ультразвука выполнена пункция и эвакуация около 40 мл темной прозрачной жидкости геморрагического характера, без запаха.
После эвакуации послеоперационной гематомы на 6-е сутки после операции сохранялась фебрильная лихорадка (38,0-38,3 °С), пациентка предъявляла жалобы на слабость, потливость. Локально: в верхнем краю раны появилась незначительная гиперемия и умеренная болезненность при пальпации (1х1 см). В анализах отмечался лейкоцитоз (лейкоциты 13,2х109/л) со сдвигом лейкоцитарной формулы влево. Повторное ультразвуковое исследование не выявило патологических жидкостных образований в ране.
На 7-е сутки после операции пациентка стала отмечать выраженные боли в послеоперационной ране, озноб, появилась анурия (объем инфузии и выпитой жидкости составил 1,5 л, по данным УЗИ мочевого пузыря и мочевыводящих путей – без патологии, мочевой пузырь пустой). Температура тела составила 38,5 °С. Дважды выполнено ультразвуковое исследование послеоперационной раны, однако данный метод исследования причины ухудшения состояния не выявил. Консультирована инфекционистом, данных за острое инфекционное заболевание не выявлено. Местно: кожа раны умеренно гиперемирована в верхнем краю раны, в остальном – без особенностей. Были сняты 2 шва с верхнего края раны, откуда выделилось около 15 мл мутного темно-коричневого отделяемого с гнилостным запахом. Взят посев на микрофлору и чувствительность к антибиотикам. С послеоперационной раны сняты все швы, стенки раневого дефекта в верхней трети раны (в области пупка) с участками гнойно-некротических тканей с гнилостным запахом, в нижней трети рана зажила первичным натяжением (рисунок 1).
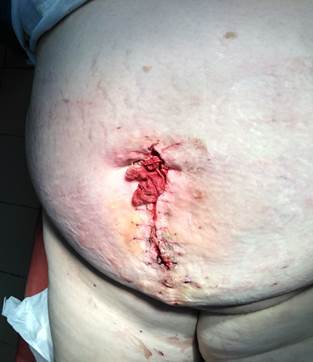
Рис. 1. 7-е сутки после герниопластики. Отмечается невыраженная гиперемия передней брюшной стенки (преимущественно справа от раны), обильное раневое отделяемое геморрагического характера с гнилостным запахом. Швы сняты
Рана санирована 3%-ным раствором перекиси водорода, девитализированные ткани удалены острым путем. Размер раны: 10х3х2 см, дно – сетчатый эндопротез с участками фибрина и некротическими тканями, из раны – гнойное отделяемое. Установлены 2 дренажные трубки в рану (рисунок 2).
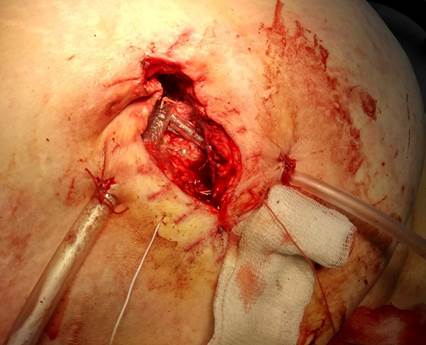
Рис. 2. Ко дну раны, представленному сетчатым протезом, через контрапертуры установлены трубчатые дренажи
Выполнено проточно-промывное дренирование послеоперационной раны с активной аспирацией, на края раны наложены узловые швы (рисунок 3).
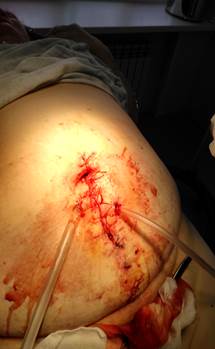
Рис. 3. Вид раны после завершения операции
Пациентке выполнялась инфузионная терапия (1200 мл 0,9%-ного раствора хлорида натрия), антибактериальная терапия (цефтриаксон, метрогил), диуретики (лазикс 40 мг), в результате чего диурез составил около 500 мл. В анализах: Ле – 16,1 * 109/л со сдвигом лейкоцитарной формулы влево, глюкоза – 7,22 ммоль/л, умеренное повышение мочевины – 8,14 ммоль/л и креатинина – 120 мкмоль/л. Остальные показатели – в пределах нормы. По проточно-промывной системе влито около 400 мл водного раствора хлоргексидина, получено около 350 мл темно-красной жидкости с хлопьями фибрина с неприятным запахом. Результат бактериологического исследования: St. aureus 107 КОЕ/л, чувствительный к метронидазолу, цефтриаксону.
Несмотря на проведенное лечение, у пациентки наблюдалось ухудшение состояния в виде увеличения болевого синдрома в области передней брюшной стенки, покраснения кожи передней брюшной стенки с образованием множественных пузырей кожи в диаметре до 1 см с мутным геморрагическим отделяемым справа от лапаротомной раны. На фоне прогрессирования гнойного процесса и ухудшения общего состояния пациентки в виде появления сердечно-сосудистой недостаточности (стойкая гипотония) и почечной недостаточности (анурия, повышение показателей мочевины и креатинина) на 9-е сутки после герниопластики пациентка переведена в отделение реанимации для кратковременной предоперационной подготовки с последующим выполнением хирургической обработки гнойного очага в условиях операционной (рисунок 4).
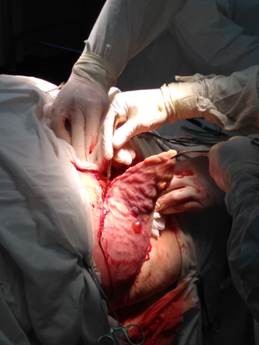
Рис. 4. Иссечение изменённого кожного-подкожного лоскута
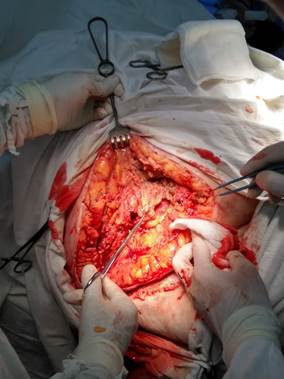
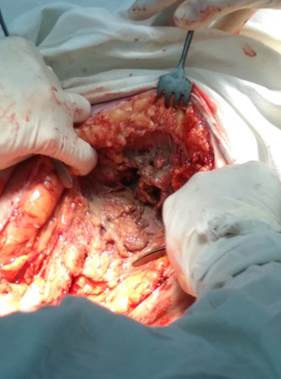
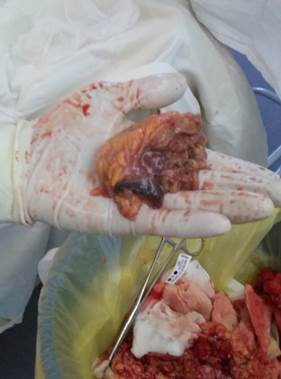
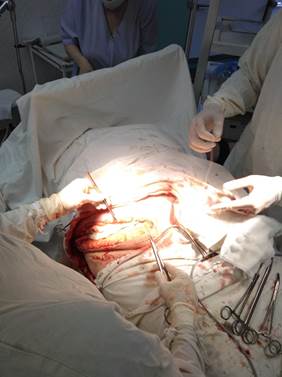
После удаления измененного кожного лоскута двумя полуовальными разрезами длиной до 25 см выполнена ревизия надапоневротического затека по подкожной жировой клетчатке по направлению к послеоперационной ране: жировая ткань с признаками гнойного расплавления с участками девитализированных тканей с гнилостным запахом, однако же прямого сообщения с послеоперационной раной выявлено не было. Взят посев на микрофлору и чувствительность к антибиотикам (рисунки 5-8).
5. 6.
7. 8.
Рис. 5-8. Вид раны после иссечения кожного лоскута: гнойное расплавление жировой ткани. Тампонирование раны марлевым тампоном с мазью левомеколь
После хирургической обработки гнойного очага пациентка получала лечение в течение 3 суток в отделении реанимации, после стабилизации витальных функций переведена в хирургическое отделение, где дважды в сутки выполнялись перевязки ран. Результат бактериологического исследования: Acinetobacter baumannii 107 КОЕ/л, чувствительный к цефокситину. В результате санации раны 3%-ным раствором H2O2, марлевыми тампонами с левомеколем отмечалось очищение раны: уменьшение общего объема девитализированных тканей, увеличение нормальной жировой ткани (рисунок 9).
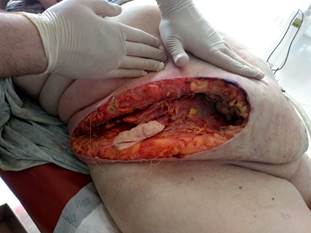
Рис. 9. На 10-е сутки после хирургической обработки гнойного очага отмечается разрастание грануляций, уменьшение локального отёка, паравульнарной гиперемии, уменьшение объема некротических тканей
В результате адекватной хирургической обработки и комплексного лечения некротического целлюлита подкожной жировой клетчатки у пациентки наступил регресс гнойно-некротического процесса, через 25 суток после хирургической обработки гнойного очага рана очистилась, на 90% заполнилась грануляционной тканью, с латерального края раны наложены узловые швы, частично закрывающие рану (рисунок 10).
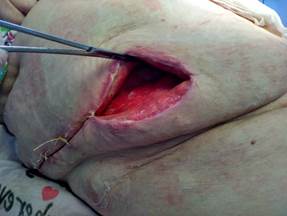
Рис. 10. Через 25 суток после хирургической обработки гнойного очага: рана очистилась, объем грануляционной ткани увеличился. Наложены вторичные швы
Ещё через 3 суток выполнено полное ушивание послеоперационной раны узловыми швами после иссечения рубцово измененных краев, в рану помещен марлевый тампон с мазью левомеколь (рисунок 11).
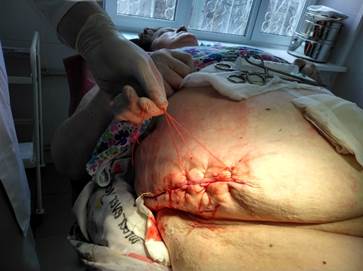
Рис. 11. Вид раны после наложения узловых швов
На 42-е сутки после хирургической обработки гнойного очага наступило заживление срединной послеоперационной раны вторичным натяжением (на рану были наложены 2 узловых шва до сопоставления краев раны), эндопротез удален не был, рана в проекции жирового «фартука» справа зажила по типу первичного натяжения, пациентка выписана, швы сняты (рисунок 12).
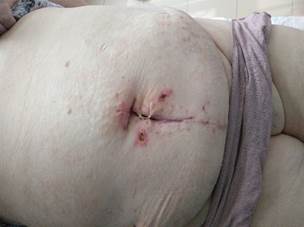
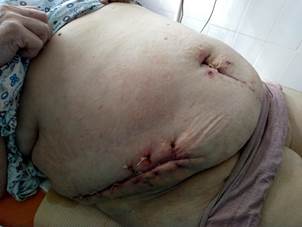
А. Б.
Рис. 12. Вид лапаротомной раны (А) и раны в области жирового «фартука» справа (Б) перед снятием швов на 42-е сутки после хирургической обработки гнойного очага
Заключение
Таким образом, в нашей хирургической практике мы встретились с редким осложнением протезирования дефекта апоневроза сетчатым имплантатом в виде некротического целлюлита передней брюшной стенки. Такое обширное и молниеносное расплавление подкожной жировой клетчатки можно отнести к сложным проблемам не только гнойной хирургии, но и плановой протезирующей герниопластики.
Мы ещё раз подтвердили, что только наиболее раннее и адекватное хирургическое вмешательство является ключевым компонентом в лечении некротического целлюлита. Только оно позволяет санировать очаг инфекции, что в сочетании с эмпирической, а затем и этиотропной антибиотикотерапией увеличивает шансы пациента на благоприятный исход.
Добровольное информированное согласие пациента: пациентка дала письменное информированное согласие на опубликование данного материала (в т.ч. фотографий) в медицинских журналах (включая их электронные версии).
Библиографическая ссылка
Багрянцев М.В., Лукоянычев Е.Е., Триколе А.И., Сизов М.А., Шахов А.В., Воробьев А.Н., Батраков И.Е., Удалова М.И. РЕТРОМУСКУЛЯРНАЯ ГЕРНИОПЛАСТИКА, ОСЛОЖНЕННАЯ НЕКРОТИЧЕСКИМ ЦЕЛЛЮЛИТОМ ПЕРЕДНЕЙ БРЮШНОЙ СТЕНКИ (КЛИНИЧЕСКИЙ СЛУЧАЙ) // Современные проблемы науки и образования. 2019. № 2. ;URL: https://science-education.ru/en/article/view?id=28698 (дата обращения: 07.06.2026).



