Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
INDICATORS OF CELLULAR COMPOSITION AT EXPERIMENTAL COLD EFFECTS
В связи с усиленными темпами освоения Крайнего Севера в настоящее время вопрос адаптации организма человека к жизни в северных широтах, где он подвергается воздействию низких природных температур, вновь становится актуальным [1; 2].
Известно, что на негативное воздействие различных факторов окружающей природной среды организм человека отвечает мобилизацией адаптационных механизмов регуляции функционирования систем, в том числе и системы крови, что может проявляться изменением её клеточного состава [3; 4]. В осуществлении защитной реакции организма большую роль играют лейкоциты, которые обеспечивают неспецифический и специфический клеточный иммунитет организма и отвечают на воздействия любых стресс-факторов. При длительном или чрезвычайно сильном воздействии неблагоприятных факторов происходят изменения иммунологической реактивности, приводящие к снижению адаптационных возможностей организма, к развитию транзиторных или стойких форм вторичной иммунной недостаточности [5].
Дисбаланс иммунной системы оказывает влияние на формирование, характер течения и исходы многих патологических процессов. Наиболее высокие уровни заболеваемости в условиях Крайнего Севера приходятся на болезни органов дыхания, нервной системы, органов чувств и системы кровообращения [1; 6; 7].
Таким образом, актуальность исследования механизмов адаптации системы крови и реакций иммунных органов на холодовое воздействие продиктована необходимостью поиска путей повышения сопротивляемости организма к низким температурам, разработки мер профилактики и коррекции нарушений иммунного ответа организма людей, постоянно и временно проживающих в условиях Заполярья, в том числе и Республики Саха (Якутия). Эта медико-социальная проблема требует глубокой и всесторонней проработки, прежде всего, на теоретическом уровне.
Данное исследование является частью комплексной работы, связанной с изучением механизмов дезадаптации в условиях Арктики и Субарктики. Данная работа проводится с учетом приоритетных направлений научной платформы «Иммунология» государственной программы «Стратегия развития медицинской науки в Российской Федерации на период до 2025 года».
Целью исследования является изучение изменений клеточного состава крови крыс в зависимости от времени их экспозиции в условиях холодового воздействия.
Материалы и методы исследования. Исследование проводили на 40 беспородных крысах-самцах массой тела 200-300 г. Выбор пола животных был продиктован необходимостью получения стабильных результатов, исключая влияние циклических изменений, характерных для организма самок. Методом случайной выборки животные были распределены на контрольную группу и опытную, разделенную на 4 подгруппы по 8 особей в каждой. Животные находились в стандартных условиях вивария, соответствующих требованиям санитарно-эпидемиологических правил СП 2.2.1.3218-14 «Санитарно-эпидемиологические требования к устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев)» (2014). Экспозицию опытных крыс производили в холодильных камерах при температуре -20 ºС с соблюдением адекватных условий влажности и вентиляции в течение 60 минут ежедневно на протяжении 30 суток.
Протокол экспериментальной части исследований, использованный на этапах содержания животных, моделирования патологических процессов и выведения их из опыта, соответствовал принципам биологической этики, изложенным в Международных рекомендациях по проведению медико-биологических исследований с использованием животных (1985); Европейской конвенции о защите позвоночных животных, используемых для экспериментов или иных научных целей (Страсбург, 1986); Приказе МЗ СССР № 755 от 12.08.1977 г. «О мерах по дальнейшему совершенствованию организационных форм работы с использованием экспериментальных животных»; Приказе МЗ РФ № 267 от 19.06.2003 г. «Об утверждении правил лабораторной практики» [8].
Исследования проводили сразу после получения проб крови на 7-е (1-я подгруппа),
14-е (2-я подгруппа), 21-е (3-я подгруппа), 30-е сутки (4-я подгруппа) после начала эксперимента. Животных выводили из опыта методом декапитации с соблюдением требований гуманности, согласно Приложению № 4 «О порядке проведения эвтаназии (умерщвления) животного» к Правилам проведения работ с использованием экспериментальных животных (приложение к Приказу МЗ СССР № 755 от 12.08.1977). Кровь получали во время декапитации животного. Гематологические исследования проводили на автоматизированном гематологическом анализаторе AbacusJunior 30, биохимические исследования сыворотки крови – на биохимическом анализаторе Mindray BA-88A с применением растворов HigtTehnology.
Статистическую обработку данных осуществляли с использованием пакета программ Statistica 6.0. После проверки вариационных рядов на правильность распределения значимость различий между ними определяли параметрическим методом с расчётом средней арифметической, ошибки средней арифметической (М±m) и t-критерия Стьюдента. Различие считали значимым при р <0,05.
Работа выполнена в Медицинском институте СВФУ им. М.К. Аммосова, исследование крови и сывороток крови выполнено в научно-исследовательской клинико-диагностической лаборатории для сельскохозяйственных и домашних животных Якутской ГСХА.
Результаты исследования и их обсуждение. В результате проведенных исследований установлены показатели периферической крови контрольных и опытных групп животных до и после воздействия холода. Показатели контрольной группы животных, содержавшихся в оптимальных условиях температуры, соответствуют физиологической норме [8], в то время как результаты, полученные у крыс, подвергавшихся холодовому воздействию, свидетельствуют об изменениях количественного состава всех форменных элементов периферической крови в разные сроки эксперимента (табл.).
Динамика показателей периферической крови крыс, подвергнутых холодовому воздействию
|
Показатели, ед. изм. |
Контрольная группа |
Опытные подгруппы (n = 32) |
|||
|
7-е сутки |
14-е сутки |
21-е сутки |
30-е сутки |
||
|
Лейкоциты, 10?/л |
14,50±1,32 |
9,36±2,47 |
15,96±2,49 |
6,91±1,24* |
6,99±0,62* |
|
Лимфоциты, % |
57,87±1,26 |
78,57±2,74* |
72,97±2,60* |
60,37±,15 |
79,75±2,15* |
|
MID, % |
14,4±1,98 |
11,52±1,18 |
15,01±0,61 |
7,88±1,44* |
4,91±1,44* |
|
Гранулоциты,% |
25,91±2,05 |
9,9±2,24* |
13,92±2,61* |
25,97±4,1 |
13,83±0,75* |
|
Эритроциты, 10¹²/л |
7,59±1,17 |
6,98±0,38 |
7,2±0,65 |
8,09±1,09 |
5,97±1,29 |
|
Гемоглобин, г/л |
127,75±1,93 |
127,75±6,87 |
132,62±10,83 |
140,12±14,82 |
120,5±13,77 |
|
Гематокрит, % |
43,29±0,72 |
41,73±2,40 |
40,33±3,67 |
58,24±5,99* |
46,14±6,8 |
|
MCV, фл |
57,25±0,52 |
59,62±0,69 |
57,62±0,66 |
66,1±0,56* |
66,07±1,05 |
|
МСН, пг |
17,41±0,22 |
18,32±0,21* |
17,86±0,25 |
15,.47±0,23* |
17,61±0,15 |
|
МСНС, г/л |
310,87±4,6 |
306,62±3,33 |
305,87±3,88 |
233,25±3,03* |
262,62±3,58* |
|
RDWc, % |
18,18±0,28 |
17,3±0,34 |
17,61±0,32 |
16,03±0,33* |
15,21±0,46* |
|
Тромбоциты, 10?/л |
931,7±36,27 |
860,87±56,4 |
885,62±76,79 |
354,62±119,09* |
483,75±111,02 |
Примечание: n - число наблюдений; * – статистически значимое отличие от данных контрольной группы (p<0,05).
Результаты исследования свидетельствуют о том, что холодовое воздействие оказывает влияние на количество клеток, обеспечивающих реакции неспецифического и специфического иммунного ответа. Уже на 7-е сутки эксперимента наблюдается тенденция снижения общего количества лейкоцитов крови (на 35,5%), которое переходит в значимое на 21-е и 30-е сутки (на 52,3% и 51,8% соответственно), несмотря на то что на 14-е сутки отмечается незначительное повышение числа клеток (на 10,1%) по сравнению с данными контрольной группы (табл., рис. 1).

Рис. 1. Общее количество лейкоцитов (х10?/л) у опытных животных в сравнении с контрольной группой в разные сроки эксперимента
В то же время количество лимфоцитов остается повышенным в течение всего эксперимента, статистически значимо возрастая на 7, 14 и 30-е сутки (на 35,7, 26,1 и 37,8% соответственно) (рис. 2).
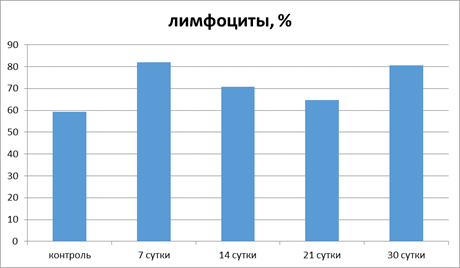
Рис. 2. Изменения относительного количества лимфоцитов в разные сроки эксперимента
в сравнении с контрольной группой
MID – показатель, отражающий содержание смеси моноцитов, эозинофилов, базофилов и незрелых клеток, достоверно снижается на 21-е сутки на 45,3%; на 30-е сутки – на 65,9% по сравнению с контрольной группой. Количество гранулоцитов (эозинофилов, нейтрофилов и базофилов) статистически значимо снижается на 7, 14 и 30-е сутки (на 61,8, 46,3 и 46,6% соответственно), а на 21-е сутки эксперимента соответствует контрольной величине (рис. 3).
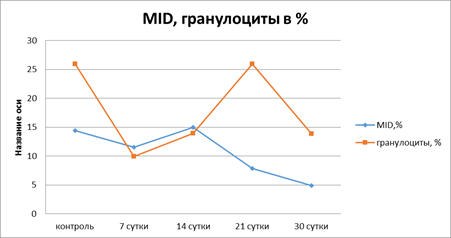
Рис. 3. Динамика изменений относительных показателей MID и гранулоцитов
в разные сроки эксперимента по сравнению с контрольной группой
Значительное снижение общего количества лейкоцитов как на 7-е, так и на 21-е и 30-е сутки эксперимента свидетельствует о том, что холодовое воздействие действительно является стрессовым фактором для теплокровных животных. Это соответствует результатам, полученным Е.Г. Костоломовой, согласно которым популяции изолированных иммунокомпетентных клеток (ИКК) по-разному реагируют на длительность холодовой экспозиции [9]. Кратковременное охлаждение является фактором, активирующим функциональную активность моноцитов и нейтрофилов, а длительное - угнетающим. В исследованиях В.М. Николаева также отмечалось, что при адаптации крыс к гипотермии изменяются показатели неспецифического клеточного иммунитета, связанные с фагоцитарной активностью лейкоцитов [10]. Статистически значимое уменьшение среднего числа поглощённых частиц лейкоцитами как в первой, так и во второй группах экспериментальных животных свидетельствует об угнетении неспецифического клеточного иммунитета при воздействии отрицательных температур. Будем полагать, что в нашем эксперименте экспозиция крыс в условиях низкой температуры в течение от 7 до 30 суток, сопровождавшаяся подавлением активности лейкоцитов, являлась достаточно длительной. Однако увеличение числа лейкоцитов на 14-е сутки (на 10,1% по отношению к контролю и на 45,6% относительно показателя на 7-е сутки) связано с кратковременной стимуляцией лейкоцитопоэза. В экспериментальных работах И.И. Шахматова на крысах-самцах линии Вистар, подвергнутых комбинированному (холодовому) плаванию в воде при температуре +7 °С, показано повышение количества лейкоцитов преимущественно за счет резкого нарастания гранулоцитов. Авторы утверждают, что в результате действия холодового фактора стимулируется специфический иммунный ответ, а реакции неспецифического ответа, опосредованные лейкоцитами, – подавляются [11].
Обращает на себя внимание существенное снижение количества тромбоцитов в периферической крови после воздействия холода на организм. Так, на 21-е сутки эксперимента отмечалось статистически значимое снижение количества тромбоцитов до 354,62±119,09 (х10?/л) по сравнению с контрольными показателями. Значительное снижение тромбоцитов отмечалось и на 30-е сутки эксперимента. Наблюдаемые нами изменения в гематологическом статусе данных животных согласуются с литературными данными, в которых описано уменьшение числа тромбоцитов, как реакция на стресс. Уменьшение количества тромбоцитов при чрезмерном холодовом воздействии объясняется непосредственным участием их в воспалительных и репаративных процессах. При тяжелом холодовом повреждении тканей происходит превалирование их потребления над продукцией, что приводит к снижению количества кровяных пластинок и появлению незрелых молодых форм с низким ферментативным и медиаторным потенциалом, что, в свою очередь, реализуется в снижении их адгезивно-агрегационной способности [12].
Повышение гематокрита, эритроцитов – одна из количественных характеристик физиологической «подстройки» организма к новым условиям жизни. Повышенный гематокрит и одновременное усиление синтеза эритропоэтина, стимулирующего созревание эритроцитов, может быть одним из признаков реакции на стресс, в нашем случае на холодовой [3].
Заключение. Таким образом, холодовое воздействие является стрессом, выражающимся в реакции со стороны всего клеточного состава крови. В результате действия холодового фактора стимулируется специфический иммунный ответ, на что указывает увеличение в крови количества лимфоцитов, а реакции неспецифического ответа, опосредованные другими видами лейкоцитами, – подавляются. Уменьшение количества тромбоцитов также представляется как целесообразная реакция организма в ответ на холодовое воздействие, так как тромбоциты принимают непосредственное участие в репаративных процессах, наблюдающихся при повреждении ткани холодом. Повышенный показатель гематокрита свидетельствует об увеличении доли форменных элементов крови относительно плазмы и является достоверным критерием ответной реакции на стресс.
Дальнейшие исследования коснутся изучения процессов пролиферации и дифференцировки иммунокомпетентных клеток органов и тканей лимфоидного комплекса (селезенка, тимус, лимфатические узлы, МАЛТ полых органов) при холодовой нагрузке.
Библиографическая ссылка
Гармаева Д.К., Аржакова Л.И., Дмитриева Т.И., Павлова Н.И., Гармаев Ц.К. ПОКАЗАТЕЛИ КЛЕТОЧНОГО СОСТАВА КРОВИ ПРИ ЭКСПЕРИМЕНТАЛЬНОМ ХОЛОДОВОМ ВОЗДЕЙСТВИИ // Современные проблемы науки и образования. 2019. № 1. ;URL: https://science-education.ru/en/article/view?id=28441 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.28441



