Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE EFFECT OF VARIOUS METHODS OF ENDOSURGICAL HEMOSTASIS ON THE OVARIAN RESERVE IN CASE OF ENUCLEATION OF ENDOMETRIOMAS IN PATIENTS OF LATE REPRODUCTIVE AGE
Среди гинекологической патологии эндометриоидные кисты яичников (ЭКЯ) стабильно занимают третье место и в структуре хирургической активности занимают одно из ведущих мест [1-3]. При этом даже при небольших размерах ЭКЯ у пациенток может наблюдаться снижение овариального резерва [3], причиной снижения которого в том числе является теория «выгорания» (burnout theory). Известно, что процесс снижения овариального резерва связан с атрезией на стадии малых антральных фолликулов, преимущественно посредством апоптоза. Причиной апоптоза и некроза примордиальных фолликулов при ЭКЯ и как следствие снижения овариального резерва является исходный оксидативный стресс, влияющий в том числе и на здоровую ткань яичника [4]. Многочисленными исследованиями было доказано, что генитальный эндометриоз сопровождается исходным дисбалансом цитокинов как периферической крови, так и перитонеальной жидкости, с преобладанием провоспалительного компонента и усилением проапоптического влияния [5, 6] и связь процессов в системе перекисного окисления липидов и антиоксидантной защиты (ПОЛ/АОЗ) и характеристик цитокинового статуса. Предполагается, что цитокиновый дисбаланс является одним из механизмов реализации оксидантного стресса, протекающего в дальнейшем с дестабилизацией липопероксидации и антиокислительной активности [6]. В случае необходимости хирургической операции (энуклеация кисты) важнейшей задачей является сохранение овариального резерва, тем более в позднем репродуктивном возрасте, с целью сохранения желанной фертильности и женского здоровья. Однако при использовании малоинвазивных технологий основным средством достижения гемостаза стали различные виды электрохирургического воздействия (что не может не приводить к дополнительному негативному воздействию на овариальную ткань), которые сопровождаются некрозом тканей, избыточным белковым катаболизмом и выраженным апоптозом клеток здоровой ткани яичника с развитием эндотоксикоза в той или иной степени в зависимости от используемых энергий. Поэтому поиск технологий интраоперационного гемостаза, минимально влияющих на систему ПОЛ/АОЗ и цитокиновом балансе и как следствие сохраняющих овариальный резерв, в том числе и у женщин позднего репродуктивного возраста, является одной из актуальных задач современной гинекологии.
Цель. Изучить влияние на овариальный резерв токсических метаболитов и изменений в цитокиновом балансе перитонеальной жидкости, полученных в результате различных методов эндохирургического гемостаза при энуклеации эндометриоидной кисты яичников у пациенток в позднем репродуктивном возрасте.
Материал и методы исследования. Обследованы 109 пациенток, прооперированных по поводу односторонней эндометриоидной кисты яичника. Всем им произведена эндохирургическая цистэктомия в плановом порядке. Размеры кист колебались от 40 до 60 мм (48,6±7,1 мм). В качестве адъювантной терапии все пациентки применяли диеногест 2 мг в сутки в течение всего периода наблюдения и далее до 6–9 месяцев в зависимости от репродуктивных планов. В соответствии с целью исследования пациентки были разделены на 3 клинические группы в зависимости от метода интраоперационного гемостаза. Пациенткам 1-й группы проведена биполярная коагуляция сосудов ложа кисты, пациенткам 2-й группы – аргоноплазменная коагуляция, 3-й группы – ложе кисты коагулировано с помощью применения рассасывающегося гемостатического материала, изготовленного по методу контролируемого окисления восстановленной целлюлозы. Группой контроля явились 35 условно здоровых женщин, поступивших на хирургическую стерилизацию. Определение принадлежности к стадии репродуктивного возраста для контрольной группы проводилось по критериям Рабочей группы по стадиям старения репродуктивной системы (STRAW+10).
Включение пациенток в клиническое исследование проводилось методом случайной выборки после получения информированного согласия и протоколировалось по стандартам Этического комитета Российской Федерации.
Из исследования исключались женщины с миомой матки, с рецидивом эндометриоидной кисты, с доброкачественными опухолями яичников другой этиологии или подозрением на малигнизацию образования, а также с наличием тяжелой соматической патологии либо другой экстрагенитальной патологии в стадии обострения.
Перед операцией определяли фолликулярный резерв по уровню антимюллерова гормона с помощью соответствующих тест-систем на иммунохимическом анализаторе «Access/DxI». Проводили исследование органов малого таза с определением размера кисты при помощи трансвагинального конвексного датчика на аппарате экспертного класса на аппаратах «Toshiba Aplio 500» с частотой 5 мГц и 6,5 мГц в режимах серой шкалы.
Во время операции и в первые сутки послеоперационного периода проводили забор перитонеальной жидкости, в которой определяли уровни содержания цитокинов (TNF-α, IL6, IL2, IL10, TNF-α) методом ИФА (ASCENT, Финляндия) и использованием панели моноклональных антител (ЗАО ВЕКТОР-БЕСТ, г. Ростов-на-Дону) расчетом провоспалительного индекса (ПВИ) как отношение IL6/IL10 (у.е). Содержание токсических метаболитов (диеновых конъюгатов (ДК) ненасыщенных жирных кислот, малонового диальдегида (МДА) и молекул средней массы (МСМ)) и антиоксидантная система (активности супероксиддисмутазы (СОД)) перитонеальной жидкости оценивались по соответствующим методикам. Рассчитывался коэффициент, определяющий баланс в системе ПОЛ/АОЗ, как отношение МДА/СОД.
Статистический анализ полученных данных проводился с использованием пакета анализа Microsoft Excel 2000 и программы «STATISTICA» 6,0. Характеристики пациентов сравнивались посредством непарного t-критерия Стьюдента, корреляция Спирмена использовалась для оценки соотношения между переменными.
Результаты исследования и их обсуждение
Группы исследования были практически однородны по клинико-анамнестическому статусу. Средний возраст пациенток составил 37,8±2,5 лет. Средний ИМТ – 27,8±6,2 кг/м². Планировали наступление беременности 32 пациентки (29,4%). Первичное бесплодие выявлено у 12 (11%), вторичное – у 16 (14,7%) пациенток.
Полученные результаты сравнительного анализа динамики количественного содержания первичных, вторичных и конечных продуктов перекисного окисления липидов (ПОЛ) и системы антиоксидантной защиты (АОЗ) перитонеальной жидкости показали, что в раннем послеоперационном периоде на фоне исходного дисбаланса системы ПОЛ/АОЗ [7] наблюдается резкое возрастание уровней как первичных (диеновые конъюгаты), так и вторичных (малоновый диальдегид) молекулярных продуктов перекисного окисления липидов, а также молекул средней массы, в целом определяющих степень эндогенной интоксикации. Так, в 1-й группе уровень ДК вырос до 11,011,0±1,9 Ед/мл (4,1±0,5 Ед/мл исходно), во 2-й группе – до 7,5±0,9 (4,2±0,6 Ед/мл) исходно и до 5,9±1,1 Ед/мл (4,1±0,4 Ед/мл исходно). Уровень МДА (мкмоль/л) повысился до 13,9±2,1 в 1-й группе (7,8±1,1 исходно, до 9,9±1,0 (исходно 7,7±1,2) во 2-й группе и до 8,8±0,5 (исходно 7,8±1,0) у пациенток 3-й группы. Параллельно в первые сутки послеоперационного периода мы отметили в перитонеальной жидкости снижение активности СОД: в 1-й группе 2,3±0,7 против 5,3±1,0 исходно, во 2-й группе 3,0±0,7 против 5,6±1,0 исходно, и минимально 4,0±0,5 против 5,4±0,9 в 3-й группе. Соответственно во всех клинических группах определялось повышение соотношения МДА/СОД (у.е), характеризующее возрастание «окислительного потенциала» перитониальной жидкости. Данное соотношение возросло в 4,4 раза в 1-й группе, в 2,4 раза во 2-й группе и только в 1,3 раза в группе 3 (гемостатический материал) (табл. 1).
Таблица 1
Динамика показателей системы ПОЛ/АОС в перитонеальной жидкости в зависимости от метода эндохирургической коагуляции, M±m
|
Показатели |
ДК, Ед/ мл |
МДА, мкмоль/л |
СОД, ед/мг |
МДА/СОД, у.е |
МСМ, Е280,у.е ОП |
|
|
Биполярная коагуляция |
До операции |
4,1±0,5 |
7,8±1,1 |
5,3±1,0 |
1,5±0,9 |
0,38±0,09 |
|
1-е сутки |
11,0±1,9*^ |
13,9±2,1*^ |
2,3±0,7*^ |
6,6±2,4*^ |
0,8±0,1*^ |
|
|
Аргоноплазменная коагуляция |
До операции |
4,2±0,6 |
7,7±1,2 |
5,6±1,0 |
1,4±0,9 |
0,41±0,9 |
|
1-е сутки |
7,5±0,9*^ |
9,9±1,0*^ |
3,0±0,7*^ |
3,4±0,8*^ |
0,6±0,1*^ |
|
|
Применение гемостатического материала |
До операции |
4,1±0.4 |
7,8±1,0 |
5,4±0,9 |
1,65±0,9 |
0,38±0,9 |
|
1-е сутки |
5,9±1,1*^ |
8,8±0,5*^ |
4,0±0,5*^ |
2,2±1,7*^ |
0,4±0,1^ |
|
|
Группа контроля, n=35 |
0,65±1,1 |
3,6±0,8 |
7,5±0,6 |
0,5±0,02 |
0,03±0,02 |
|
где символ «*» соответствует статистически значимому различию показателей в послеоперационном периоде по сравнению со средними значениями аналогичных показателей до операции (р<0,005).
где символ «^» соответствует статистически значимому межгрупповому различию (р<0,005).
При анализе результатов динамики уровня цитокинов в перитонеальной жидкости выявлено возрастание провоспалительного потенциала, выражающееся в достоверном повышении концентрации IL 6 и TNF-α во всех клинических группах. При этом максимальный прирост как IL 6, так и TNF-α наблюдался в 1-й группе (при проведении биполярной коагуляции (65,8±4,3 против 28,6±5,3 исходно) и (9,5±0,9 против 7,1±1,6 исходно)), минимально – в 3-й группе (IL 45,7±4,9 против 28,4±3,9 исходно) (табл. 2)
Таблица 2
Динамика показателей цитокинового статуса перитонеальной жидкости в зависимости
от метода эндохирургической коагуляции, M±m
|
Показатели |
IL 10 пкг/мл |
IL 6 пкг/мл |
IL 2, пкг/мл |
TNF-α, пкг/мл |
|
|
Биполярная коагуляция, n=32 |
До операции |
10,2±1,4 |
28,6±5,3 |
6,5±2,1 |
7,1±1,6 |
|
1-е сутки |
10,1±1,9 |
65,8±4,3*^ |
7,2±0,9 |
9,5±0,9*^ |
|
|
Аргоноплазменная коагуляция, n=35 |
До операции |
9,9±0,9 |
27,9±4,6 |
6,5±1,6 |
7,0±1,8 |
|
1-е сутки |
11,16±1,4 |
56,5±6,8*^ |
7,52±0,9 |
9,2±0,7*^ |
|
|
Применение гемостатического материала, n=32 |
До операции |
10,3±0,8 |
28,4±3,9 |
6,6±1,6 |
7,1±0,7 |
|
1-е сутки |
12,3±2,04 |
45,7±4,9*^ |
7,3±0,9 |
9,05±0,7*^ |
|
|
Группа контроля, n=35 |
9,2±1,4 |
10,8±2,8 |
4,4±1,6 |
1,9±0,7 |
|
где символ «*» соответствует статистически значимому различию показателей в послеоперационном периоде по сравнению со средними значениями аналогичных показателей до операции (р<0,005).
где символ «^» соответствует статистически значимому межгрупповому различию (р<0,005).
Отставание противовоспалительного характеризовалось отсутствием динамики уровня IL10 и выражалось в достоверном возрастании провоспалительного индекса во всех клинических группах (р<0,005): в 1-й группе в 3 раза, во 2-й в 1,8 раза и в 3-й в 1,5 раза (рис. 1).
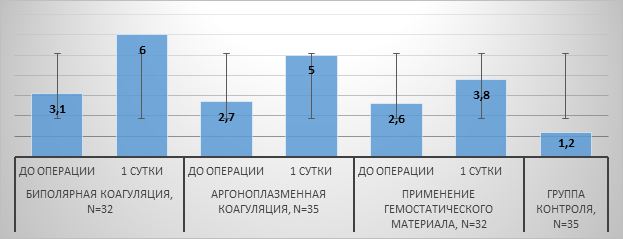
Рис. 1. Динамика ПВИ (IL6/IL10) перитонеальной жидкости в зависимости
от метода эндохирургической коагуляции, M±m
Полученные результаты показали тесную взаимосвязь процессов перекисного окисления липидов и системы антиоксидантной защиты с цитокиновым профилем в перитонеальной жидкости больных с ЭКЯ, поскольку все реакции иммунитета в той или иной степени кислородозависимы. Это подтверждается статистически значимыми сильными положительными корреляционными взаимосвязями между процентами повышения IL6, TNF-α и процентом прироста коэффициента МДА/СОД во всех клинических группах. Коэффициент корреляции составил для IL6 и МДА: r=0,82 – в 1-й группе, r=0,89 – во 2-й группа и r=0,78 – в 3-й группе и для TNF-α (р <0,005): r=0,87 – в 1-й группе , r=0,82 – во 2-й группе и r=0,81 – в 3-й группе.
Исследование овариального резерва, определяемого в нашем исследовании по уровню АМГ (негормонозависимый показатель), показало, что антимюллеров гормон Г в сыворотке крови значительно снизился после операции во всех группах независимо от того, какой метод гемостаза был применен, и через три месяца ни в одной из клинических групп не вернулся к дооперационным значениям. При средних дооперационных параметрах, составляющих 4,7±2,9 нг/мг у всей когорты обследуемых, через месяц после операции он составил 1,8±0,9 нг/мг в 1-й группе, 2,44±0,6 нг/мл во 2-й группе и 2,97±1,1 нг/мл в 3-й группе, р<0,005 по всем группам. Максимально уровень АМГ снизился при применении во время цистэктомии коагуляции биполярным электродом. При применении гемостатического материала снижение уровня АМГ было минимальным. К третьему месяцу послеоперационного периода при условии выполнения аргоноплазменной коагуляции и применения гемостатического материала уровень АМГ прирастал до 2,8±0,9 нг/мг во 2-й группе и до 2,97±1,1 нг/мл в 3-й группе. При условии выполнения биполярной коагуляции параметры овариального резерва, определяемые по АМГ, продолжали снижение до 1,4±0,6 нг/мг (рис. 2).
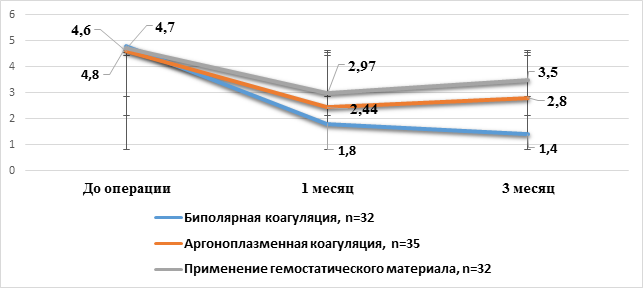
Рис. 2. Сравнительная характеристика динамики овариального резерва в послеоперационном периоде пациенток с ЭКЯ в зависимости от метода эндохирургического гемостаза, M±m
С целью выяснения возможной взаимосвязи между снижением АМГ у пациенток позднего репродуктивного возраста после энуклеации кисты и параметрами ПОЛ/АОС перитонеальной жидкости в раннем послеоперационном периоде мы провели корреляционный анализ взаимоотношений процента снижения АМГ к 3-му месяцу послеоперационного периода и коэффициентом МДА/СОД. Процент снижения АМГ через 3 месяца после операции во всех клинических группах при прямой взаимосвязи сильно коррелировал с коэффициентом МДА/СОД (r=0,89 – 1-я группа, r =0,91 – 2-я группа и r=0,88 – 3-я группа). Коэффициент корреляции между ПВИ перитонеальной жидкости и процентом снижения АМГ также указывал на сильную прямую связь (r=0,86 – 1-я группа, r=0,81 – 2-я группа и r=0,84 – 3-я группа).
Заключение
Таким образом, в данном исследовании показано, что при энуклеации эндометриоидной кисты яичника усугубляется местный дисбаланс в системе цитокинов и ПОЛ/АОЗ, что может играть определяющую роль в глубоком снижении овариального резерва яичников у пациенток позднего репродуктивного возраста. При энергозависимом интраоперационном гемостазе на фоне регуляторной дисфункции, определяемой инертностью выработки IL2, на местном уровне нарушается сбалансированность функционального состояния межклеточных иммуномодуляторов IL6, TNFα их антагониста ИЛ-10, что ведет к усилению проапоптических влияний и замедлению регенеративно-восстановительных реакций. В результате усугубления дисбаланса в системе цитокинов и ПОЛ/АОЗ развиваются глубокие патофизиологические сдвиги, следствием которых становятся накопление токсических метаболитов, ишемический некробиоз в периоперационной зоне и нарушение тканевого ремоделирования. Данный процесс наиболее выражен при применении коагуляции биполярным электродом. Наименьшие сдвиги отмечены у пациенток позднего репродуктивного возраста после цистэктомии в системах ПОЛ/АОЗ и цитокиновом балансе и как следствие в снижении овариального резерва наблюдаются при щадящем методе применения интраоперационных гемостатиков в виде рассасывающегося гемостатического материала, изготовленного по методу контролируемого окисления восстановленной целлюлозы.
Библиографическая ссылка
Соколова Е.И., Куценко И.И., Кравцова Е.И., Томина О.В. ВЛИЯНИЕ РАЗЛИЧНЫХ МЕТОДОВ ЭНДОХИРУРГИЧЕСКОГО ГЕМОСТАЗА НА ОВАРИАЛЬНЫЙ РЕЗЕРВ ПРИ ЭНУКЛЕАЦИИ ЭНДОМЕТРИОИДНЫХ КИСТ У ПАЦИЕНТОК ПОЗДНЕГО РЕПРОДУКТИВНОГО ВОЗРАСТА // Современные проблемы науки и образования. 2018. № 5. ;URL: https://science-education.ru/en/article/view?id=28182 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.28182



