Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE POSSIBILITY OF NON-PHARMACOLOGICAL CORRECTION OF VITAMIN D DEFICIENCY FOR THE PREVENTION OF DISORDERS OF BONE METABOLISM IN CHILDREN WITH ARTICULAR FORM OF JUVENILE IDIOPATHIC ARTHRITIS
Ювенильный идиопатический артрит (ЮИА) по определению Международной лиги ревматологических ассоциаций (ILAR) – артрит неизвестной этиологии, начинающийся в возрасте до достижения 16 лет и длящийся более 6 недель, при условии исключения другой патологии суставов [1]. ЮИА отнесен, по данным Всемирной организации здравоохранения (ВОЗ), к наиболее актуальным проблемам педиатрии и ревматологии.
Частота распространения ЮИА в мире достигает 19,8 случая на 100 000 населения в возрасте до 16 лет при ежегодной регистрации до 3,2 нового случая заболевания на 100 000 детей [2]. По данным А.А. Баранова с соавторами, распространенность ЮИА в России среди детей до 18 лет достигает 62,3 случая на 100 000 детского населения, при этом первичная заболеваемость составляет 16,2 на 100 000 [3; 4].
Современный период изучения различных патогенетических звеньев течения ЮИА характеризуется особым вниманием к формированию изменений в костной ткани. Нарушения со стороны костной ткани, обусловленные снижением минеральной плотности костной ткани (МПКТ), могут быть зарегистрированы как при первых признаках артрита, так и на более поздних стадиях заболевания.
Своевременно не диагностированные и не подвергшиеся коррекции метаболические нарушения в костной ткани ведут не только к формированию необратимых изменений скелета [5], но у детей с ЮИА еще и становятся одной из причин стойкой инвалидизации. Поэтому профилактика нарушений костного метаболизма и коррекция сниженной МПКТ, еще до клинических проявлений остеопении, важна для улучшения качества жизни пациентов с ЮИА.
Цель исследования. Оценить возможность немедикаментозной коррекции дефицита витамина D для профилактики нарушений костного метаболизма у детей с суставной формой ЮИА.
Материалы и методы исследования. В исследование были включены 32 пациента с суставной формой ЮИА и 28 детей с другими артритами. Возраст детей, принявших участие в исследовании - от 2 до 10 лет. У всех детей, по результатам предварительного лабораторного исследования, были выявлены дефицит/недостаточность уровня 25(ОН)D в сыворотке крови (до 20 нг/мл) и снижение уровня костной прочности по результатам оценки интегрального показателя Z-score, полученного при проведении ультразвуковой остеоденситометрии (аппарат «Omnisense 7000») и характеризующего стандартное отклонение от нормы по возрасту, полу и весу скорости прохождения ультразвуковой волны через кость (в исследование включались дети с отклонениями Z-score от -1,5 до - 2,5 SD). Отобранных участников исследования разделили на три подгруппы так, чтобы они были максимально однородны по полу, возрасту и количеству пациентов с ЮИА: подгруппа «А» – дети получали рациональное питание и специализированный продукт для энтерального питания, содержащий 52 МЕ витамина D3 в 100 мл (немедикаментозная коррекция дефицита/недостаточности витамина D) (n=20); подгруппа «Б» – дети получали только рациональное питание (n=20); подгруппа «В» – дети находились на медикаментозной коррекции дефицита/недостаточности витамина D официнальными таблетированными препаратами, содержащими 200 МЕ холекальциферола и 1,25 мг кальция карбоната в 1 таблетке (медикаментозная коррекция) (n=20).
До начала назначения продукта для энтерального питания все дети были протестированы с помощью метода ретроспективного воспроизведения питания. Применили суррогатный опрос и анкетирование (на вопросы отвечали родители ребенка) по методике анализа частоты потребления пищи [6]. До заполнения анкеты с родителями детей была проведена разъяснительная беседа о порядке ее заполнения. При анализе анкет была установлена частота потребления за неделю продуктов, вносящих существенный вклад в получение организмом ребенка необходимых для нормального костного метаболизма элементов: кальция, фосфора, магния, марганца, цинка и витамина D.
Для доказательства возможности применения продуктов для энтерального питания с целью профилактики остеопении, развивающейся на фоне витамин D-дефицитных состояний, у детей с суставной формой ЮИА был выбран специализированный диетический продукт для оптимизации питания детей - медицинская детская смесь Педиашур 1.0 (PediaShure), применяемая не только для полной замены питания, но и как дополнительное питание к основному рациону у детей от 1 года до 10 лет. Продукт выпускается в удобной упаковке, что позволяет применять его как в домашних условиях, так и в школе, на прогулке.
Пищевая ценность сбалансированного по белкам, жирам и углеводам продукта составляет 101 Ккал/100 мл, при этом в нем содержится полный комплекс необходимых для организма ребенка макро- и микроэлементов (кальций, фосфор, цинк, селен, железо и другие) и витаминов, включая витамин D3 в количестве 52 МЕ/100 г. Рекомендуемая схема применения этого продукта 2 раза в день по 1 флакону (200 мл) в дополнение к основному рациону питания.
Согласно полученным данным, суточное потребление указанных элементов и витамина D было снижено у 85% респондентов. Только 4 ребенка (10%), согласно проведённому опросу, могли быть отнесены к группе с достаточным потреблением витамина D. Это были дети до пяти лет, в рационе которых с достаточной частотой были представлены молоко и молочные продукты.
Родителям детей из подгрупп «А» и «Б» было предложено примерное меню на неделю, включающее максимальный набор продуктов, вносящих существенный вклад в потребление кальция, фосфора и витамина D с учетом возраста обследуемых пациентов. В период проведения исследования (4 недели) дети из подгрупп «А» и «Б» не принимали медикаментозных препаратов витамина D3.
Родителям детей из подгруппы «А» был выдан 4-недельный набор специализированного продукта для энтерального питания из расчета 2 флакона продукта в сутки, содержание холекальциферола в которых составляло 208 МЕ.
Родители детей из подгруппы «В» на период проведения исследования получили таблетированный препарат витамина D из расчета 1 таблетка в сутки для детей от 2 до 5 лет и 2 таблетки в сутки для пациентов старше 5 лет, что соответствовало 200-400 МЕ холекальциферола в сутки.
До начала исследования и по его завершении у всех детей было проведено определение уровня 25(ОН)D в сыворотке крови.
Характеристика детей, вошедших в исследование, представлена в таблице 1.
Таблица 1
Характеристика детей, вошедших в исследование
|
Показатель |
Подгруппы |
|||
|
А (n=20) |
Б (n=20) |
В (n=20) |
||
|
Мальчики |
9 (45 %) |
9 (45 %) |
13 (65 %) |
|
|
Девочки |
11 (55 %) |
11 (55 %) |
8 (40 %) |
|
|
Возраст |
М±m |
6,6±2,54 |
6,8±1,94 |
7,2+1,97 |
|
До 3 лет |
3 (15 %) |
0 |
0 |
|
|
Старше 3 лет |
17 (85 %) |
20 (100 %) |
20 (100 %) |
|
|
Концентрация 25(ОН)D нг/мл (М±m) исходная |
16,25±5,28 |
19,45+5,16 |
16,37+6,12 |
|
Обеспеченность детей витамином D после проведенной коррекции оценивали согласно рекомендациям Международного общества эндокринологов: дефицит – уровень 25(ОН)D <20 нг/мл; недостаточность – 21–29 нг/мл; нормальное содержание – 30–100 нг/мл [7].
Результаты исследования и их обсуждение. Согласно полученным данным в подгруппе «А» все дети до проведения коррекции находились в зоне дефицита (75%) или недостаточности (25%). После коррекции доля детей, имеющих уровень 25(ОН)D ниже 30 нг/мл, не превышала 30%, причем показатели 25(ОН)D на уровне дефицита (менее 20 нг/мл) не были зарегистрированы ни у одного ребенка.
Если до начала коррекции среди детей из подгруппы «А» с олигоартикулярным вариантом (ОАВ) ЮИА у всех пациентов регистрировали дефицит витамина D (ниже 20 нг/мл), то после коррекции более 62% обследованных достигали уровня 25(ОН)D в сыворотке крови более 30 нг/мл, а у оставшихся детей удалось перевести состояние дефицита витамина D в недостаточность. При полиартикулярном варианте (ПАВ) ЮИА удалось у всех детей с недостаточностью витамина D добиться повышения его уровня в сыворотке крови свыше 30 нг/мл, а у 50% детей с дефицитом витамина D увеличить его уровень в сыворотке крови до 21-29 нг/мл. Применение немедикаментозной коррекции дефицита витамина D у детей с другими артритами в анамнезе позволило более чем у 80% пациентов добиться нормальных значений 25(ОН)D в сыворотке крови (более 30 нг/мл).
В подгруппе «Б» 95% детей на момент начала исследования имели уровень 25(ОН)D в сыворотке крови ниже 30 нг/мл, лишь у 1 ребенка уровень витамина D находился в зоне дефицита. Через 4 недели наблюдения за пациентами этой подгруппы имело место незначительное улучшение показателей 25(ОН)D в сыворотке крови, а доля детей, преодолевших порог в 30 нг/мл, увеличилась до 10%.
В подгруппе «Б» через 4 недели наблюдения отмечали снижение доли пациентов с дефицитом витамина D (ниже 10 нг/мл): среди детей с ОАВ и ПАВ течения ЮИА на 50% и 10% соответственно. Среди детей с другими артритами в анамнезе удалось добиться двукратного увеличения доли пациентов с уровнем 25(ОН)D в сыворотке крови более 30 нг/мл.
В подгруппе «В» 90% детей на момент начала исследования имели дефицит витамина D (уровень 25(ОН)D в сыворотке крови ниже 20 нг/мл), лишь у 2 пациентов уровень витамина D находился в зоне недостаточности (21-29 нг/мл). Через 4 недели медикаментозной коррекции у пациентов этой подгруппы имело место значительное улучшение показателей 25(ОН)D в сыворотке крови, а доля детей, преодолевших порог в 30 нг/мл, составила 85%.
В подгруппе «В» через 4 недели медикаментозной коррекции у всех пациентов с ПАВ течения ЮИА, у 90% детей с ОАВ течения ЮИА и в 87,5% случаев у детей с другими артритами в анамнезе отмечали положительный результат – достижение концентрации 25(ОН)D в сыворотке крови уровня выше 30 нг/мл.
На рисунке продемонстрирована структура обеспеченности витамином D детей в подгруппах «А», «Б» и «В» до и после проведения исследования.
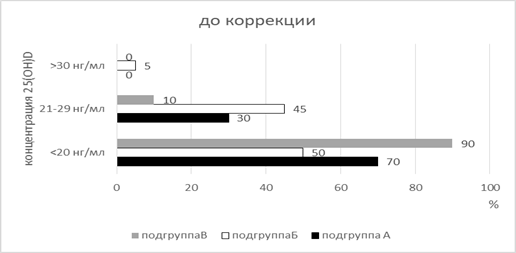
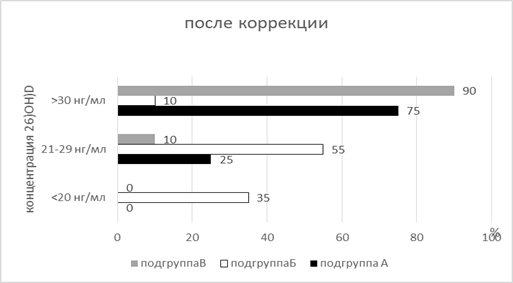
Структура обеспеченности витамином D детей в подгруппах «А», «Б» и «В» до и после проведения исследования
Как видно из рисунка, в подгруппе «Б» по окончании наблюдения имело место перераспределение детей по уровню 25(ОН)D. Так, 15% пациентов этой подгруппы смогли увеличить уровень витамина D в сыворотке крови до 21-29 нг/мл только за счет питания, обогащенного продуктами, богатыми витамином D, и лишь у 5% детей удалось корректировать недостаточность 25(ОН)D до уровня нормы. В подгруппах «А» и «В» прослеживалась четкая тенденция к увеличению концентрации 25(ОН)D в сыворотке крови пациентов, получающих как специализированный продукт для энтерального питания, так и таблетированный препарат витамина D3, до уровня более 30 нг/мл в 75% и 90% случаев соответственно.
В таблице 2 представлены данные по содержанию 25(ОН)D в сыворотке крови обследованных детей из подгрупп «А», «Б» и «В» до и после исследования.
Таблица 2
Содержание 25(ОН) D в сыворотке крови детей подгрупп «А», «Б» и «В» до и после исследования
|
Подгруппа |
Вариант течения суставной формы ЮИА |
До коррекции (M+m) |
После коррекции (M+m) |
р |
|
А |
Олигоартикулярный |
12,94+3,5 |
31,33+7,60 |
<0,05 |
|
Полиартикулярный |
16,87+5,74 |
37,6+9,64 |
<0,05 |
|
|
Артрит в анамнезе |
20,06+4,50 |
34,28+5,15 |
<0,05 |
|
|
Для всей группы |
16,26+5,28 |
34,11+7,74 |
<0,05 |
|
|
Б |
Олигоартикулярный |
18,73+3,86 |
21,86+2,65 |
>0,05 |
|
Полиартикулярный |
17,8+5,26 |
21,30+7,01 |
>0,05 |
|
|
Артрит в анамнезе |
22,03+6,36 |
25,13+6,51 |
>0,05 |
|
|
Для всей группы |
19,45+5,16 |
22,68+6,11 |
>0,05 |
|
|
В |
Олигоартикулярный |
14,71+2,89 |
32,69+6,87 |
<0,05 |
|
Полиартикулярный |
17,45+1,64 |
31,85+5,74 |
<0,05 |
|
|
Артрит в анамнезе |
17,47+3,93 |
36,07+7,12 |
<0,05 |
|
|
Для всей группы |
16,37+6,12 |
34,30+6,98 |
<0,05 |
Выводы. Таким образом, увеличение в подгруппах «А» и «В» после 4-недельного курса как немедикаментозной, так и медикаментозной коррекции дефицита 25(ОН)D в сыворотке крови доли детей с нормальной обеспеченностью витамином D с 0 до 75% и 90% случаев соответственно свидетельствует об эффективности примененных методов, а отсутствие достоверного отличия в достигнутом уровне 25(ОН)D в сыворотке крови у пациентов этих подгрупп подтверждает возможность применения немедикаментозной коррекции дефицита витамина D для профилактики остеопении, основанной на использовании специализированных продуктов для энтерального питания.
Применение немедикаментозных методов коррекции дефицита витамина D на амбулаторном этапе ведения больных с ЮИА с целью профилактики развития у них нарушений костного метаболизма позволяет, кроме того, снизить психоэмоциональное напряжение пациентов, обусловленное необходимостью соблюдения комплаенса приема медикаментозных препаратов витамина D3.
Библиографическая ссылка
Спиваковская А.Ю., Черненков Ю.В., Спиваковский Ю.М. ВОЗМОЖНОСТИ НЕМЕДИКАМЕНТОЗНОЙ КОРРЕКЦИИ ДЕФИЦИТА ВИТАМИНА D ДЛЯ ПРОФИЛАКТИКИ НАРУШЕНИЙ КОСТНОГО МЕТАБОЛИЗМА У ДЕТЕЙ С СУСТАВНОЙ ФОРМОЙ ЮВЕНИЛЬНОГО ИДИОПАТИЧЕСКОГО АРТРИТА // Современные проблемы науки и образования. 2017. № 6. ;URL: https://science-education.ru/en/article/view?id=27166 (дата обращения: 16.05.2026).



