Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
STUDY CYTOSTATIC EFFECT OF COMPLEX APOLIPOPROTEIN A-I WITH VINBLASTINE
Создание новых лекарственных форм противоопухолевых препаратов – задача современная и актуальная. В последние два десятилетия сформировался новый взгляд на липопротеины (ЛП) плазмы крови и их белковые компоненты как на естественные нанопереносчики лекарственных препаратов [6,10]. Показано, что использование липопротеинов высокой плотности в комплексе с даунорубицином приводило к увеличению эффективности транспорта и цитостатического действия препарата в отношении клеток НА-1 гепатомы мышей [5]. В литературе представлены работы, в которых показана возможность использования основного белкового компонента аполипопротеина А-I в качестве транспортной формы лекарственных препаратов [8]. Ранее нами была показана способность аполипоаротеина А-I образовывать устойчивые комплексы с противоопухолевыми препаратами актиномицином Д и винбластином и проникать в цитоплазму и ядра клеток асцитной карциномы Эрлиха [2].
Целью настоящей работы явилось изучение эффективности цитостатического действия аполипопротеина А-I в комплексе с винбластином на модели асцитной карциномы Эрлиха.
МЕТОДИКА. Выделение липопротеинов из плазмы крови человека проводили методом изоплотностного ультрацентрифугирования в растворах KBr в присутствии 3 мМ ЭДТА-Na2 на центрифуге «Optima L-90K, Beckman-Coulter» (Австрия) с использованием ротора 70.1 Ti [4]. Получали три основные фракции липопротеинов: липопротеины очень низкой плотности (ЛПОНП, 0,94
Аполипопротеин А-I выделяли из фракции ЛПВП. Делипидирование проводили охлажденной смесью хлороформ-метанол (1:1) из расчета 20 мл смеси на 1 мл ЛПВП с последующей многократной отмывкой эфиром. Для получения апоА-I (апоА-I) суммарные белки ЛПВП в растворе 3% Ds-Na и 0,1% меркаптоэтанола наносили на колонку (1,6 х 100 см) с Сефарозой 6В-CL («Pharmacia», Швеция) и элюировали 5мМ Трис-НСl буфером, рН 8,6, содержащим 6 М мочевину, 0,01% азид натрия и 1 мМ фенилметансульфонилфторид. Проверка чистоты апоА-I осуществлялась с помощью электрофореза в 10% ПААГ с Ds-Na. Белковые полосы визуализировали 0,1% Кумасси G-250 в смеси метанола и 10% уксусной кислоты (1:1) [4].
Обессоливание апоА-I проводили методом гель-фильтрации (колонка: 40 ´ 0,8 см, Сефадекс G-25 («Pharmacia», Швеция), элюент: 5мМ трис-НСl буфер, рН 7,4, содержащий 0,15 М NaCl. Профиль элюции регистрировали на УФ-детекторе при длине волны 280 нм. Концентрация обессоленного белка составляла 0,2 мг/мл.
В работе использовали 1 мМ маточный раствор винбластина (ЛЭНС, ФАРМ, Россия).
Пролиферативную активность клеток оценивали по скорости включения 3Н-тимидина («Amersham», Англия) в ДНК. Последний добавляли в среду инкубации в дозе 2 мкКи/мл за 2 часа до окончания эксперимента. Реакцию останавливали добавлением 0,2н раствора NaOH. Для измерения радиоактивности содержимое лунки переносили на целлюлозные фильтры «Whatman 3 MM» (Англия), которые последовательно промывали от несвязавшейся метки раствором 10% трихлоруксусной кислоты и смесью этанол-эфир (1:1). Радиоактивность измеряли на сцинтилляционном счётчике «Mark-III»(США) и выражали в имп/мин на 1 мг белка [7]. Содержание белка в образцах определяли по методу Варбурга и Христиана [1].
Эксперименты проводили на клетках асцитной карциномы Эрлиха. Выделение клеток из перитонеального экссудата проводили на 10 день после перевивания. Под легким эфирным наркозом мышей забивали с помощью дислокации шейных позвонков, вскрывали брюшную полость в нижнем латеральном отделе. Собирали перитонеальный экссудат и вносили в центрифужные пробирки. Центрифугировали в течение 10 мин при 150g для осаждения клеточных элементов. Осадок клеток трижды промывали большими объемами холодного раствора Рингера-Кребса. Подсчет клеток проводили в камере Горяева. Жизнеспособность клеток оценивали по исключению трипанового синего [3].
Комплекс аполипопротеина А-I с винбластином (апоА-I–винбластин) получали, выдерживая их смесь в молярном соотношении 1:1 в 0,05 М калий-фосфатном буфере, рН 7,4, содержащим 0,15 М NaCl, в течение 15 мин при комнатной температуре. Комплекс апоА-I–винбластин добавляли к культуре клеток асцитной карциномы Эрлиха и инкубировали в течении 5 часов. Концентрация апоА-I в среде инкубации составляла от 20 мкг/мл до 5 мкг/мл, винбластина от 1 мкг/мл до 0,1мкг/мл.
В качестве контроля использовали клетки карциномы, которым в среду инкубации добавляли физиологический раствор.
Статистическую обработку данных проводили при помощи программы StatPlus 2009 Professional 5.8.4., (США). Статистическую значимость полученных результатов оценивали с помощью t-критерия Стьюдента при уровне значимости p<0,05.
Результаты и обсуждение
Из литературы известно, что винбластин (Vinblastine) – алкалоид, содержащийся в растении барвинок розовый (Vinca rosea L.), а также в растении катарантус розовый (Catharanthus roseus L.). Механизм противоопухолевого действия объясняют способностью связываться с молекулами тубулина, торможением образования митозного веретена, и блокированием тем самым деление клетки, т. е. блокирование митоза на стадии метафазы. Рабочие концентрации препарата в экспериментах in vitro составляют в диапазоне от 10 мкг/мл до 0,1 мкг/мл [9]. Мы проводили оценку цитостатического действия в течении пяти часов инкубации. Предварительные эксперименты показали, что антипролиферативный эффект для винбластина без переносчика на модели асцитной карциномы Эрлиха был отмечен при концентрации 1мкг/мл уже через пять часов инкубации. Показано, что добавление в питательную среду аполипопротеина А-I в комплексе с винбластином в той же концентрации (1мкг/мл) так же снижало скорость биосинтеза ДНК рис.1.
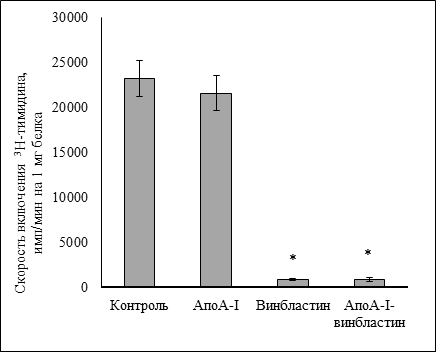
Рис.1. Изменение скорости биосинтеза ДНК в клетках асцитной карциномы Эрлиха. Концентрация винбластина 1 мкг/мл
* - достоверное различие по сравнению с контролем (р < 0,001).
Снижение концентрации цитостатика до 0,1 мкг/мл показало, что в присутствии комплекса аполипопротеина А-I с винбластином скорость биосинтеза ДНК снижалась на 41% . Инкубация при добавлении винбластина без переносчика оставляла значения на уровне контрольных рис.2.
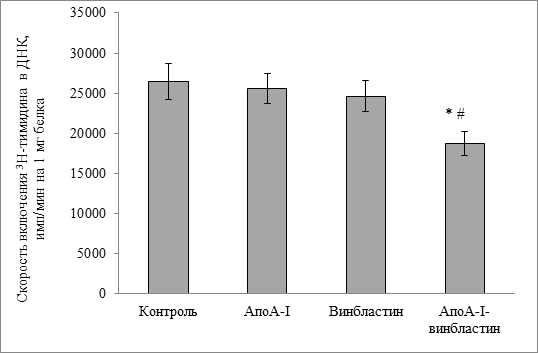
Рис.2. Изменение скорости биосинтеза ДНК в клетках асцитной карциномы Эрлиха. Концентрация винбластина 0,1 мкг/мл.
* - достоверное различие по сравнению с контролем (р < 0,001)
# - достоверное различие по сравнению с группой винбластин (р < 0,05).
Похожий эффект был получен при использовании концентрации винбластина 0,05 мкг/мл риc. 3. Снижение скорости биосинтеза ДНК при добавлении комплекса составило 23 % по сравнению с контролем. Добавление в среду инкубации винбластина без аполипопротеина А-I оставляло значения на уровне контрольных.
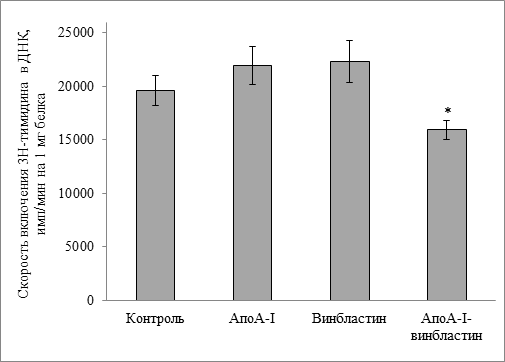
Рис.3. Изменение скорости биосинтеза ДНК в клетках асцитной карциномы Эрлиха. Концентрация винбластина 0,05 мкг/мл.
* - достоверное различие по сравнению с контролем (р < 0,05)
Дальнейшее уменьшение концентрации цитостатика не выявило влияния комплекса аполипопротеина А-I с винбластином на пролиферацию опухолевых клеток. Таким образом, была определена наименьшая концентрация комплекса, при которой был обнаружен цитостатический эффект.
Полученные результаты позволяют сделать вывод об эффективности цитостатического действия комплекса аполипопротеина А-I с винбластином на модели асцитной карциномы Эрлиха в экспериментах in vitro, поскольку комплекс снижает биосинтез ДНК в опухолевых клетках карциномы при использовании концентраций цитостатика, при которых препарат без переносчика не оказывает влияния на пролиферацию опухолевых клеток.
Библиографическая ссылка
Князев Р.А., Трифонова Н.В., Поляков Л.М. ИЗУЧЕНИЕ ЭФФЕКТИВНОСТИ ЦИТОСТАТИЧЕСКОГО ДЕЙСТВИЯ КОМПЛЕКСА АПОЛИПОПРОТЕИНА A-I С ВИНБЛАСТИНОМ // Современные проблемы науки и образования. 2015. № 6. ;URL: https://science-education.ru/en/article/view?id=23832 (дата обращения: 19.05.2026).



