На долю соединительной ткани приходится более 50 % массы тела животного. Существенной особенностью, отличающей ее от других и присущей в большей или меньшей степени всем ее разновидностям, является количественное преобладание межклеточного вещества над клеточными элементами. Межклеточный матрикс состоит из волокнистых компонентов, а пространство между ними заполнено основным веществом, содержащим гликопротеины. Волокнистые компоненты состоят из коллагеновых и эластиновых волокон.
Белковый состав соединительной ткани представлен в основном коллагеном и эластином, на их долю приходится практически 90 % всех белков. Это фибриллярные белки с характерной удлиненной формой молекулы, обусловленной параллельным расположением полипептидных цепей. Аминокислотный состав коллагена и эластина отличается от мышечных. В коллагене на долю остатков глицина и аланина приходится около 45 %, также содержатся такие аминокислоты: гидроксилизин и гидроксипролин. На долю пролина и гидроксипролина приходится около 21 %. В эластине суммарное содержание глицина, аланина, валина и пролина составляет почти 70 %. Изоэлектрическая точка смещена в слабокислую область [4]. Еще одной характерной чертой является регулярность в последовательности аминокислот, чего нельзя сказать о белках мышечной ткани. Для данных белков характерно присутствие повторяющихся участков аминокислот. В коллагене - в виде триплетов четырех видов (Х – иминокислота, Y – аминокислота):
- Gly - Х - Х -; - Gly - Х - Y -; - Gly - Y - Х -; - Gly - Y - Y -.
В эластине - тетрамер: - Gly - Gly- Val - Pro -; пентамер: - Pro - Gly - Val - Gly - Val -; гесамер: - Pro - Gly - Val - Gly - Val - Ala.
Для соединительнотканных белков характерно присутствие внутри- и межмолекулярных поперечных сшивок: альдольная, гистидин-альдольная, лейцин-норлейциновая, основание шиффа. В результате появляется возможность ковалентного связывания четырех боковых цепей друг с другом, причем они могут принадлежать разным молекулам белка.
В эластине значительно меньше содержание лизина это обусловлено тем, что боковые цепи четырех остатков аминокислоты ферментативным путем превращаются в десмозин, в результате формируется поперечная сшивка между соседними полипептидными цепями в молекуле эластина. Именно присутствие десмозина отличает эластин от всех других белков, включая и коллаген.
Благодаря своей уникальной структуре белки соединительной ткани в нативном состоянии не подвергаются действию протеолитических ферментов. Ткани, содержащие коллаген и эластин, отличаются особой прочностью, способностью выдерживать значительные нагрузки.
При всем сходстве данных белков, каждый из них является индивидуальным белком, со свойствами присущими только ему одному.
Молекула коллагена имеет относительную молекулярную массу 300000, длину 280 нм и толщину 1,4 нм. Каждая a-цепь содержит в среднем около 1000 аминокислотных остатков. Еще одной особенностью коллагена является его гетерогенность. В настоящее время описано 28 типов коллагена, которые кодируются более чем 40 генами. Они отличаются друг от друга по аминокислотной последовательности, а также по степени модификации – интенсивности гидроксилирования или гликозилирования. Общим для всех коллагенов является существование одного или более доменов, содержащих тройную спираль и присутствие их во внеклеточном матриксе [5].
Эластин изучен меньше, чем коллаген. Наличие гибкой случайной конформации молекул эластина и большое количество поперечных сшивок обеспечивает исключительное свойство эластической ткани - обратимую деформацию под влиянием механического воздействия.
Практическое применение имеет в основном коллагенсодержащее сырье, это связано со способностью коллагена образовывать гели при взаимодействии с водой. Коллаген находит широкое применение в медицине для пластики сосудов, дефектов кожи, кости, мозговой оболочки, тазового дна, трахеи, печени и селезенки. Применяется в виде гемостатических средств и тампонов, мембран для диализа, шовного материала, а также для доставки лекарственных средств в организм человека, в пищевой промышленности – в качестве гелеобразователя.
Цель работы исследование возможности использования соединительнотканных белков в качестве носителей биологически активных веществ.
Материалы и методы исследований
Объектами исследования были сухожилия и выйная связка крупного рогатого скота, желатин, растворы гидролизатов коллагена и эластина, соли йода и железа, а также растительные настои, содержащие фенольные соединения, в частности антоцианы.
Основные этапы получения гидролизата коллагена: измельчение сухожилий, последовательная солевая и кислотная экстракция, тепловая обработка и охлаждение. Раствор гидролизата коллагена имел светло-матовый цвет, без видимых границ раздела фаз.
Эластин выделяли из выйной связки при последовательной экстракции: солевой, щелочной, водной. Растворимую форму белка получали методом биотрансформации.
Гидролизат представляет собой сложную смесь пептидов, жидкость светло-желтого цвета, без вкуса и запаха. Содержание белка в 1 мл гидролизата коллагена и эластина составило 30 мг и 40 мг соответственно.
При проведении экспериментов использовали аналитические методы качественного и количественного анализа.
Результаты исследований и их обсуждение
В результате проведенных исследований получены растворимые формы соединительнотканных белков – гидролизаты коллагена и эластина, которые исследовали в качестве матрицы микроэлементов, в частности железа и йода.
Источниками микроэлементов служили сульфат железа (II) и йодид калия. Одним из основных условий при проведении реакции являлся показатель рН среды. Выбор рН среды связан со свойствами микроэлементов и фермента. Так, в кислой среде йод восстанавливается до молекулярного состояния и улетучивается, в щелочной среде рН > 8,0 образуется гипойодид. Фермент при рН выше 6,0 инактивируется. Учитывая данные факторы, в растворах устанавливали рН 7,0 – 7,2. Расчет вводимого количества йодида калия производили по содержанию йода (76,5%).
При взаимодействии железа и гидролизатов коллагена и эластина были исследованы значения рН (9,0; 5,5; 3,5)±0,2. При рН 9,0±0,2 наблюдалось изменение окраски от светло-желтого (гидролизат эластина) и светло-матового (гидролизат коллагена) до темно-коричневого цвета с выпадением осадка в виде хлопьев, что снижало органолептические свойства и указывало на окисление железа.
При рН среды 3,5 и 5,5 наблюдалось одинаковое связывание железа без визуальных изменений растворов. Однако, учитывая значения рН максимальной устойчивости комплексов и большинства пищевых систем, выбрано значение 5,5±0,2.
Оптимальная температура процессов связывания йода и железа соединительнотканными белками выбрана 0-4 °С, так как при положительных температурах возможно микробное обсеменение исследуемых растворов.
Известно, что химические процессы протекают во времени. Для установления максимальной степени связывания в растворы гидролизатов эластина и коллагена вносили разные концентрации солей железа и йода и контролировали содержание микроэлементов через каждые 2 часа. Концентрации микроэлементов были подобраны исходя из суточной потребности организма человека в них [3]. Экспериментально установлено, что максимальное взаимодействие железа с гидролизатами наблюдалось по истечении 24 часов, в случае йода – 20 часов.
По результатам исследований учитывая совокупность данных по ИК - спектроскопии (о наличии полиглициновых структур и отсутствие связи C-I), содержанию глицина в гидролизатах, диссоциацию йодида калия в растворах на ионы, избирательное расщепление пептидной цепи пепсином (Х- глицин) можно предположить о возможности возникновения ионной связи между протонированными группами NH3+ гидролизатов и I-. На основании приведенных доводов, предложена гипотетическая модель связывания йода гидролизатами соединительнотканных белков:
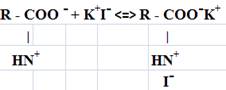
Для выяснения взаимодействия катиона железа с пептидами эластина и коллагена проведены исследования с использованием методов ИК и ЯМР-спектроскопии.
При ИК-спектроскопии в области 1400-1390 см-1 у образцов гидролизата эластина присутствует пик, который отвечает за группировку COO- . Данная область не содержит аналогичный пик в спектре в образцах эластин-железо. Следовательно, можно предположить, что свободная карбоксильная группа, присутствующая в пептидах гидролизата эластина, присоединила к себе железо с образованием комплекса. В диапазоне спектра 1130-1080 см-1 в образцах «эластин-железо» и «коллаген - железо» наблюдалось появление пиков, отвечающих за сульфатную группировку и свидетельствующих о возникновении ионной связи с SO42-.
Для более полной информации о взаимодействии между соедительнотканными белками и железом исследовали ядерно-магнитно-резонансные (ЯМР) спектры опытных образцов.
Анализ спектров показал, что в гидролизатах содержится большее количество СОО- групп (области 160-180 м.д., наличие большего количества пиков), в отличие от той же области в гидролизатах с железом. В области 50-65 м.д., которая отвечает за >СН-N<, не появилось новых пиков, но сдвиги в этой области также присутствовали.
Учитывая координационное число Fe+2 равно 4, возможно образование димера в результате связывания железа с двумя атомами кислорода и азота. Полученный комплекс может быть назван хелатным комплексом железа. Однако возможно и образование тетрамера, при условии, что группа NH - является функциональной группой аминокислоты. На основе результатов ИК- и ЯМР- спектроскопии предложена вероятностная модель взаимодействия гидролизата коллагена и эластина с железом:
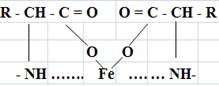
В результате исследований установлено, что 1 см3 раствора «эластин-железо» содержит 0,51 мг железа, «коллаген-железо» - 0,41 мг [1]. Разное количество связанного железа гидролизатами эластина и коллагена можно объяснить разными условиями гидролиза эластина и коллагена. При получении гидролизата эластина был использован направленный ферментативный гидролиз, с использованием пепсина, и соответственно можно прогнозировать по каким связям рвется пептидная цепочка. В случае получения гидролизата коллагена использовался кислотный гидролиз, приводящий к хаотическому разрыву пептидной связи.
В результате проведенных исследований установлены оптимальные условия и режимы взаимодействия йода и железа с гидролизатами коллагена и эластина. Полученные ассоциаты, содержащие йод и железосодержащие комплексы могут быть представлены как в жидкой, так и порошкообразной форме. Исследования стабильности полученных образцов дали положительные результаты при воздействии технологических процессов и в течение срока хранения. Для получения порошкообразной формы использовали атмосферную сублимационную сушку.
Таким образом, разработаны технологии органических форм йода и железа на основе гидролизатов соединительнотканных белков, способных связывать заданное количество микроэлемента.
На последующих этапах рассматривали возможность использования растительных отваров в качестве растворителя для желатина. Желатин – гидролизованный коллаген, который используется в качестве гелеобразователя в пищевой промышленности. В качестве растительного сырья использовали шелуху красного и желтого луков. Предварительно был изучен химический состав шелухи и определены содержания фенольных соединений. Цвет шелухи и самого лука определяются присутствием антоцианов.
Рассматривали изменения вязкости растворов желатина, полученных на отваре шелухи красной (опыт 1) и желтой (опыт 2). Результаты исследований количественного содержания фенольных соединений в растворах желатина разных концентраций представлены в таблице 1.
Таблица 1 - Количественное содержание фенольных соединений
|
Массовая доля желатина, % |
Опыт 1 |
Опыт 2 |
||
|
Сумма фенольных соединений |
В том числе, полифенольные соединения |
Сумма фенольных соединений |
В том числе, полифенольные соединения |
|
|
Отвар |
8,47 |
6,35 |
6,8 |
3,95 |
|
1% |
6,7 |
3,4 |
5,9 |
2,48 |
|
2% |
6,35 |
3,05 |
5,72 |
2,3 |
|
3% |
5,6 |
2,72 |
5,45 |
2,12 |
|
4% |
4,48 |
2,04 |
5,08 |
1,98 |
Количественное содержание фенольных соединений уменьшается в растворах желатина в отличие от исходных отваров. Вязкость растворов желатина на основе отваров была выше водных растворов желатина той же концентрации [2]. Это возможно объясняется тем, что происходит взаимодействие белковых молекул желатина с фенольными соединениями растительных отваров. Опытные образцы по вкусу, запаху и аромату не отличались от водных растворов желатина, цвет соответствовал цвету растительных отваров. Использование отваров в качестве растворителя желатина способствует экономии желатина при приготовлении растворов.
Таким образом, модифицированные соединительнотканные белки могут быть использованы в качестве матрицы биологически активных веществ: йода, железа и фенольных соединений.
Работа выполнения в рамках госзадания МОиН РФ №2014-23.
Рецензенты:
Данилов М.Б., д.т.н., профессор, заведующий кафедрой «Технология мясных и консервированных продуктов», ФГБОУ ВПО Восточно-Сибирского государственного университета технологий и управления, г. Улан-Удэ.
Ханхалаева И.А., д.т.н., профессор, заведующий кафедрой «Стандартизация, метрология и управление качеством», ФГБОУ ВПО Восточно-Сибирского государственного университета технологий и управления, г. Улан-Удэ.



