Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
LOWER JAW BONE REGENERATION USING TISSUE ENGINEERING
хирургии поиск путей оптимизации
репаративного остеогенеза также связан
с развитием дентальной имплантологии…
Иорданишвили А.К.
Восстановление дефектов костной ткани нижней челюсти является одной из наиболее актуальных проблем современной стоматологии и ортопедии. Причины потери костной ткани разнообразны: удаление зубов, воспалительные процессы, травмы, опухоли, остеопороз. В ряде случаев в стоматологической практике процесс ортопедической реабилитации связан с необходимостью заживления костных дефектов нижней челюсти. В связи с этим поиск оптимального материала для пластического замещения дефектов нижней челюсти является актуальным.
В последние годы широкое распространение получили методы клеточной терапии, основанные на применении остеогенных клеток, полученных из различных тканевых источников: костного мозга, жировой ткани [4], пульпы зуба, периферической крови и т.д. [1]. По мере накопления и анализа данных, касающиеся клеточной инженерии формируется новое направление: разработка различных конструкций по своим биологическим свойствам, приближающимся к нативной костной ткани [2, 3].
Совершенно очевидно, что использование тканеинженерных конструкции должно быть четко аргументировано в зависимости от характера, типа и локализации повреждения. В связи с этим, накопленный в настоящее время достаточно обширный материал нуждается в дальнейших экспериментальных и клинических подтверждениях эффективности конструкций и выработке четких показаний к их использованию. Одним из требований к пластическому материалу при ортопедической и любой другой патологии является тканеспецифичность, отсутствие токсичности, высокий регенераторный потенциал и формирование органоспецифической ткани в зоне трансплантации [5].
Выбор пластического материала для замещения дефекта костной ткани связан особенностями гистогенеза нижней челюсти. Известно, что в процессе эмбрионального развития и при регенерации костная ткань формируется на основе десмального остеогенеза.
Подобным требованиям отвечает разработанный в Новосибирском научно-исследовательском институте травматологии и ортопедии им. Я.Л.Цивьяна трехмерный остеотрансплантат. Структурная композиция трехмерного остеотрансплантата представлена клетками, матриксом и сосудами, что обеспечивает быструю адаптацию в условиях трансплантации.
Преимуществом остеотрансплантата являются: отсутствие антигенной активности, что позволяет производить ксенотрансплантацию.
Цель: исследовать остеорегенераторные потенции остеотрансплантата при замещении дефекта костной ткани нижней челюсти в эксперименте.
Материалы и методы
Исследование выполнено на животных с соблюдением положений Хельсинской декларации Всемирной медицинской ассоциации и Правилами проведения работ с использованием экспериментальных животных (утв. Приказом Министерства Здравоохранения Российской Федерации от 19.03.2003 г. №226).
Материалом для культивирования служили хондробласты, извлеченные в стерильных условиях из позвоночника новорожденного мини – поросенка. В стерильных условиях выделяют пластинки роста тел позвонков. Пластинки роста дважды промывают раствором фосфатного буфера и измельчаются в чашке Петри скальпелем. Кусочки переносятся в пробирки с раствором 1,5 % коллагеназы в среде RPMI 1640 с добавлением 20% FBS. Инкубируют в течение 12 часов. Далее суспензию дважды промывают от коллагеназы раствором фосфатного буфера. Клетки ресуспензируют в PBS. Жизнеспособность клеток хондробластов оценивают с помощью красителя трипанового синего в счетной камере Горяева.
Выделенные хондробласты культивируют в условиях инкубатора при 37°С при 90% влажности и 5% СО2 в чашках Петри в культуральной среде RPMI 1640 с добавлением 20% FBS и гентамицином 1 г/л в течение 3-4 недель. Далее производят пассирование клеток с помощью смеси растворов 0,25% трипсина и 0,02% раствора ЭДТА. Клетки центрифугируют при 2000 об/мин в течение 10 минут. Клеточный агрегат культивируют в 6-луночном планшете с питательной средой 10% FBS в течение 4-6 недель. Смену среды осуществляли 2 раза в неделю до получения хондротрансплантата.
Остеогенную дифференцировку хондротрансплантата производили путем помещения в питательную среду, содержащую индукторы остеогенной дифференцировки: 10 милимоль/л ß-глицерофосфа, 100 наномоль/л дксаметазона и 0,2 милимоль/л аскорбиновой кислоты.
Остеогенную дифференцировку трансплантата подтверждали методами традиционной морфологии, гитстохимии.
Основными структурными компонентами трехмерного остеотрансплантата являются остеогенные клетки (остеобласты), предкостный матрикс, содержащий гидроксиаппатит, коллаген I типа и протеогликаны. Наличие сформированных каппилляров является фактором быстрой остеоинтеграции в условиях трансплантации.
Благодаря данным особенностям трехмерный остеотрансплантат обладает потенциями к формированию диффинитивной костной ткани.
Экспериментальная проверка регенераторных потенций остеотрансплантата выполнена на 10 самцах крыс линии Wistar, возрастом 1 месяц. Под общим наркозом, скальпелем произвели разрез 5 мм в проекции угла нижней челюсти. Распатором отслоили жевательную мышцу – обнажили кость. При помощи твердосплавного шаровидного бора, с вестибулярной поверхности ветви нижней челюсти на расстоянии 3 мм выше угла нижней челюсти, сформировали трепанационное отверстие диаметром 1 мм. Животным I группы дефект заполняли трехмерным остеотрансплантатом диаметром 1,2 мм. За счет трехмерной структуры и упруго эластических свойств остеотрансплантат плотно прилегал к стенкам артифициального дефекта. Замещенный трехмерный остеотрансплантатом дефект закрывали фасцией и жевательной мышцей. Десяти животным контрольной группы формировали трепанационное отверстие диаметром 1 мм, и закрывали фасцией и жевательной мышцей, не заполняя дефект. Рану ушили материалом «Vicryl».
Животных выводили из эксперимента через 2 недели, 1, 3, 6 месяцев. Визуально оценивали наличие остаточного дефекта и выраженность гипертрофии мягких и костных тканей в области трансплантации. Зону трансплантации исследовали рентгенологически. Препараты нижней челюсти фиксировали в 10% нейтральном формалине, декальцинировали в трилоне «Б», после проводки заливали в парафин и окрашивали гематоксилинэозином и по Ван Гизону. Оценку процесса репаративного остеогенеза проводили под микроскопом «Carl Zeiss».
Результаты исследования
Через 2 недели эксперимента (рис 1) зона бывшего дефекта заполнена остеогенной тканью, среди которой сформированы первичные костные структуры. Вокруг первичных костных балочек располагаются активные остеобласты в виде цепочек. Межбалочное пространство занято остеобластами на разной стадии дифференцировки и сосудистыми полостями, выстланными эндотелием. Зона трансплантации окружена костной тканью с признаками активации остеогенеза: на внутренней поверхности костных балок располагаются активные остеобласты.
Через 1 месяц эксперимента (рис.2) в зоне трансплантации сформирована примитивная костная ткань балочного строения. Между балками располагается костный мозг и сосуды, заполненные эритроцитами. Костные балки имеют мозаичное строение. Участки более зрелой костной ткани с регулярным расположением остеобластов и линиями склеивания чередуются с зонами примитивной костной ткани. Остеобласты располагаются нерегулярно, матрикс гомогенный, линии склеивания отсутствуют. Костные структуры окружены цепочками остеобластов. Активный процесс остеогенеза продолжается.
Через 3 месяца эксперимента (рис.3) зона трансплантации заполнена костной тканью балочного строения. В некоторых участках процесс трансформации в органоспецифическую костную ткань все еще не завершен. Участки примитивной костной ткани располагаются среди зрелых структур. Процесс остеогенеза еще не закончен. Вокруг костных балок располагаются активные остеобласты. Между костными структурами сформированы очаги костного мозга.
Через 6 месяцев эксперимента (рис.4) в области пластического замещения дефекта остеотрансплантатом образовался единый костный массив. Зона трансплантации слилась с материнским ложем, границы бывшего дефекта установить невозможно. В центре сформированной костной ткани происходит процесс ремоделирования в пластинчатую костную ткань органоспецифичную для нижней челюсти. На поверхности располагается костная пластинка зрелого строения, в центральных отделах более зрелые структуры чередуются с участками в состоянии ремоделирования.
Через 6 месяцев эксперимента (контроль) (рис.5) артифициальная полость заполнена соединительно-тканным регенератом плотноклеточной структуры, между фибробластами и единичными сосудами располагаются коллагеновые волокна. Процесс костеобразования отсутствует.
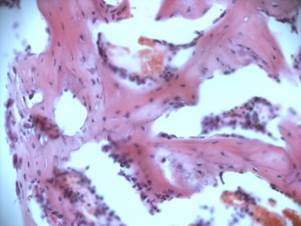
Рис 1. Зона бывшего дефекта заполнена примитивной костной и остеогенной тканью. Гематоксилин-эозин х 400
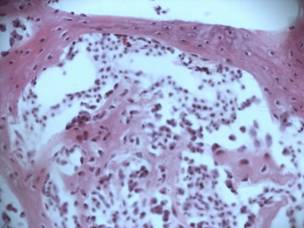
Рис. 2. Костная ткань балочного строения, костные балки окружены цепочками остеобластов с элементами костного мозга между балками. Гематоксилин-эозин х 200
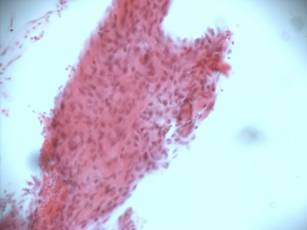
Рис.3. В области артифициального дефекта располагается молодая костная ткань балочного строения. Гематоксилин-эозин х 400
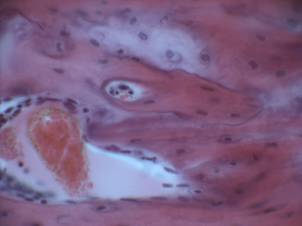
Рич.4. Дефект заполнен органоспецифичес-кой костной тканью. Наблюдается полная интеграция материнского ложа со сформи-рованной костной тканью на основе остео-трансплантата. Гематоксилин-эозин х 400
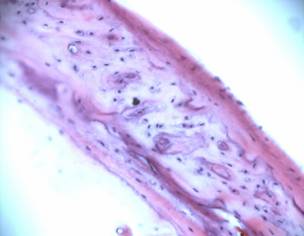
Рис.5. Область бывшего артифициального дефекта заполнена соединительной тканью, редкими кровеносными сосудами. Гематоксилин-эозин х 200
Заключение
Замещение дефекта костной ткани нижней челюсти остеотрансплантатом обеспечивает быструю регенерацию на основе остеогенных структурных компонентов пластического материала: остеобластов синтезирующих углеводные, белковые и минеральные компоненты кости, кровеносных сосудов, выстланных эндотелием, синтезирующим факторы роста сосудов (А.М. Зайдман, 1999; Maes C., 2002), инициирующие механизм реваскуляризации. Процесс остеогенеза осуществляется прямым путем на основе сформированной in vitro остеогенной ткани. Подобные свойства трансплантата позволяют осуществить полное замещение дефекта в короткие сроки. Уникальные свойства исследуемого пластического материала позволяют осуществить ксенотрансплантацию и тем самым избежать дополнительных манипуляций, связанных с забором трансплантата у пациентов.
Рецензенты:Дровосеков М.Н., д.м.н., главный врач клиники «Доктор Стоматолог», г. Новосибирск;
Железный С.П., д.м.н., профессор, ООО «Профессорская клиника Железных», г. Новосибирск.
Библиографическая ссылка
Зайдман А.М., Иванова Н.А., Косарева О.С., Сухих А.В., Корель А.В. РЕГЕНЕРАЦИЯ КОСТНОЙ ТКАНИ НИЖНЕЙ ЧЕЛЮСТИ МЕТОДОМ ТКАНЕВОЙ ИНЖЕНЕРИИ // Современные проблемы науки и образования. 2015. № 6. ;URL: https://science-education.ru/en/article/view?id=23234 (дата обращения: 16.05.2026).



