Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
STUDY RESULTS OF DNA DAMAGE IN MONONUCLEAR CELLS IN PATIENTS WITH PSORIASIS BY DNA COMET ASSAY
У исследователей мультифакториальныеболезни привлекают особое внимание, поскольку имеют генетическую компоненту, но при этом не подчиняются менделевскому наследованию (одна мутация – одна болезнь). Такие болезни рассматривают как результат взаимодействия большого числа факторов генетической природы и среды обитания, в том числе возраста, пола итабакозависимости[10]. Появлению генетически обусловленных заболеваний способствует спонтанная или индуцированная нестабильность генома, сопровождающаяся мутациями в нескольких генах. Феномен нестабильности генома, как любое биологическое явление, может иметь негативное или позитивное значение для организма. Поэтому важную роль в исследованиях играет изучение изменений в геноме [2,5].
Метод ДНК-комет впервые был предложен P.Ostling и K.Johanson в 1984г., является быстрым и чувствительным способом, позволяющим оценивать интегральную целостность генома, а также получать адекватную информацию об общем уровне повреждения ДНК клеток [3, 9]. Не вызывает сомнения, что спонтанная нестабильность ДНК различается в клетках различных тканей и органов, однако остается открытым вопрос о том, какие из нихявляютсянаиболее чувствительными индикаторами для различных генотоксикантов[1].
Кроме того, отмеченоповышение уровня разрывов ДНК при аутоиммунных, нейродегенеративных, генетически детерминированных, злокачественных, острых инфекционных и ряде других мультифакториальныхзаболеваний по сравнению со здоровыми людьми [1,3]. Подобныеисследования у больных псориазом, получающих различные виды иммуносупрессивной терапии, не проводились.Примерных нормативов уровня поврежденности ДНКмононуклеарных клеток крови в доступной литературе мы не обнаружили, что весьма затрудняет применение это перспективного метода диагностики в практике работы врача, в частности дерматовенеролога.
Все это явилось поводом для проведения настоящего исследования, имеющего своей целью изучениевозможностей метода ДНК-комет в дополнительной диагностике и оптимизации лечения псориаза.
Материалы и методы
Для достижения цели нами были решены следующие задачи: 1) определен фоновый уровень поврежденности ДНК больных псориазом в сравнении с контрольной группой здоровых лиц, 2) оценены различия уровня поврежденности ДНК у лиц разного возраста, пола и в зависимости от вредной привычки – курения, 3)предложены примерные границы референтного интервалауровня поврежденности ДНКмононуклеарныхклеток крови для здоровых некурящих лиц.
В настоящее время общепризнано, что табачный дым является самым распространенным из доказанных канцерогенов для человека и одной из основных причин заболеваемости, инвалидности и смертности. В целом ряде специальных опытов и исследований была убедительно подтверждена способность компонентов табачного дыма образовывать с ДНК мутагенные аддукты, которые могут приводить к генетической нестабильности с повышенной вероятностью появления и накопления мутаций или другим повреждениям клеточных генов [6]. Однако в работе Арутюняна Р. М. отмечено, что повышение уровня повреждений ДНК в группе курящих по сравнению с некурящими было получено в эксфолиативных клетках слизистой ротовой полости, но аналогичное исследование в лимфоцитах дало противоречивые результаты. Результаты оценки уровней повреждений ДНК в различных возрастных группах тоже противоречивы, однако большинство из них свидетельствует об отсутствии корреляции частоты ДНК-комет с возрастом [1].Поэтому для разработки примерных границ референтного интервалауровня поврежденности ДНК были взяты мононуклеарные клетки периферической крови группы некурящих доноров от 18 до 60 (73 человека, 38мужчин и 35женщин).
В исследовании приняли участие73 больных псориазом, находящихся на стационарном лечении в БУЗ Омской области «ККВД» и103 донора БУЗ Омской области «Центр крови»в качестве группы контроля.Исследование клеток крови методом ДНК-комет проводилось в лаборатории кафедры клинической фармакологии ОмГМУ.
Критерии включения в основную группу (больных псориазом) сформулированы следующим образом: возраст старше 18 лет, добровольное согласие на участие в исследовании, заверенное личной подписью,диагноз «Псориаз вульгарный, прогрессирующая стадия (L40.0)», индексPASI более 10%.Критериями исключения были: пустулезный псориаз, псориатическая эритродермия, злокачественные новообразования и воздействие ионизирующей радиации в анамнезе, тяжелые заболевания печени и почек, хронические заболевания в стадию обострения, вирусные гепатиты, а также диагностические и лечебные процедуры с использованием рентгеновского и других видов облучения в течение четырех недель, прием алкоголя за двое суток до исследования. Образцы крови в основной группе взяты у 68 мужчин и 5 женщин в возрасте от 18 лет до 60 лет.
Отбор в группу сравнения (контрольную группу) осуществлялся согласно критериям включения: обследование согласно утвержденному порядку медицинского обследования донора крови и её компонентов [7], возраст от 18 до 60 лет, добровольное информированное согласие на участие в исследовании, заверенное личной подписью. Критериями исключения явились хронические заболевания в стадии обострения, применение лекарственных препаратов, диагностические и лечебные процедуры с использованием рентгеновского и других видов облучения в течение четырех недель, прием алкоголя за двое суток до исследования.В группе сравнения исследована кровь 55 мужчин и 48 женщин в возрасте от 18 лет до 60 лет.
Протокол исследования был одобрен локальным научным этическим комитетом ОмГМУ.
Кровь была получена посредством вакуумных систем в общем объеме 2 мл. Хранение и транспортировка крови осуществлялась в пробирках, покрытых раствором ЭДТА (К2) с использованием консерванта в соотношении 1:1. Консервант готовился extempore соединением растворовRPMI-1640 и ДМСО в соотношении 8:2. Хранение консервированной крови осуществлялось при температуре – 20оС, транспортировка – при 4оС. Проводили поэтапную обработку клеток крови: получение гель-слайдов с подложкой из агарозы и суспензии исследуемых клеток, помещение клеток в агарозный гель и нанесение на гель-слайды, лизис, щелочную денатурацию, электрофорез, фиксацию, окрашивание и микроскопический анализ [3]. Окрашивание люминесцентным красителем SIBR Green, анализ с помощью флюоресцентного микроскопа (ЛОМО, МИКМЕД 6, фильтр возбуждения, дихронное зеркало, запирающий фильтр, объектив 20Х). Сканирование и обработку ДНК-комет проводили при помощи программы САSP (рис.1).Нарисунке 1 представлены гель-слайды клеток крови: А – неповрежденные клетки (форма клетки не изменена), Б – поврежденные клетки (форма клетки изменена, имеется хвост кометы). И в этом хвосте находится фрагментированная ДНК, вышедшая из ядра клетки. При этом, чем больше процент содержания ДНК в хвосте кометы, тем выше уровень поврежденности ДНК клетки.
 А
А
 Б
Б
Рис.1. Гель-слайды клеток крови: А – неповрежденные клетки, Б – поврежденные клетки
Статистическая обработка данных проводилась на основании современных методических подходов[8], с использованием пакета STATISTICA 6.1,MicrosoftOfficeExcel2007. Проверку нормальности распределения количественных параметров проводили с помощью критериев Колмогорова-Смирнова, Лиллиефорса и Шапиро-Уилка. Описание совокупности и разработка референтных интервалов уровня поврежденности ДНК мононуклеарных клеток крови проводилось методом персентилей,с использованием показателей медианы (Р50), верхних и нижних децилей (Р10 и Р90), квартилей (Р25 и Р75), минимума (Р0) и максимума (Р100).За верхнюю границу нормы изучаемого признака взят показатель Р75 в группе некурящих доноров. Для оценки связей применялся метод ранговой корреляции Спирмена с расчетом коэффициента корреляции rs и уровня статистической значимости р, а также визуализацией связи в целях ее проверки. Для сравнения количественных показателей двух независимых групп использован U-критерий Манна-Уитни, метод Фишера и χ2.В исследовании результаты считались значимыми при р< 0,05, значения уровня значимости приведены в виде р = 0,000….
Результаты исследования и их обсуждение
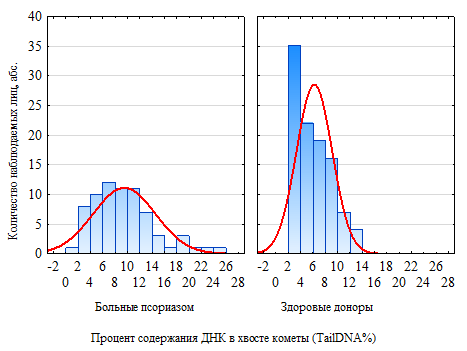
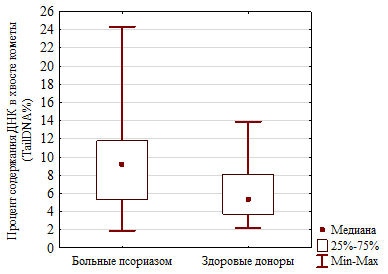
Болезнь. На рисунке 2 представлены результаты распределения уровня поврежденности ДНК мононуклеарных клеток крови в основной и контрольной группах. На рис 2А – количество наблюдаемых лиц в зависимости от уровня показателя,2Б – показатели распределения: медианы (Р50), квартилей (Р25 и Р75), минимума (Р0) и максимума (Р100).
А
Б
Рис. 2. Сравнительная характеристика показателей ДНК в хвосте кометы в группах больных и здоровых (U=2144,0; p=0,000): А – распределение наблюдаемых лиц в зависимости от уровня показателя, Б – показатели статистической нормы изучаемого признака (медианы Р50, квартилей Р25 и Р75), а также минимума (Р0) и максимума (Р100)
Как видно из рисунка 2, между группами больных псориазом и здоровых установлены статистически значимые различия по изучаемому показателю ДНК в хвосте кометы.
Во-первых, визуально распределение спонтанного уровня поврежденности ДНК в группе здоровых резко ассиметрично, с выраженной правой ветвью, что указывает на то, что большая часть здоровых людей имеет минимальный процент содержания ДНК в хвосте кометы клеток крови. Среди больных псориазом распределение признака приближается к нормальному, симметрично и уплощено, так что процент содержания ДНК в хвосте кометы в этой группе составляет от 1,9 до 24,3%, в то время как в группе здоровых – от 2,2 до 13,9% (рис. 2А и 2Б). В отношении определения нормы признака важно то, чтотреть здоровых людей имели минимальные показатели признака (от 2 до 4%) (рис. 2А). Однако же и часть больных, а именно 9 человек, имело такой же низкий уровень признака.
Во-вторых, отмечено статистически значимое превышение изучаемого показателя в группе больных по сравнению с контролем –9,2 и 5,4%[1] (U=2144,0; p=0,000).Подобное различие спонтанной фоновой поврежденности ДНК между здоровыми донорами и больными псориазом, возможно, указывает на генетическую природу заболевания, геномную нестабильность – селективный механизм, который позволяет клеткам приспособиться к изменившимся условиям существования с постепенной нормализацией своих функций или связано с прогрессирующей стадией данного заболевания, сопровождающейся повышением интенсивности процессов перекисного окисления липидов в плазме крови и избыточным образованием активных форм кислорода, обладающих генотоксическими и мутагенными свойствами.
Таким образом, можно утверждать, что этот метод информативен и для больных псориазом, результаты вполне приемлемы и объяснимы с точки зренияэтиопатогенеза и клиники псориаза [4].
Пол. Установлено отсутствие зависимости уровня изучаемого показателя от пола на примере контрольной группы. У мужчинпроцент ДНК в хвосте кометы составил от 2 до 14,3%, у женщин от 2 до 13%. В среднем по медиане у мужчин– 5,9, у женщин – 4,9% (при не существенных различиях).
Курение. При сравнении мужчин и женщин в контрольной группе по признаку «курение» статистически значимого различия не выявлено (χ2=0,18; р=0,67), то есть группы мужчин и женщин по признаку курения однородны и их можно сравнивать.
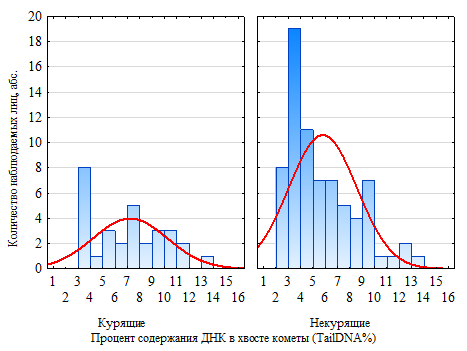
На рисунке 3приведеныхарактеристики распределения уровня поврежденности ДНК ядросодержащих клеток крови в контрольной группе среди курящих и некурящих лиц контрольной группы.
А
Б
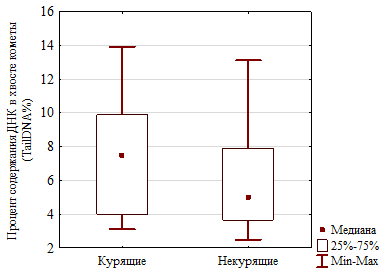
Рис. 3. Сравнительная характеристика показателей ДНК в хвосте кометы среди курящих и некурящих в группе здоровых доноров: А – количество наблюдаемых лиц в зависимости от уровня показателя (U=784,0; p=0,024), Б – показатели распределения: медианы (Р50), квартилей (Р25 и Р75), минимума (Р0) и максимума (Р100)
В контрольной группе установлено статистически значимое превышение показателя спонтанного уровня поврежденности ДНК в ядросодержащих клетках крови курящих по сравнению с некурящими –7,5 и 5,0%, соответственно (U=784,0; p=0,024). Большая часть исследуемого контингента имеют уровень признака в диапазоне от 3 до 4 (рис. 3).
В группе больных псориазом не установлено статистически значимого различия изучаемого признака по признаку курения: у курящих среднее значение по медиане составило 9,6%, у некурящих – 8,7%.
То есть, получены противоречивые результаты зависимости исследуемого признака от курения у больных и здоровых.
Референтныйинтервалуровня поврежденности ДНК в ядросодержащих клетках крови.На рисунке 4 представлены показатели распределения изучаемого признака в контрольной группе, с разделением курящих и некурящих (поскольку отмечены статистически значимые различия).
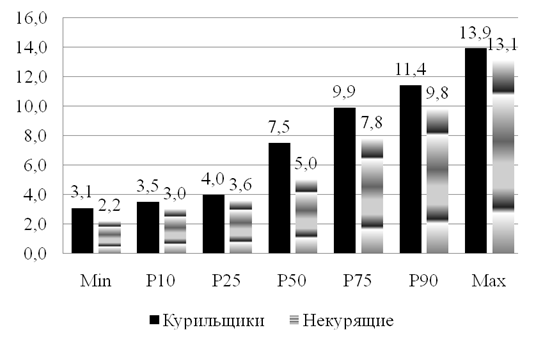
Рис. 4. Показатели распределения поврежденности ДНК в ядросодержащих клетках крови курящих и некурящих лиц контрольной группы
При решении задачи разработки границ референтного интервала уровня поврежденности ДНК в ядросодержащих клетках крови было принято положение о том, что о патологии свидетельствует увеличение признака, а не уменьшение. Поэтому нижней границей референтного интервала изучаемого признака принят 0,0 (минимальное значение показателя или Р0), а в качестве верхней границы – значениетретьего квартильного интервала Р75, причем для некурящих. Таким образом, возможный уровень поврежденности ДНК у здоровых лиц варьирует в пределах от 0 до 7,8% (Р0– Р75) .
Возраст. Отмечено отсутствие зависимости уровня поврежденности ДНК мононуклеарных клеток крови от возраста как в основной (rs = -0,061, р = 0,616), так и контрольной группах (rs= -0,094, р = 0,345) (рис. 5). Как видно из рисунка 5, минимальный уровень показателя – около 2,0% – имели пациенты в возрасте31, 34, 39 и 58 лет, а максимальный уровень признака – более 18%- отмечен у пациентов в возрасте от 29 до 46 лет. Стрелочками отмечены пациенты, имевшие минимальный уровень поврежденности ДНК ядросодержащих клеток крови, а в овале, очерченным черной сплошной линией представлены больные с максимальными показателями.
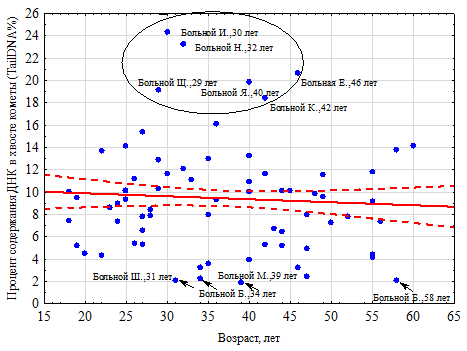
Рис.5. Зависимость уровня поврежденности ДНК мононуклеарных клеток крови от возраста у больных псориазом
Установленный фактсогласуется с данными литературы (Арутюнян Р. М, Оганесян Г.Г, Нерсесян А. К., 2001).
Интерпретируя полученные результаты, можно сделать вывод, что в группе больных псориазом уровень поврежденности ДНК клеток крови не зависел от возраста и наличия вредной привычки курение, а в контрольной группе – степень поврежденности ДНК у курящих была выше, а от возраста и пола не зависела.
Различия уровня поврежденности ДНК ядросодержащих клеток крови среди мужчин и женщин в основной группе будут опубликованы позднее.
Выводы:
1. Результаты нашего исследования показали, что фоновая поврежденность ДНК периферических мононуклеарных клеток крови у больных псориазом по сравнению с контрольной группой выше: соответственно, 9,2 и 5,4% по медиане (U=2144,0; p=0,000).
2. В контрольной группе отмечены статистически значимое превышение степени поврежденности ДНК в группе курильщиков по сравнению с некурящими: 7,5 и 5,0% по медиане (U=784,0; p=0,024). У больных псориазом такой зависимости не установлено: у больных курильщиков степени поврежденности ДНК составляет 9,6%, а у некурящих больных – 8,65% (U=588,0; p=0,783).
3. Не установлено зависимости фонового уровня поврежденности ДНК ядросодержащих клеток крови от возраста ни в основной, ни в контрольных группах. В контрольной группе не отмечено существенных различий изучаемого признака у мужчин и женщин.
4. Предложены границы референтного интервала уровня поврежденности ДНК ядросодержащих клеток крови – от 0 до 7,8%. Интервал рассчитан по данным некурящих здоровых лиц.
5. Метод ДНК-комет является чувствительным методом для определения спонтанного или индуцированного уровня поврежденности ДНК клеток крови больных псориазом и может быть использован в дальнейших исследованиях в направлении изучениягенотоксичностииммуносупрессивныхметодов терапии псориаза.
Коллектив авторов выражает признательностьруководству и сотрудникам БУЗ ОО «ККВД»иБУЗ ОО «Центр крови» за помощь в наборе клинического материала.
Рецензенты:Матусевич С.Л., д.м.н., доцент кафедры, заведующий кафедрой кожных и венерических болезней с курсом косметологии ГБОУ ВПО «Тюменский государственный медицинский университет» Министерства здравоохранения РФ, г.Тюмень;
Немчанинова О.Б., д.м.н., профессор, заведующая кафедрой дерматовенерологии и косметологии ГБОУ ВПО «Новосибирский государственный медицинский университет» Министерства здравоохранения РФ, г.Новосибирск.
[1]среднее значение по медиане
Библиографическая ссылка
Охлопков В.А., Гудинова Ж.В., Полещук Е.И., Жернакова Г.Н., Скальский С.В., Роскошная Д.В., Ступакова Л.В., Репина Т.В. РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ УРОВНЯ ПОВРЕЖДЕННОСТИ ДНКМОНОНУКЛЕАРНЫХ КЛЕТОК КРОВИ БОЛЬНЫХ ПСОРИАЗОМ МЕТОДОМ ДНК-КОМЕТ // Современные проблемы науки и образования. 2015. № 6. ;URL: https://science-education.ru/en/article/view?id=23073 (дата обращения: 19.05.2026).



