Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
DEVELOPMENT OF STANDARD TIME FOR THE PCR IN THE DIAGNOSIS OF AVIAN INFLUENZA
Эффективным молекулярным методом диагностики гриппа птиц является метод полимеразой цепной реакции (ПЦР) [1]. ФБУН ЦНИИ эпидемиологии совместно с ФГБУ ВГНКИ разработана тест-система «Грипп» для ветеринарных целей, позволяющая обнаруживать РНК вируса гриппа А и идентифицировать субтипы с использованием как электрофоретического способа детекции, так и гибридизационно-флюоресцентной детекции в форматах реального времени (например, с помощью амплификаторов «Rotor Gene» 3000/6000, «iQ5» или «iCycler iQ») и по конечной точке (с помощью детекторов «АЛА-1/4» или «Джин») [2]. Для эффективного использования рабочего времени ветеринарных специалистов, занятых постановкой ПЦР при диагностике инфекционных болезней мелких домашних животных разработаны нормы времени на осуществление реакции электрофоретической детекцией продуктов амплификации в агарозном геле и в режиме реального времени [3] и постановку ПЦР при описторхозе плотоядных животных [4].
Цель исследования. Разработка норм времени методом полимеразной цепной реакции с использованием различных его вариаций при диагностике гриппа птиц.
Материал и методы исследования. Исследования проводились в отделе вирусологии и генно–молекулярной диагностики ФГБУ «Татарская межрегиональная ветеринарная лаборатория». В качестве модели изучения выбрана диагностика гриппа птиц методом полимеразой цепной реакции с использованием различных методов: 1) постановка ПЦР электрофоретическим методом – формат EPh; 2) постановка ПЦР в режиме реального времени – формат FRT; 3) постановка ПЦР по конечной точке – формат FEP. Исследования проводили в несколько этапов: 1) изучение лабораторного оборудования при диагностике болезней птиц; 2) определение видов и методов диагностики вируса птичьего гриппа; 3) определение графика проведения хронометражных и фотохронометражных исследований; 4) изучение затрат труда на фотохронометражные и хронометражные исследования при постановке ПЦР на гриппа птиц; 5) анализ полученных результатов; 6) апробация полученных норм времени в лаборатории. Было проведено 31 хронометражное и 25 самохронометражных наблюдения и моделирование опыта с марта по август 2015 года с соблюдением требований Методических рекомендаций по нормированию труда ветеринарных специалистов (Одобрено НТС МСХ РФ 26 декабря 2014 г.). При постановке ПЦР ветеринарные специалисты отдела руководствовались «Инструкцией по применению тест-системы «ГРИПП» для выявления и дифференциации вируса гриппа птиц методом полимеразой цепной реакции» (производитель: ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, г. Москва), методическими указаниями МУ 1.3.2569 – 09. Нормы времени устанавливали для шести форматов постановки ПЦР на грипп птиц.
Обычно с птицеводческих хозяйств биологический материал поступает партиями от 10 и более проб одновременно. В качестве наиболее распространенного количества одновременно проводимых исследований мы брали 10 проб. Независимо от количества одновременно участвующих в постановке ПЦР образцов каждый раз проводили постановку положительных и отрицательных контролей (2 образца).
Результаты исследования и их обсуждение. В отделе вирусологии и генно–молекулярной диагностики ФГБУ «Татарская МВЛ» ежегодно проводится 3357 исследований на грипп птиц, в том числе методом ПЦР – 265. Проведению хронометражного исследования предшествовала предварительная подготовка хронометристом: тщательное изучение постановки ПЦР в различных вариациях; подготовка хронометражных листов и секундомера; согласование графика проведения исследований с руководством ФГБУ «Татарская МВЛ» и сотрудниками отдела вирусологии и генно–молекулярной диагностики. Осуществлены хронометражные наблюдения за работой четырех опытных ветеринарных врачей со стажем более 3-х лет.
Биологическим материалом для исследования служили помет; мазки из клоаки или с глотки и трахеи; трахеальные смывы; внутренние органы, мясо птицы, субпродукты; яйцо больной (подозреваемой в заболевании) птицы. Мазки и смывы для постановки ПЦР использовали без предварительной обработки. Остальной биологический материал подвергался предварительной обработке.
Постановку ПЦР осуществляли два ветеринарных специалиста, первый проводил исследования в 1 и 2 зонах, с переходом с одной зоны в другую с предварительной сменой одежды. Второй специалист работал в 3 зоне, где проводил детекцию продуктов амплификации методом электрофореза в агарозном геле и осуществлял учет и интерпретацию полученных результатов.
Разработаны нормы времени на подготовку биологического материала одной пробы, при одновременной подготовке 10 и 20 проб. Затраты времени ветеринарного специалиста на подготовку 1 пробы помета к исследованию составили 4,4 мин., 10 проб – 14,6 мин., 20 проб – 26,5 мин. Ветеринарный специалист на подготовку пробы внутренних органов, мяса, субпродуктов затрачивает 4,6, 17,7 и 32,7 мин.; яйца – 4,5, 16,9, 31,1 мин. соответственно. В зависимости от количества одновременно подготавливаемых проб затраты времени на подготовку одной пробы заметно сокращаются. Стандартные отклонения нормы времени составляют во всех случаях не более 2,0 %. В качестве модели нормы времени при подготовке всех видов биологического материала при диагностике гриппа птиц методом ПЦР использовали средние затраты труда ветеринарного специалиста, что составило при исследовании 1 пробы – 4,2 мин., 10 проб – 13,3 мин., 20 проб – 24,0 мин. Наблюдается заметная экономия времени на подготовку биоматериала с увеличением количества одновременно исследуемых проб.
Диагностику гриппа птиц методом ПЦР разными способами постановки реакции всегда начинают с выявления генома вируса Influenza virus A. При обнаружении РНК вируса осуществляется дальнейшее исследование с типированием выявленного вируса. Расчеты затрат рабочего времени ветеринарных специалистов на постановку ПЦР при диагностике гриппа птиц приведены в таблице 1.
Таблица 1
Затраты рабочего времени ветеринарных специалистов на диагностику гриппа птиц методом ПЦР в различных форматах при применении тест-системы «ГРИПП»
|
Форматы постановки ПЦР |
Затраты времени на исследование, мин. |
||
|
1 пробы |
10 проб |
20 проб |
|
|
Формат EPh (выявление РНК вируса гриппа А) |
39,6 ±0,44 |
104,4±1,2 |
180,3±1,6 |
|
в том числе на 1 исследование |
39,6 |
10,4 |
9,0 |
|
Формат EPh (выявление РНК вируса гриппа А и идентификация субтипов H5 и H7) |
64,6±0,52 |
158,5±1,2 |
268,8±1,2 |
|
в том числе на 1 исследование |
64,6 |
15,9 |
13,4 |
|
Формат FEP (выявление РНК вируса гриппа А) |
29,7±0,53 |
93,1±1,0 |
166,7±1,6 |
|
в том числе на 1 исследование |
29,7 |
9,3 |
8,3 |
|
Формат FEP (выявление РНК вируса гриппа А и идентификация субтипов H5, H7 и H9) |
41,3±0,5 |
121,8±1,18 |
214,6±1,5 |
|
в том числе на 1 исследование |
41,3 |
12,2 |
10,7 |
|
Формат FRT (выявление РНК вируса гриппа А) |
27,6±0,43 |
87,9±0,8 |
158,9±1,23 |
|
в том числе на 1 исследование |
27,6 |
8,8 |
7,0 |
|
Формат FRT (выявление РНК вируса гриппа А и идентификация субтипов H5, H7 и H9) |
37,5±0, 5 |
112,4±0,72 |
201,1±1,0 |
|
в том числе на 1 исследование |
37,5 |
11,2 |
10,1 |
При исследовании единичной пробы методом ПЦР с электрофоретической детекцией продуктов амплификации в агарозном геле затраты времени ветеринарного врача составляют 39,6 мин. (выявление вируса гриппа А) и 64,6 мин. (идентификация субтипов вируса гриппа А); при одновременном исследовании 10 проб соответственно 104,4 и 158,5 мин., 20 проб – 180,3 и 268,8 мин. Затраты времени на одну пробу составили при одновременном исследовании 10 проб – 10,4 мин., 20 проб – 9,0 мин. (выявление вируса гриппа А) 15,9 и 13,4 мин. (идентификация субтипов вируса гриппа А). Увеличение количества затрачиваемого ветеринарным врачом времени при обнаружении РНК вируса гриппа А обусловлено идентификацией субтипов H5 и H7. Для продолжения реакции используют образцы РНК, давшие положительные результаты на наличие генома вируса гриппа A. При этом добавляются следующие этапы: проведение амплификации; детекция продуктов амплификации методом электрофореза в агарозном геле; учет и интерпретация результатов; внесение результатов анализа в автоматизированную систему «Веста».
В структуре затрат рабочего времени при исследовании на грипп птиц в формате EPh (рисунок 1) при исследовании единичной пробы (отрицательная реакция) наибольший удельный вес занимает экстракция РНК из исследуемого материала (28,5 %) и детекция продуктов амплификации в агарозном геле (26,5 %), меньше – проведение амплификации (18,4 %) и постановка реакции обратной транскрипции (16,9 %). При одновременном исследовании 10 и 20 проб наибольший удельный вес приходится на экстракцию РНК – 49,9 и 54,9 %, в то же время заметно уменьшаются затраты времени, связанные с детекцией продуктов амплификации в агарозном геле – 14,0 и 10,9 % соответственно. Наблюдается так же уменьшение затрат времени при проведении амплификации и постановка реакции обратной транскрипции. Затраты времени, связанные с учетом интерпретации полученных результатов занимают в пределах десяти процентов и возрастают прямо пропорционально объемам одновременно проводимых исследований.
При выявлении вируса гриппа птиц постановка реакции продолжается – идет типирование выявленного вируса. При этом структура рабочего времени ветеринарного специалиста не меняется, однако, изменяются объемы выполняемых работ в зоне 2 и 3 за счет включения повторных этапов ПЦР. Так, при исследовании единичной пробы в структуре работ наибольший удельный вес занимает детекция продуктов амплификации в агарозном геле – 33,7 % и проведение амплификации – 26,2 %. Соответственно, увеличиваются затраты времени, связанные с учетом, интерпретацией и занесением полученных результатов в автоматизированную систему «Веста» (12,2 %). Аналогичные изменения наблюдаются в структуре затрат рабочего времени ветеринарного специалиста, осуществляющего одновременные исследования 10 и 20 проб.
Затраты рабочего времени ветеринарного врача, проводящего исследование на грипп птиц методом ПЦР с электрофоретической детекцией продуктов амплификации в агарозном геле как при отрицательной, так и при положительной реакции постановка ПЦР занимает от 32,58 % (при исследовании 1 пробы, отрицательной реакции) до 72,3 % (при исследовании 20 проб, отрицательной реакции). Соответственно подготовительно-заключительные работы составляют от 27,7 до 67,4 %. Следует отметить, что наблюдается заметное сокращение затрат времени ветеринарного специалиста, связанные с обслуживанием рабочего места при одновременном исследовании 10 и 20 проб как при получении отрицательной реакции, так и при положительной реакции (когда дальнейшая работа сопряжена с типизацией вируса гриппа А).
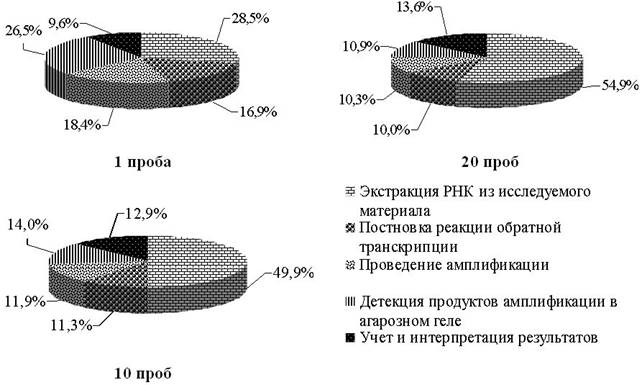
Рис.1. Структура затрат рабочего времени ветеринарного врача при применении тест-системы «ГРИПП» для выявления вируса гриппа птиц (Influenza virus A) методом ПЦР в формате EPh
Аналогичным образом осуществлен анализ затрат рабочего времени ветеринарного врача при исследовании на грипп птиц методом ПЦР по конечной точке (формат FEP) и в режиме реального времени (формат FRT). Затраты времени ветеринарного специалиста при исследовании на грипп птиц в формате FEP при исследовании единичной пробы на выявление вируса гриппа А составляет 29,7 мин., при одновременном исследовании 10 проб – 93,1 и 20 проб – 166,7 мин., при идентификации субтипов вируса гриппа А 41,3, 121,8 и 214,6 мин. соответственно.
При проведении исследований на выявление вируса гриппа А методом ПЦР по конечной точке в структуре затрат рабочего времени ветеринарного специалиста на исследование 1 пробы экстракция РНК из исследуемого материала занимает 38,4 %, проведение обратной транскрипции – 22,6 % и амплификации – 17,2 %. По сравнению с постановкой реакции ПЦР в формате EPh заметно сокращается время, затрачиваемое на детекцию (14,6 %), так как последнее осуществляется с применением флюоресцентного ПЦР детектора «Джин-4». Завершение работы с внесением полученных результатов в автоматизированную систему «Веста» занимает 16,9 % времени. При одновременном исследовании как 10, так 20 проб ветеринарный специалист больше времени затрачивает на работу в 1 зоне (экстракция РНК из исследуемого материала) – 56,5 и 60,1 %, меньше – на детекцию результатов 6,4 и 5,4 % соответственно. При идентификации субтипов (H5, H7 и H9) вируса гриппа А структура затрат рабочего времени ветеринарного специалиста внешне похоже на структуру затрат рабочего времени при выявлении вируса гриппа А.
Норма времени на выявление вируса гриппа птиц с применением тест-системы «ГРИПП» методом ПЦР в режиме реального времени (формат FRT) при исследовании 1 пробы составляет 27,6 мин., при идентификации субтипов (H5, H7 и H9) вируса гриппа А – 37,5 мин. В структуре затрат рабочего времени при отрицательной реакции приходится на экстракцию РНК вируса из исследуемого материала – 41,3 %, завершение работы – 12,7 %; при положительной реакции на проведение амплификации затрачивается 33,2 %, постановку обратной транскрипции – 17,8 %. При одновременном исследовании 10 и 20 проб затраты времени при выявлении вируса гриппа А (отрицательная реакция) составляют 87,9 и 112,4 мин., продолжении реакции с типизацией вируса соответственно 158,9 и 201,1 мин.. Экономия времени при одновременном исследовании 10 и 20 проб происходит при постановке реакции обратной транскрипции и проведении амплификации с применением амплификатора «Rotor Gene».
Метод полимеразной цепной реакции является одним из наиболее эффективных методов диагностики болезней животных и птиц. Материально-техническое оснащение лаборатории ФГБУ «Татарская МВЛ» позволило провести исследования и разработать нормы времени в трех различных режимах: электрофоретическим методом, в режиме реального времени и по конечной точке. Разработке норм времени предшествовала тщательная подготовка. Были проведены хронометражные исследования за процессом проведения ПЦР в различных режимах, однако исследования, связанные с хронометрированием «положительных» проб, в основном моделировались или опытные ветеринарные специалисты лаборатории составляли самохронометражные листы, так как за период исследования выявления вируса гриппа А (Influenza virus A) не было. Таким образом, разработаны нормы времени при исследовании на грипп птиц с использованием тест-система «Грипп» в трех вариациях и в каждой вариации постановки ПЦР норма времени в двух вариантах: 1) выявление РНК вируса гриппа А; 2) выявление РНК вируса гриппа А и идентификация субтипов вируса гриппа А.
Выводы:
1. Метод полимеразной цепной реакции является эффективным методом диагностики болезней животных и птиц.
2. Оптимальное количество одновременно исследуемых проб методом ПЦР в условиях ветеринарных лабораторий 10 и более, это позволяет экономить время ветеринарного специалиста за счет сокращения отдельных рабочих процессов во время постановки реакции.
3. Ветеринарный специалист при исследовании на грипп птиц с использованием тест-система «Грипп» методом ПЦР в режиме реального времени (формат FRT) затрачивает наименьшее время, что составляет при выявлении вируса гриппа А при исследовании единичной пробы 27,6 мин, 10 проб – 87,9 и 20 проб – 158,9 мин., при типизации вируса – соответственно 37,5, 112,4 и 201,1 мин.
Рецензенты:
Василевский Н.М., д.вет.н., профессор, заместитель директора по НИР ФГБУ «Федеральный центр токсикологической, радиационной и биологической безопасности», г. Казань;
Галиуллин А.К., д.вет.н., профессор, заведующий кафедрой микробиологии, вирусологии и иммунологии ФГБОУ ВПО «Казанская государственная академия ветеринарной медицины имени Н.Э. Баумана», г. Казань.
Библиографическая ссылка
Трофимова Е.Н., Шастин П.Н., Тюлкин С.В., Вафин Р.Р. РАЗРАБОТКА НОРМ ВРЕМЕНИ НА ПОСТАНОВКУ ПЦР ПРИ ДИАГНОСТИКЕ ГРИППА ПТИЦ // Современные проблемы науки и образования. 2015. № 2-2. ;URL: https://science-education.ru/en/article/view?id=22490 (дата обращения: 17.05.2026).



