В настоящее время во всем мире насчитывается около 347 млн больных сахарным диабетом, при этом около 50% всех больных диабетом приходится на наиболее активный, трудоспособный и репродуктивный возраст 30–59 лет. Еще 20 лет назад численность больных диабетом не превышала 30 млн человек. В 2012 г. около 1,5 млн смертей были непосредственно вызваны сахарным диабетом, которым охвачено более 85% стран. Учитывая темпы роста этого заболевания, эксперты ВОЗ прогнозируют, что количество больных сахарным диабетом к 2030 г. увеличится в 1,5 раза, а сахарный диабет займет 7-е место среди ведущих причин смертности населения [10]. Пациенты с сахарным диабетом часто подвержены таким острым осложнениям, как диабетический кетоацидоз, вызванный накоплением в крови продуктов промежуточного метаболизма жиров (кетоновые тела); гипогликемия, вызванная передозировкой сахароснижающих препаратов и приводящая к гипогликемической коме; гиперосмолярная кома, связанная с сильным обезвоживанием вследствие полиурии; лактацидотическая кома, обусловленная накоплением в крови молочной кислоты. Кроме того, наблюдаются и поздние осложнения: диабетическая ретинопатия, ангиопатия, полинейропатия, нефропатия, артропатия, энцефалопатия и диабетическая стопа. При диабете повышен риск развития психических расстройств, таких как депрессии, тревожные расстройства, расстройства приема пищи [2, 9].
Таким образом, актуальной задачей современной фармацевтической науки остается поиск новых биологически активных соединений с перспективой создания оригинальных отечественных лекарственных препаратов, а также реализации программы импортозамещения. Определенный интерес для данных исследований представляют производные 2,4-диоксобутановых кислот – 5-арил-3-ариламино-3Н-фуран-2-оны, так как способны вступать в реакции дециклизации с NH-нуклеофилами различного строения. Кроме того, возможность введения разного рода заместителей-фармакофоров в фурановый цикл имеет практическое значение в плане дальнейших биологических испытаний.
Для оптимизации фармакологического скрининга и сокращения затрат на лабораторных животных используются различные компьютерные программы, способные прогнозировать возможную биологическую активность. Также широко используются докинговые исследования для оценки возможного взаимодействия химических субстанций с активными сайтами белков рецепторов в сравнении с лекарственными препаратами [7], что позволяет производить целенаправленный синтез биологически активных соединений более эффективно и с минимальными затратами.
Целями настоящего исследования являются анализ потенциальной биологической активности с использованием программы PASS-Online [8], а также практическое изучение гипогликемической активности N-замещенных 5-арил-3-ариламино-3Н-фуран-2-онов (1) и продуктов их взаимодействия (2) с рядом аминов на модели аллоксанового сахарного диабета.
Материалы и методы
Ранее среди производных 2,4-диоксобутановых кислот были обнаружены вещества, обладающие высокой анальгетической, гипогликемической, противовоспалительной, антикоагулянтной и антигипоксической активностью [4, 5]. Для расширения ряда биологически активных соединений решено воспользоваться предварительным планированием их синтеза в ряду N-замещенных амидов 4-арил-2-гидрокси-4-оксо-2-бутеновых кислот (2). Виртуальная библиотека сформирована из соединений, содержащих различные заместители в арильном, ариламинном и гетероциклическом фрагментах:
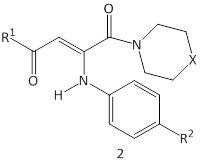
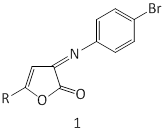
1: R=H (а), Cl (б).
2: X=NH, R1=C6H5, R2=4-BrC6H4 (а), 4-ClC6H4 (б), 4-NO2C6H4 (в), 4-CH3OC6H4 (г), R1=4-ClC6H4, R2=4-BrC6H4 (д), 4-ClC6H4 (е), 4-NO2C6H4 (ж), 4-CH3OC6H4 (з); X=O, R1=C6H5, R2=4-BrC6H4 (и), 4-ClC6H4 (к), 4-NO2C6H4 (л), 4-CH3OC6H4 (м), R1=4-ClC6H4, R2=4-BrC6H4 (н), 4-ClC6H4 (о), 4-NO2C6H4 (п), 4-CH3OC6H4 (р).
В каждую группу включались соединения, доступные для синтеза известными методами [5]. Результаты исследования приведены в таблице 1.
Острую токсичность определяли на белых нелинейных мышах обоего пола массой 20–22 г с определением LD50 по методу Г.Н. Першина. Соединения вводили перорально в виде взвеси в 2%-ном крахмальном растворе из расчета 0,1 мл/10 г веса однократно. Контрольным животным вводили эквиобъемное количество 2%-ного крахмального раствора. За животными вели наблюдение в течение 14 дней, фиксируя поведение, интенсивность и характер двигательной активности, наличие и характер судорог, координацию движений, тонус скелетной мускулатуры, реакции на тактильные, звуковые и световые раздражители, частоту и глубину дыхательных движений, ритм сердечных сокращений, состояние волосяного и кожного покрова, окраску видимых слизистых оболочек, потребление воды и пищи, изменение массы тела [6].
Гипогликемическую активность изучали на модели аллоксанового сахарного диабета, который моделировали внутрибрюшинным введением аллоксана тригидрата («Alfa Aesar®») в дозе 170 мг/кг [6]. Опыты выполнены на белых нелинейных крысах обоего пола массой 220–260 г. Животных лишали пищи за 16 ч до опыта и на время его проведения. Эксперименту подвергали животных, у которых развивалась острая гипергликемия через 72 ч после введения диабетогена. Исследуемые соединения 1а,б; 2в,г,и-н и субстанцию препарата сравнения – метформина гидрохлорид (ОАО «Фармакон») [3] вводили перорально крысам с аллоксановым сахарным диабетом в дозе 50 мг/кг в виде взвеси в 2%-ном крахмальном растворе. Концентрацию глюкозы в крови животных определяли с помощью глюкометра Сателлит® экспресс (ООО «Компания «ЭЛТА») до введения исследуемых веществ и через 120 мин после начала эксперимента. Результаты представлены в таблице 2 и рисунке 1.
Эксперименты проводились в соответствии с международными этическими и научными стандартами проведения исследований на животных [6]. Достоверность различий между группами оценивали с помощью методов параметрической статистики (t-критерий Стьюдента). Различия между выборками считали значимыми при p ≤ 0,05.
Результаты исследования и их обсуждение
Согласно полученным результатам (см. табл. 1) в спектре фармакологической активности изучаемых соединений с наибольшей вероятностью соединения 1а,б будут обладать сахароснижающей, противовирусной и антигельминтной активностью. У соединений 2а-р вероятно проявление противовирусной, антидиабетической активности, а также возможное использование при нарушениях психической деятельности и для лечения диабетической нефропатии. Из побочных эффектов наиболее вероятно проявление судорог и психических расстройств.
Таблица 1
Результаты анализа соединений в системе PASS
|
Шифр соединения |
Прогнозируемая активность |
Прогнозируемые неблагоприятные эффекты |
|
1а |
Фибринолитическая, ингибитор гастрина, антигельминтная, активатор инсулина, стимулятор эритропоэза |
Психозы, гематурия, цианоз, депрессия, аллергический дерматит |
|
1б |
Активатор инсулина, противовирусная (аденовирус), уменьшение раздражения слизистой глаз, антидиабетическая (тип 2) |
Психозы, гематурия, цианоз, депрессия, аллергический дерматит |
|
2а |
Ретинопротекторная, лечение возрастной дегенерации макулы (желтого пятна), лечение диабетической нефропатии, антидиабетическая (тип 2) |
Судороги, психозы, гипокальцемия, галакторея, мышечная слабость |
|
2б |
Антиневротическая, активатор кальциевых каналов, активатор инсулина, уменьшение раздражения слизистой глаз |
Судороги, экстрапирамидальное влияние, галакторея, полиорганная недостаточность |
|
2в |
Активатор инсулина, противовирусная (аденовирус), уменьшение раздражения слизистой глаз, антидиабетическая (тип 2) |
Судороги, психозы, галакторея, цианоз, гипокальцемия |
|
2г |
Лечение диабетической нефропатии, ингибитор входа вируса, антидиабетическая (тип 2), ингибитор MDM2 (противоопухолевая) |
Судороги, тремор, гипокальцемия, психозы, желудочно-кишечные кровотечения |
|
2д |
Противовирусная (вирус гриппа), ингибитор ГАМК-трансаминазы, против Helicobacter pylori, лечение диабетической нефропатии |
Судороги, психозы, галакторея, мышечная слабость, потеря веса |
|
2е |
Активатор инсулина, противовирусная (аденовирус), уменьшение раздражения слизистой глаз, антидиабетическая (тип 2) |
Психозы, гематурия, цианоз, депрессия, аллергический дерматит |
|
2ж |
Фибринолитическая, ингибитор гастрина, антигельминтная, активатор инсулина, стимулятор эритропоэза |
Психозы, гематурия, цианоз, депрессия, аллергический дерматит |
|
2з |
Ретинопротекторная, лечение возрастной дегенерации макулы (желтого пятна), лечение диабетической нефропатии, антидиабетическая (тип 2) |
Судороги, психозы, гипокальцемия, галакторея, мышечная слабость |
|
2и |
Активатор инсулина, противовирусная (аденовирус), уменьшение раздражения слизистой глаз, антидиабетическая (тип 2) |
Судороги, экстрапирамидальное влияние, галакторея, полиорганная недостаточность |
|
2к |
Антиневротическая, активатор инсулина, активатор кальциевых каналов, уменьшение раздражения слизистой глаз |
Психозы, гематурия, цианоз, депрессия, аллергический дерматит |
|
2л |
Фибринолитическая, активатор инсулина, ингибитор гастрина, антигельминтная, стимулятор эритропоэза |
Психозы, гематурия, цианоз, депрессия, аллергический дерматит |
|
2м |
Лечение диабетической нефропатии, антидиабетическая (тип 2), ретинопротекторная, лечение возрастной дегенерации макулы (желтого пятна), |
Судороги, психозы, гипокальцемия, галакторея, мышечная слабость |
|
2н |
Антиневротическая, активатор инсулина, активатор кальциевых каналов, уменьшение раздражения слизистой глаз |
Судороги, экстрапирамидальное влияние, галакторея, полиорганная недостаточность |
|
2о |
Противовирусная (аденовирус), уменьшение раздражения слизистой глаз, антидиабетическая (тип 2) |
Психозы, гематурия, цианоз, депрессия, аллергический дерматит |
|
2п |
Антиневротическая, активатор кальциевых каналов, активатор инсулина, уменьшение раздражения слизистой глаз |
Судороги, экстрапирамидальное влияние, галакторея, полиорганная недостаточность |
|
2р |
Противовирусная (аденовирус), уменьшение раздражения слизистой глаз, антидиабетическая (тип 2) |
Психозы, гематурия, цианоз, депрессия, аллергический дерматит |
Нами установлено, что изученные соединения обладают высоким профилем безопасности (LD50 > 1350 мг/кг) и ориентировочно могут быть отнесены к четвертому классу опасности (ГОСТ Р 53856-2010) [1]. Общее состояние, внешний вид, реакция на внешние раздражители экспериментальных мышей в течение всего наблюдения являются удовлетворительными и не отличаются от контрольной группы животных. Следует отметить, что токсичность полученных соединений ниже, чем у препарата сравнения – метформина (LD50 = 1250 мг/кг).
Исследование гипогликемической активности показало, что сахароснижающим действием обладает соединение 1б, а вещества 1а, 2г, 2и достоверно повышают уровень сахара в крови экспериментальных животных, что может быть вызвано стимулированием выработки инсулиназы (см. табл. 2 и рис. 1). Выявлено, что в ряду 3-иминофуранонов (1а,б) при введении электроноакцепторного радикала в ароильный заместитель у соединения 1б происходит усиление гипогликемических свойств. Среди продуктов раскрытия 2в,г,и-н отмечено незначительное снижение уровня глюкозы в крови лабораторных животных.
Таблица 2
Гипогликемическая активность соединений
|
№ |
Уровень глюкозы, ммоль/л |
% торможения гипергликемии через 120 мин |
|
|
0 мин |
120 мин |
||
|
1а |
8,7±0,4 |
13,9±0,9 |
-60,1±3,7***1***2 |
|
1б |
17,7±0,4 |
13,3±0,3 |
25,0±1,5***1***2 |
|
2в |
15,4±1,2 |
13,4±1,4 |
13,0±4,3***2 |
|
2г |
16,1±1,7 |
21,3±1,5 |
-31,9±9,3*1***2 |
|
2и |
8,6±0,5 |
11,2±1,6 |
-30,8±12,2*1**2 |
|
2к |
26,8±1,4 |
25,7±2,3 |
4,0±11,6**2 |
|
2л |
17,7±3,5 |
17,2±3,1 |
2,7±13,7*2 |
|
2м |
13,7±2,4 |
14,1±3,4 |
-3,0±9,5**2 |
|
2н |
20,7±1,5 |
19±0,5 |
8,4±5,2***2 |
|
Контроль (алл.д.) |
19,6±0,8 |
19,1±0,9 |
2,6±0,7 |
|
Метформин |
18,8±0,9 |
9,2±0,8 |
51,8±2,2***1 |
Примечание: *=p<0,05, **=p<0,01, ***=p<0,001; 1 – по сравнению с контролем (аллоксановый сахарный диабет); 2 – по сравнению с метформином
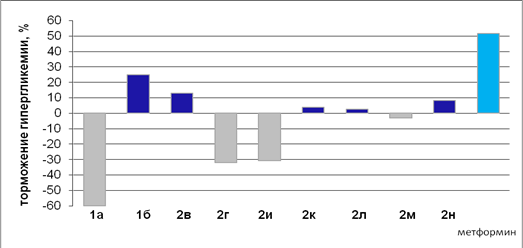
Рис. 1. Гипогликемическая активность исследуемых соединений
Выводы
1. У исследованных производных 2,4-диоксобутановых кислот отмечена более низкая токсичность, чем у препарата сравнения метформина.
2. У продуктов раскрытия 3-иминофуранонов выраженной гипогликемической активности не выявлено.
3. Введение электроноакцепторного заместителя в ароильный фрагмент 3-иминофуранонов приводит к усилению гипогликемических свойств, что делает перспективным их дальнейшее изучение.
Работа выполнена при финансовой поддержке РФФИ (проект № 14-03-96016 р_урал_а).
Рецензенты:
Вихарева Е.В., д.фарм.н., профессор, заведующая кафедрой аналитической химии ГБОУ ВПО «Пермской государственной фармацевтической академии», г. Пермь;
Ярыгина Т.И., д.фарм.н., профессор, профессор кафедры фармацевтической химии ФОО ГБОУ ВПО «Пермской государственной фармацевтической академии», г. Пермь.
Библиографическая ссылка
Кожухарь В.Ю., Пулина Н.А., Юшкова Т.А., Рубцов А.Е., Краснова А.И. ТЕОРЕТИЧЕСКОЕ ОБОСНОВАНИЕ НЕКОТОРЫХ ФАРМАКОЛОГИЧЕСКИХ СВОЙСТВ И ИЗУЧЕНИЕ ГИПОГЛИКЕМИЧЕСКОЙ АКТИВНОСТИ ПРОИЗВОДНЫХ 2,4-ДИОКСОБУТАНОВЫХ КИСЛОТ // Современные проблемы науки и образования. 2015. № 5. ;URL: https://science-education.ru/en/article/view?id=22097 (дата обращения: 24.04.2026).



