Производные 1Н-пиримидин-4-она являются перспективной группой биологически активных соединений [1; 3]. Обладая широким спектром фармакологических свойств, соединения данной группы при этом практически нетоксичны [2]. Ранее нами были получены и исследованы производные 1,3-диазинона-4, обладающие противовоспалительной активностью [6; 7]. В продолжение исследований, посвященных поиску новых НПВС в ряду производных 1,3-диазинона-4 [4; 8], нами было изучено влияние заместителей во втором положении ядра 4-оксопиримидина на величину противовоспалительной активности 2-винилензамещенных производных 4-(2,6-диметил-4-оксо-5-фенил-4Н-пиримидин-1-ил)-бензсульфамида.
Цель исследования
Фармакологический скрининг противовоспалительной активности и выявление взаимосвязи структура – биологическое действие в ряду серосодержащих 2-винилензамещенных производных 1Н-пиримидин-4-она.
Материалы и методы
Исследование противовоспалительной активности соединений проводилось на модели «ватная гранулема», на крысах–самках линии Wistar массой 200-250 г, содержавшихся в стандартных условиях вивария со свободным доступом к воде и пище. Исследуемые соединения вводились животным в дозе 50 мг/кг перорально через зонд в виде суспензии с твином-80. Животных вводили в состояние хлоралгидратного наркоза (доза 350 мг/кг), в области спины выстригалась шерсть. В асептических условиях под кожу каждого животного вшивался стерильный ватный шарик массой 15 мг. В течение 7 дней животным 1 раз в сутки вводили исследуемые соединения. Контрольная группа получала физиологический раствор. В качестве препарата сравнения использовали диклофенак в дозе, в пересчете соответствующей суточной дозе для человека. Подопытных животных разделили на 10 групп по 6 особей в каждой: животным групп 1–8 вводили исследуемые вещества, животные 9-й группы получали препарат сравнения – диклофенак, 10-я группа – контрольная. На восьмой день опыта ватные шарики с образовавшейся вокруг них грануляционной тканью извлекались, взвешивались, а затем высушивались до постоянной массы при 60–65 °С. Величину экссудации определяли по разнице масс (мг) извлеченного шарика до и после высушивания, уровень пролиферации – по разнице в массе (мг) высушенного шарика с его исходной массы (15 мг) [5].
Для построения модели прогноза противовоспалительной активности использовали программу TEST (Toxicity Estimation Software Tool), позволяющую получить информацию о 799 молекулярных дескрипторах. Программа является бесплатной и находится в открытом доступе на сайте Управления по охране окружающей среды (http://www.epa.gov/nrmrl/std/qsar/qsar.html).
Результаты работы и их обсуждение
По итогам исследования противовоспалительной активности на модели «ватная гранулема» были получены следующие результаты (табл. 1).
Таблица 1
Результаты определения противовоспалительной активности 2-винилензамещенных производных 4-(2,6-диметил-4-оксо-5-фенил-4Н-пиримидин-1-ил)-бензсульфамида на модели «ватная гранулема»
|
Экссудация |
Пролиферация |
|
|
Контроль |
263.50±5.25## |
65.83±1.89## |
|
Диклофенак |
186.00±5.60** -29.4%<PK |
36.56±1.12** -52.4%<PK |
|
1 |
251.17±6.01*## -4.7%<PK +35.04%>PD |
56.33±2.08**## -14.43%<PK +54.08%>PD |
|
2 |
259.17±7.64## -1.6%<PK +39.34%>PD |
45.34±1.76**## -31.14%<PK +23.99%>PD |
|
3 |
185.67±7.14** -29.53%<PK -0.18%<PD |
36.67±2.35**# -44.3%<PK +0.3%>PD |
|
4 |
179.83±3.04** -31.75%<PK -3.31%<PD |
38.50±1.31**## -41.51%<PK +5.31%>PD |
|
5 |
164.83±7.22**# -37.45%<PK -11.38%<PD |
25.33±1.80**# -61.5%<PK -30.72%<PD |
|
6 |
164.67±3.20**# -37.51%<PK -11.46%<PD |
32.17±1.62** -51.13%<PK -12.01%<PD |
|
7 |
279.67±4.71*## +6.14%>PK +50.36%>PD |
45.50±2.32**## -30.88%<PK +24.45%>PD |
|
8 |
215.83±5.17*# -18.09%<PK +16.04%>PD |
33.83±1.92**# -48.61%<PK -7.47%<PD |
|
Примечания: * - достоверно относительно контроля (* - p = <0,5, ** - p = < 0,05); # - достоверно относительно препарата сравнения (# - p = < 0,5, ##- p = < 0,05); PD – процент относительно диклофенака; PK – процент относительно контроля. |
||
Из таблицы 1 видно, что все соединения проявляют противовоспалительные свойства. Соединение 3 снижает экссудацию и пролиферацию на уровне препарата-сравнения - диклофенака. Соединения 4, 5 и 6 – снижают экссудацию на 3,31; 11,38; и 11,46% достоверно относительно диклофенака. Также соединения 5 и 6 достоверно снижают и уровень пролиферации в сравнении с препаратом диклофенак на 30,72 и 12,01% соответственно. Соединения 1, 2 и 7 характеризуются более низкой противовоспалительной активностью, не превосходящей действие диклофенака.
Нами была проанализирована взаимосвязь между энергиями взаимодействия виртуальных структур с аминокислотными фрагментами активного центра фермента циклооксигеназа-2, полученными в ходе молекулярного докинга, и экспериментально выявленной величиной экссудации и пролиферации. Энергии образования лиганд-ферментного комплекса, а также разница относительно контроля, величин пролиферации и экссудации, выявленных на модели ватной гранулемы, приведены в таблице 2.
Таблица 2
Результаты молекулярного докинга и противовоспалительная активность 2-винилензамещенных производных 4-(2,6-диметил-4-оксо-5-фенил-4Н-пиримидин-1-ил)-бензсульфамида
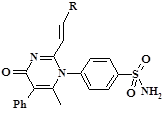
|
Исследуемый объект |
R |
Энергия докинга |
Снижение экссудации, мг |
Снижение пролиферации, мг |
|
Диклофенак |
- |
-100.33 |
77.50 |
29.27 |
|
1 |
|
-25.56 |
12.33 |
9.50 |
|
2 |
|
-58.37 |
4.33 |
20.49 |
|
3 |
|
-137.34 |
77.83 |
29.16 |
|
4 |
|
-147.93 |
83.67 |
27.33 |
|
5 |
|
-106.85 |
98.67 |
40.50 |
|
6 |
|
-65.86 |
98.83 |
33.66 |
|
7 |
|
-24.64 |
-16.17 |
20.33 |
|
8 |
|
-138.77 |
47.67 |
32.00 |
По таблице 2 видно, что полученные данные в целом согласуются с результатами молекулярного докинга.
Нами было проанализировано влияние заместителей при виниленовой группе на величину противовоспалительной активности соединений. В качестве модельного, использовали соединение 1, содержащее незамещенный стирильный радикал. Таким образом, определено, что введение метоксигруппы в п-положение (2), не оказывает значимого влияния на величину противовоспалительной активности, однако при введении в то же положение этоксигруппы (3) активность значительно увеличивается. Введение нитрогруппы (4) или галогена (5) в ароматическое кольцо также приводит к увеличению противовоспалительного действия. Среди 2-виниленгетерилпроизводных наибольшей активностью характеризуется соединение 6, содержащее фрагмент фенилпиразола. Также выяснено, что введение тиофенильного радикала (8) значительно увеличивает противовоспалительную активность, в отличие от фрагмента фурила в структуре соединения 7, характеризующегося отсутствием активности в эксперименте.
Была построена модель противовоспалительной активности в ряду синтезированных 2-винилензамещенных производных. С этой целью на основании программы TEST было получено 799 молекулярных дескрипторов для каждого из соединений, приведенных в таблице 2. Далее полученные результаты переводились в сводную таблицу программы Microsoft Excel, из которой экспортировались в демоверсию программы Molegro Data Modeller. Кроме данных по молекулярным дескрипторам, были включены результаты фармакологических исследований (таблица 2). Указанное программное обеспечение позволяет строить математические модели, такие как линейная, квадратические регрессии, регрессия по методу опорных векторов, а также модели на основании нейросети.
Расчеты проводили в двух вариантах: с учетом молекулы диклофенака натрия и без него. Во всех случаях в программе Molegro Data Modeller строилась корреляционная таблица для 2 видов биологической активности и 799 дескрипторов. В ячейках таблицы указаны коэффициенты корреляции каждого из дескрипторов со значениями биологической активности.
1.1 Диклофенак не принимался в расчет при построении модели. Из 799 дескрипторов выявлены 3, дающие наибольшие значения коэффициента корреляции (табл. 3).
Таблица 3
Выбранные дескрипторы для построения моделей противовоспалительной активности без учета диклофенака
|
№ дескриптора |
Название дескриптора в соответствии с руководством программы TEST |
R2 для экссудации |
R2 для пролиферации |
|
1 |
MDEO12 |
0,621 |
0,575 |
|
2 |
GATS6e |
0,557 |
0,167 |
|
3 |
ALOGP |
0,549 |
0,252 |
ALOGP - коэффициент разделения в системе октанол/вода, характеризующий липофильность/гидрофильность молекулы.
GATS6e - один из вариантов автокорреляции Гири. Топологический дескриптор, описывающий топологию и молекулярную геометрию молекул в 2D-плоскости.
MDEO12 - расстояние между ребрами молекулярных графов для всех первичных и вторичных атомов кислорода.
На основании выбранных дескрипторов строились указанные выше математические модели, а также проводилась кросс-валидация с исключением по одному для подтверждения достоверности модели. Наилучшие результаты были показаны для линейной и квадратической регрессий (табл. 4).
Таблица 4
Результаты построения линейной и квадратической регрессий для данных по экссудации (без учета диклофенака)
|
Модель расчета |
R2 |
R2 для валидации с исключением по одному |
|
Линейная регрессия |
0,8734 |
0,4685 |
|
Квадратическая регрессия |
0,8734 |
0,6557 |
Наилучший результат получен для квадратической регрессии с использованием 3 дескрипторов.
Модель: Экссудация = (("MDEO12"*6.97798-0.922291)*0.651049 + ("GATS6e"*12.9081-8.25551)*-0.144891 + ("ALOGP "*1.16075e-06-1.85812)*-0.632383+4.66412) / 0.0219381
Аналогичным образом строились модели для данных по пролиферации (табл. 5).
Таблица 5
Результаты построения линейной и квадратической регрессий для данных по пролиферации (без учета диклофенака)
|
Модель расчета |
R2 |
R2 для валидации с исключением по одному |
|
Линейная регрессия |
0,7985 |
0,4022 |
|
Квадратическая регрессия |
0,7985 |
0,5533 |
Наилучший результат получен для квадратической регрессии с использованием 3 дескрипторов.
Модель: Пролиферация = (("MDEO12"*6.97798-0.922291)*0.935186 + ("GATS6e"*12.9081-8.25551)*-0.819244 + ("ALOGP"*1.16075e-06-1.85812)*-0.845302+4.07431) / 0.103917
1.2 Препарат сравнения - диклофенак принимался в расчет при построении модели.
При построении корреляционной матрицы выявлены 3 дескриптора со следующими корреляциями (табл. 6).
Таблица 6
|
№ дескриптора |
Название дескриптора в соответствии с руководством программы TEST |
R2 для экссудации |
R2 для пролиферации |
|
1 |
MDEO12 |
0,634 |
0,607 |
|
2 |
MATS7v |
0,298 |
0,548 |
|
3 |
ALOGP2 |
0,395 |
0,122 |
ALOGP2 - возведенный в квадрат вышеописанный дескриптор ALOGP.
MATS7v - один из вариантов автокорреляции Морана. Топологический дескриптор, описывающий топологию и молекулярную геометрию молекул в 2D-плоскости.
На основании выбранных дескрипторов строились указанные выше математические модели, а также проводилась кросс-валидация с исключением по одному для подтверждения достоверности модели. Наилучшие результаты были показаны для линейной и квадратической регрессий (табл. 7).
Таблица 7
Результаты построения линейной и квадратической регрессий для данных по экссудации (с учетом диклофенака)
|
Модель расчета |
R2 |
R2 для валидации с исключением по одному |
|
Линейная регрессия |
0,8322 |
0,5634 |
|
Квадратическая регрессия |
0,8305 |
0,6877 |
Наилучший результат получен для квадратической регрессии с использованием 3 дескрипторов.
Модель: Экссудация = (("MDEO12"*7.08684-0.832604)*0.603674+("MATS7v"*14.1954+ 1.01058)*0.0923387 + ("ALOGP2"*0.39351-8.26949)*-0.476176+4.81382) / 0.0229615
Аналогичным образом строились модели для данных по пролиферации (табл. 8).
Таблица 8
Результаты построения линейной и квадратической регрессий для данных по пролиферации (с учетом диклофенака)
|
Модель расчета |
R2 |
R2 для валидации с исключением по одному |
|
Линейная регрессия |
0,7636 |
0,3358 |
|
Квадратическая регрессия |
0,7635 |
0,4971 |
Наилучший результат получен для квадратической регрессии с использованием 3 дескрипторов.
Модель: Пролиферация = (("MDEO12"*7.08684-0.832604)*0.512207 + ("MATS7v"*14.1954+ 1.01058)*0.448644 + ("ALOGP2"*0.39351-8.26949)*-0.0920217+4.088) / 0.106647
Выводы
Для ряда 2-винилензамещенных серосодержащих производных 1Н-пиримидин-4-она, полученных по данным осуществленного ранее молекулярного конструирования, была выявлена выраженная противовоспалительная активность. Выявлены соединения-лидеры, превосходящие препарат сравнения – диклофенак и по антиэкссудативной, и по антипролиферативной активности в тесте на модели ватной гранулемы. Выявлено влияние природы заместителя при виниленовом фрагменте исследуемых соединений на величину противовоспалительной активности. По результатам исследования была построена корреляционная матрица и модель прогноза противовоспалительной активности для 2-винилензамещенных производных 4-(2,6-диметил-4-оксо-5-фенил-4Н-пиримидин-1-ил)-бензсульфамида на основании 2D-дескрипторов методами квадратической и линейной регрессии.
Рецензенты:
Погребняк А.В., д.х.н., к.фарм.н., профессор кафедры неорганической, физической и коллоидной химии, Пятигорский медико-фармацевтический институт – филиал ГБОУ ВПО «ВолгГМУ» Минздрава России, г. Пятигорск.
Погорелый В.Е., д.б.н., профессор кафедры фармакологии с курсом клинической фармакологии, Пятигорский медико-фармацевтический институт, филиал, ГБОУ ВПО «ВолгГМУ» Минздрава России, г. Пятигорск.