Распространенность заболеваний суставов у людей неуклонно растет. Среди артритов особое положение занимают ревматические процессы, в основе патогенеза которых лежит аутоиммунное воспаление соединительной ткани оболочки суставов, которое приводит к стойкой деформации суставов, нарушению их функции, и, как правило, трудно поддается лечению. Для ревматоидного артрита характерны хроническое персистирующее течение, наличие системных проявлений, ранняя инвалидизация больных и высокий процент летальности [2,4,6]. Стандартная базисная терапия ревматических заболеваний суставов направлена на подавление активности иммунного воспалительного процесса в синовиальной ткани сустава, замедление развития заболевания, профилактику системных проявлений. Средства базисной терапии представлены такими фармакологическими группами как цитостатики, иммунодепрессанты, глюкокортикоиды, имеющими ряд серьезных побочных эффектов [9]. Поэтому поиск альтернативных малотоксичных лекарственных средств для лечения ревматических артритов представляется актуальным.
Для оценки противовоспалительного действия потенциальных противовоспалительных средств широко используется экспериментальная модель адьювантного артрита (АА), которая характеризуется развитием вторичного воспаления в суставах и окружающих мягких тканях с преобладанием пролиферативного компонента [10]. Ранее на данной модели нами впервые выявлена противовоспалительная активность нового малотоксичного аминокислотного комплекса лития, синтезированного под руководством заведующего научно-исследовательской лабораторией координационных соединений КФУ, кандидата химических наук В.Г. Штырлина, сопоставимая с эффективностью диклофенака натрия и метионина [1,8]. Это явилось предпосылкой для дальнейшего углубленного изучения его эффективности в сравнении с препаратом базисной терапии ревматоидного артрита метотрексатом.
Цель исследования
Целью настоящего исследования стала оценка эффективности аминокислотного комплекса лития в сравнении с метотрексатом при терапии адьювантного артрита у крыс.
Материалы и методы
Эксперименты проводили на 32 крысах линии Wistar обоего пола массой 180±20 грамм, содержащихся в стандартных условиях лаборатории. Исследования были одобрены локальным этическим комитетом Казанского ГМУ. Животных разделили на группы по 8 в каждой – интактную, контрольную и 2 опытные. Крысам в группах контроля и в опытных моделировали хроническое воспаление субплантарным введением в заднюю лапку 0.1 мл полного адьюванта Фрейнда (Sigma) [5]. Животным первой опытной группы с 15 по 45 день эксперимента с лечебной целью внутрибрюшинно вводили комплекс лития с метионином (LiMet) в эффективной дозе 100 мг/кг ежедневно, а второй опытной группы - метотрексат в дозе 1мг/кг 1 раз в неделю в течение 3 месяцев. Контрольным животным внутрибрюшинно инъецировали воду для инъекций в эквиобъеме. Степень выраженности отека относительно интактной лапки определяли в динамике, измеряя объем лап плетизмометром «Ub Ugo Basile 37140». Противовоспалительное действие исследуемых веществ оценивали по степени подавления отека относительно показателей контрольной группы. В ходе эксперимента наблюдали за общим состоянием, изменением массы тела и выживаемостью животных, на 10 и 18 неделе опыта делали компьютерную рентгеновскую томографию суставов аппаратом КРТ «ОКО». Снимки консультировал врач-рентгенолог, заведующий отделением РКБ Нагорных Б.П. Также, в конце эксперимента забирали кровь для общего и биохимического анализа, определяли количество лейкоцитов, эритроцитов, уровень гемоглобина, гематокрит, СОЭ, подсчитывали лейкоформулу и цветовой показатель. В сыворотке крови определяли уровень холестерина, общего белка, билирубина, активность трансаминаз печени, щелочной фосфатазы и ревматоидный фактор. Анализы крови проводили на гематологическом анализаторе «Medonic» и биохимическом анализаторе «БиАн».
Результаты обрабатывали статистически с использованием программ Microsoft Office Еxсel, применяя t-критерий Стьюдента, U-критерий Манна-Уитни, хи-квадрат Пирсона. Критерием достоверности различий служило значение p<0,05.
Результаты и их обсуждение
На 2-й день после инъекции полного адьюванта Фрейнда возникала региональная воспалительная реакция в лапке, которая нарастала к 3-му дню и проявлялась в виде покраснения, болезненности при пальпации и отека. Прирост объема лапки крыс в контрольной группе относительно интактной составил в среднем 1,05±0,04 мл и был принят за 100%. Изучаемые препараты вводили с 15 дня от начала эксперимента, ориентируясь на вторичное усиление отека в суставах до 1,2±0,02мл. К 4 неделе эксперимента у контрольных животных с моделированным адьювантным артритом наблюдали генерализацию процесса с формированием вторичных изменений в виде усиления и распространения отека на вышележащие суставы, появления пальпируемых подкожных узелков на хвосте. С 5-6 недели у животных в группах с АА наблюдали различающиеся по степени выраженности региональные вторичные изменения в виде деформации и ограничения движения в мелких суставах стоп, голеностопных, коленных и тазобедренных суставах с сохранением отека лапок в контроле, зафиксированном плетизмометрически (Рисунок 1).
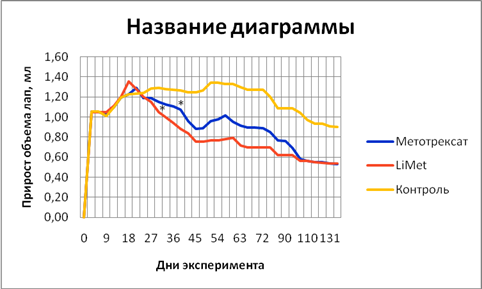
Рис.1. Динамика прироста объема лап контрольных и опытных крыс с адьювантным артритом; * – далее различия достоверны по отношению к контролю (p<0,05).
В разные сроки от начала лечения метотрексат и LiMet подавляли воспалительный отек в лапах крыс. (Рисунок 2).
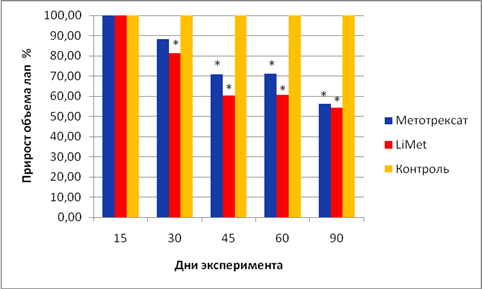
Рис. 2. Степень подавления отека лап крыс с адьювантным артритом, леченых LiMet и метотрексатом, в процентном отношении к контролю, взятому за 100%; * - различия с контролем достоверны (p<0,05).
Развитие достоверного противовоспалительного эффекта при терапии метотрексатом наблюдалось через 3 недели терапии (39 день опыта), когда метотрексат подавлял отек на 19,14%. Лечебный эффект LiMet проявился через 2 недели терапии (30 день опыта), когда подавление отека составило 18,76% (p<0,05) по сравнению с контролем. Противовоспалительная активность LiMet в конце 4 недели терапии (45 день опыта) составила 39,53%, а метотрексата 29,29%. После завершения 3 месячного курса терапии метотрексатом (103 день опыта) выраженность воспалительного отека у животных в данной группе уменьшилась на 43,85% по сравнению с контролем. Аминокислотный комплекс лития на этом сроке оказывал аналогичное действие, достоверно подавляя отек на 45,60%.
Проведенная компьютерная рентгеновская томография выявила у контрольных животных с АА подвывихи проксимальных фаланговых суставов, выраженную изъеденность по суставной поверхности коленных и голеностопных суставов, сужение суставных щелей пястнофаланговых суставов, крупные эрозии в дистальных отделах бедренной кости, отек мягких тканей до уровня тазобедренного сустава по сравнению с интактными животными (рисунок 3А, Б).
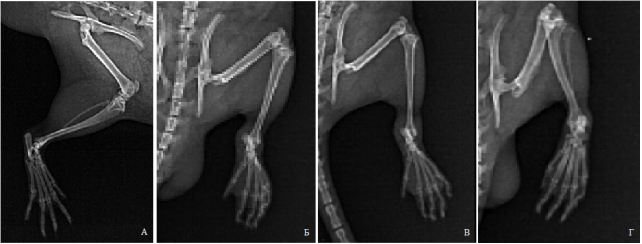
Рис.3. КРТ суставов задней лапы у крыс: А) интактная; Б) контрольная (АА без терапии); В) опытная (терапия АА метотрексатом); Г) опытная (терапия АА LiMet)
Изменения на рентгеновских снимках указывают на патологический процесс в костях и суставах лап у животных с АА, характерный для ревматических поражений суставов кистей и стоп у человека [7]. В группе животных, леченых метотрексатом и аминокислотным комплексом лития, отсутствовали сужение суставных щелей и подвывихи суставов, однако имелись единичные кистовидные просветления костей и эрозии суставных поверхностей. Отек мягких тканей распространялся в группе метотрексата и LiMet до коленного сустава (Рисунок 3 В, Г).
В ходе эксперимента у контрольных животных изменения в суставах сопровождались некротизацией кожи больных лапок с выделением серозно-геморрагической жидкости, снижением прироста массы тела на 63% к концу опыта и гибелью животных. У крыс, получавших терапию метотрексатом, не наблюдались некрозы на коже лапок, однако отмечалось поредение шерстяного покрова со 2 недели терапии, с восстановлением через 1 месяц после отмены препарата. Животные, получавшие лечение аминокислотным комплексом лития, не имели некрозов кожи больных лапок, по состоянию шерстяного покрова и прибавки веса они не отличались от интактных животных, что указывает на отсутствие общетоксического действия LiMet (Рисунок 4).
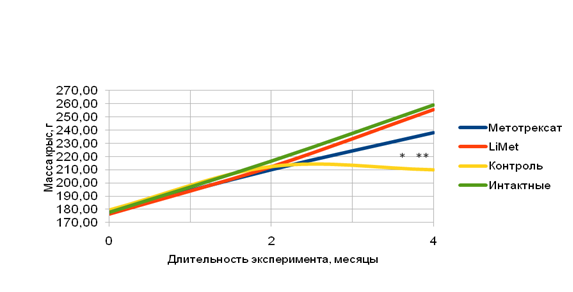
Рис.4. Динамика изменения массы тела крыс в группах.
P<0,05 * - к интактным животным, ** - к LiMet
При анализе показателей крови контрольных животных выявлено достоверное увеличение СОЭ, общего числа лейкоцитов и процентного содержания эозинофилов, палочкоядерных и сегментоядерных нейтрофилов, уменьшение относительного содержания лимфоцитов и моноцитов, снижение гемоглобина, гематокрита по сравнению показателями крыс интактной группы. Результаты указывают на сохраняющиеся воспалительные изменения в крови у крыс контрольной группы через 18 недель после моделирования АА, а также на типичное для длительно протекающего РА системное проявление заболевания в виде анемии [2,4,6,9]. Метотрексат корригировал анемию, лейкоцитоз, эозинофилию и лимфоцитопению, повышение СОЭ, сопровождающие течение АА, однако, полностью не устранял моноцитопению и палочкоядерный нейтрофилез. Все показатели периферической крови крыс, после терапии литиевым комплексом метионина, в конце эксперимента статистически не отличались от показателей интактной группы (Таблица 1).
Таблица 1
Состояние периферической крови крыс в конце эксперимента
|
Показатель крови |
Интактные |
АА контроль вода стерильная в/б 1 месяц |
Метотрексат 1 мг/кг в/б 1 раз в неделю 3 месяца |
LiMet 100 мг/кг 1 раз в день 1 месяц |
|
Эритроциты ×1012/л |
7,08±0,51 |
6,67±0,24 |
7,36±0,25** |
7,53±0,46** |
|
Гемоглобин г/л |
141,83±6,08 |
122,50±4,50* |
137,25±4,57** |
146,67±5,65**/*** |
|
Цветовой показатель |
0,60±0,03 |
0,55±0,26 |
0,56±0,24 |
0,58±0,02 |
|
Гематокрит % |
42,90±1,95 |
37,30±1,20* |
39,93±1,24*/** |
42,00±1,30**/*** |
|
Лейкоциты ×109/л |
6,98±1,60 |
13,25±1,55 * |
6,76±2,32 ** |
6,18±1,70** |
|
Эозинофилы % |
2,50±1,52 |
5,00±0,00 * |
3,50±1,29 |
3,17±1,60** |
|
Палочко- ядерные нейтрофилы % |
1,33±0,52 |
9,00±1,00* |
6,25±3,10* |
2,00±0,89 ** |
|
Сегменто -ядерные нейтрофилы % |
20,50±2,88 |
45,67±5,03* |
21,00±4,16 ** |
17,50±3,27 ** |
|
Лимфоциты % |
59,83±4,71 |
36,67±6,51 * |
60,50±5,51 ** |
65,67±7,71** |
|
Моноциты % |
15,83±1,17 |
3,67±0,58 * |
8,75±1,50*/** |
11,67±3,27*/** |
|
СОЭ (мм/ч) |
1,00±0,00 |
10,00±0,00* |
3,00±0,82 ** |
1,33±0,52 ** |
*- p<0,05 по сравнению с интактной группой/ **с контролем/***с метотрексатом
Биохимический анализ крови показал наличие ревматоидного фактора в крови крыс
контрольной группы, а в группах интактных и леченых животных его отсутствие. В конце эксперимента показатели общего белка, холестерина, билирубина, активности трансаминаз печени во всех опытных группах были в пределах физиологических норм. В группе нелеченых животных наблюдалось достоверное снижение уровня щелочной фосфатазы до 46.33±2.84 Ед/л по сравнению с показателями интактных животных (84.17±16.68Ед/л), что можно расценивать как признак анемии или истощения организма [3].
Развитие АА во всех группах сопровождалось гибелью животных. Основная масса животных погибла с 54 по 63 день в период обострения заболевания. К 90 дню опыта в контроле погибло 50% животных, в группе метотрексата — 37,5%, а в группе крыс, получавших терапию литиевым комплексом метионина, – 12.5%. В конце эксперимента гибель животных в контрольной группе составила 67,5% относительно интактной группы, в опытной группе, получавшей препарат сравнения метотрексат – 37,5%, а литиевый комплекс метионина – 12,5% (Таблица 2).
Таблица 2
Выживаемость животных в группах на разных сроках эксперимента
|
Дни опыта |
Интактные крысы |
Крысы с моделированным адьювантным артритом |
||||||
|
Контроль (нелеченные) стерильная вода в/б |
Метотрексат 1мг/кг в/б 1 раз в 7 дней 3 месяца |
LiMet 100мг/кг в/б 1 раз в день 1 месяц |
||||||
|
Погибло/ выжило |
Выживаемость % |
Погибло/ выжило |
Выживаемость% |
Погибло/ выжило |
Выживаемость% |
Погибло/ выжило |
Выживаемость % |
|
|
1 |
0/8 |
100 |
0/8 |
100 |
0/8 |
100 |
0/8 |
100 |
|
45 |
0/8 |
100 |
1/7 |
87,5 |
1/7 |
87,5 |
0/8 |
100 |
|
90 |
0/8 |
100 |
4/4 |
50* |
3/5 |
62,5 |
1/7 |
87,5 |
|
135 |
0/8 |
100 |
5/3 |
37,5* |
3/5 |
62,5 |
1/7 |
87,5** |
* p<0,05 по сравнению с интактной группой/ **с контролем/***с метотрексатом
Заключение
Таким образом, изучаемый новый комплекс лития с метионином в дозе 100 мг/кг внутрибрюшинно ежедневно в течение 30 дней на модели адьювантного артрита у крыс проявляет противовоспалительную активность, сопоставимую с таковой метотрексата. Достоверный противовоспалительный эффект у аминокислотного комплекса лития проявляется раньше, чем у препарата сравнения. Его курсовое применение у крыс с АА предупреждает развитие вторичных изменений, характерных для вторичного аутоиммунного воспалительного процесса, снижает агрессивность его течения и защищает животных от гибели.
Рецензенты:
Бойчук С.В., д.м.н., профессор, заведующий кафедрой общей патологии ГБОУ ВПО «Казанский ГМУ», г. Казань;
Семина И.И., д.м.н., профессор, заведующий ЦНИЛ ГБОУ ВПО «Казанский ГМУ», г. Казань.



