Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
DEVELOPMENT OF TECHNIQUES DEFINITIONS GLYCINE AND SUCCINIC ACID IN TABLETS NOOTROPIC ACTION BY CAPILLARY ELECTROPHORESIS
Одной из задач при разработке нового лекарственного препарата является его стандартизация. Согласно существующим нормативным документам,количественное определение субстанции глицина проводят методом кислотно-основного титрования в неводных средах, кислоты янтарной – алкалиметрическим методом.Согласно имеющим литературным данным определение данных веществ при их совместномприсутствиине описано. При разработке способов анализа лекарственных средствпреимущественно используются физико-химические методы, к которым относится интенсивно развивающийся метод разделения сложных смесей –капиллярный электрофорез, позволяющий анализировать ионные и нейтральные компоненты различной природы с высокой экспрессностью и уникальной эффективностью[1,7].На сегодняшний день известен ряд методик количественного определения глицина и кислоты янтарной методом капиллярного электрофореза, но методикиихопределения при совместном присутствии и в присутствии других компонентов отсутствуют.
С учетом химических свойств и значений рКаглицина и кислоты янтарнойдля определения в условиях одного анализа целесообразно использовать ведущий электролит со значением рН≥9 и более, так как в этом случае оба компонента будут являться анионами и соответственно могут быть проанализированы в условиях капиллярного зонного электрофореза.
Известно, что 99,9% ионизированнойформы вещества находится при рН, превышающихрКа на 3 единицы. Ввиду того, что рКаглицина по карбоксильной группе имеет значение 2,31, а янтарной кислоты рКа1 = 3,55 и рКа2 = 5,69, то можно сказать, что при использовании буферного раствора с рН = 9 все карбоксильные группы заряжены будут по иону на 99,9% [2].
рКаглицина по алифатической аминогруппесоставляет 9,71[2] и аминогруппа будет ионизирована на 99,9% в растворах при рН менее 6,7.Ввыбранных условиях (буферный раствор с рН = 9) аминогруппа ионизирована только на 36,5%, т.е. можно предположить, что в данном электролите будет преобладать анионная форма глицина.
Цель работы
Разработка методики качественного и количественного определения глицина и кислоты янтарной в таблетках ноотропного действия с применением капиллярного электрофореза.
Материалы и методы исследования
Для исследования использовали субстанцииглицина с количественным содержанием 99,5% (WIRUD®GL10001, производитель WIRUDGmbH, Германия),кислоты янтарной с содержанием 99,7% (HuanlongFoodAdditivesCorporation, Китай), а также образцы таблеток разрабатываемого препарата ноотропного действия «Гинкготропил-форте»(экспериментальная серия от 27.11.14)[6].Сухие экстракты гинкго двулопастного и лабазника вязолистного получены нами путем сгущения жидких экстрактов 1:2 на 70% этаноле с последующей сушкой под вакуумом до влажности невыше 5%, при температуре не выше 40 ⁰С.
Работу проводили с использованием системы капиллярного электрофореза Капель 105(группа компаний Люмэкс, Россия) с кварцевым капилляром диаметром 75 мкм, общей длинной 60 см и эффективной длинной 50 см. Детектирование осуществляли спектрофотометрически придлине волны равной 200 нм в катодной области капилляра. Напряжение составляло +20 кВ, температура опыта 30°С. Ввод пробы осуществляли гидродинамически 150 мБар×с.Для подготовки капилляра и восстановления его поверхности проводили его последовательную промывку водой, 0,5 М раствором кислоты хлористоводородной, водой, 0,5 М раствором натрия гидроксида, водой и затем ведущим электролитом.В качестве ведущих электролитов в работе использовались 0,01 М боратные буферные растворы с рН 9 и 10[3].
Также оценивалось влияние приложенногов режиме анализа давления на время миграции и эффективность исследуемых веществ, используя следующие режимы: 0, 10, 20, 30 мБар.
Методика:около 0,2 г (точная навеска) массы растертых таблеток помещали в мерную колбу вместимостью 100 мл, растворяли в небольшом количестве воды очищенной до полного растворения, затем доводили объем раствора до метки тем же растворителем и перемешивали. 1 мл полученного раствора центрифугировали в течении 5 минут при 8000мин-1 и подвергали анализу, прикладывая по ходу эксперимента давление 10 мБар.Параллельно вводили пробы растворов стандартных образцов глицина и кислоты янтарной. Расчет содержания глицина и кислоты янтарной проводили по формуле:
![]()
![]() – площадь исследуемого вещества;
– площадь исследуемого вещества;
![]() – площадь стандартного образца;
– площадь стандартного образца;
![]() – навескастандартного образца, взятого для
анализа, г;
– навескастандартного образца, взятого для
анализа, г;
![]() – навеска испытуемого образца, взятого для
анализа, г;
– навеска испытуемого образца, взятого для
анализа, г;
![]() – средняя масса таблеток, г;
– средняя масса таблеток, г;
![]() –объем мерной колбы, используемые для
приготовления растворов, мл;
–объем мерной колбы, используемые для
приготовления растворов, мл;
![]() – объем аликвоты, взятой для анализа, мл.
– объем аликвоты, взятой для анализа, мл.
Приготовление растворов стандартных образцов. Точные навески глицина (около 0,1000г), кислоты янтарной (около 0,0200 г) помещали в мерную колбу вместимостью 100 мл и далее поступали как описано в вышеприведенной методике.Смесь кислот готовили из полученных растворов,смешивая их в одинаковой пропорции и подвергали анализу.
Приготовление модельных смесей таблеток
Модельная смесь таблеток состоит изглицина (около 0,1000 г), кислоты янтарной (около 0,0200 г), экстракта гинкго двулопастного сухого (около 0,0300г),экстракта лабазника вязолистного сухого (около0,0300 г),аспасвита (около 0,0040 г), полипласдон XL 10 (около 0,0260 г), кальция стеарата (около 0,0020 г), коллидона 90 (около 0,0025 г).
Модельная смесь таблеток без глицина и кислоты янтарной состоит из компонентов, представленных выше, за исключением глицина и кислоты янтарной соответственно.
Результаты исследований и их обсуждение
В ходе эксперимента было установлено, чтоэлектролит с рН 9 является оптимальным для анализа компонентов. Время миграции глицина составляет 4,5 минуты, кислоты янтарной – 12 минут (рис.1). Увеличение рН электролита до 10 нецелесообразно в связи со значительным увеличением времени миграции янтарной кислоты (при рН 10 время миграции составляет 19 минут), а также потерей эффективности анализируемых веществ (табл.1) [3].
В предложенных условиях был проанализирован раствор смеси СОглицина и кислоты янтарной при совместном присутствии.
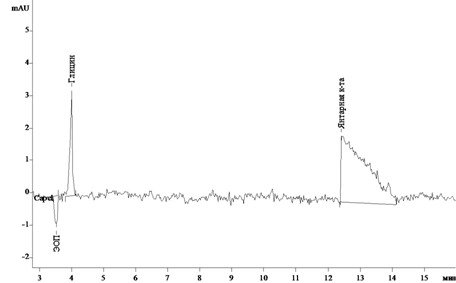
Рис.1.Электрофореграмма раствора глицина и кислоты янтарной
Далее в разработанных условиях было изучено влияние режима давления в процессе анализа на время миграции и эффективность глицина и кислоты янтарной при совместном присутствии (табл. 1).
Как следует из таблицы 1 в качестве оптимального, следует использовать давление равное 10 мБар, обеспечивающее наилучшие параметры эффективности при приемлемых значениях времени миграции веществ.
Таблица 1
Выбор оптимальных условий анализа глицина и кислоты янтарной при совместном присутствии
|
Условия анализа |
Глицин |
Кислота янтарная |
||
|
t, мин. |
N |
t, мин. |
N |
|
|
Боратный буферный раствор (рН = 9,0) |
4,42 |
10241 |
12,10 |
2450 |
|
Боратный буферный раствор (рН = 10) |
5,12 |
2192 |
18,87 |
1914 |
|
Боратный буферный раствор (рН = 9,0 + 10 мБар) |
3,5 |
12040 |
8,92 |
14669 |
|
Боратный буферный раствор (рН = 9,0 + 20 мБар) |
3,1 |
14390 |
6,38 |
9308 |
|
Боратный буферный раствор (рН = 9,0 + 30 мБар) |
2,53 |
12012 |
5,03 |
6173 |
Предварительно на модельной смеси таблеток изучиливлияние биологически активных соединений сухих экстрактов гинкго двулопастного и лабазника вязолистногона определение глицина и кислоты янтарной. С этой целью сравнивали электрофореграммырастворов суммы сухих экстрактов и суммы глицинаи кислоты янтарной. Было установлено, что присутствующие в экстрактах гинкго и лабазника биологически активные вещества (БАВ)и вспомогательные вещества таблетокне мешают определению глицина и кислоты янтарной(рис. 2 и 3).
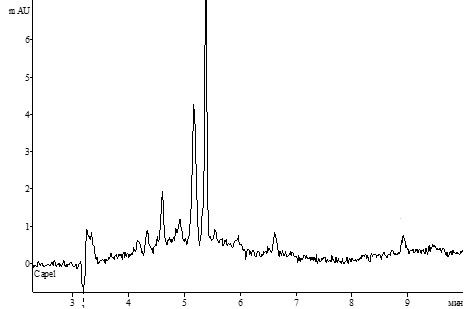
Рис.2. Электрофореграмма модельной смеси без глицина и кислоты янтарной
Кроме того, на электрофореграмме раствора модельной смеси таблетокисследуемыекислотыполностьюразделеныс другими компонентами пробы (рис.3).
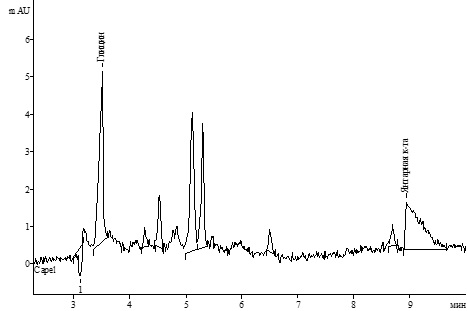
Рис.3. Электрофореграммамодельной смеси таблеток
Проведенные исследования позволили нам предложить методику идентификации глицина и кислоты янтарной путем сравнения времен миграцииглицина и кислоты янтарной на электрофореграммах раствора таблеток и соответствующих стандартных образцов.К качественным результатам относится определение идентичности компонента пробы внешнему стандартному веществу по времени появления соответствующего пика [5].В связи сэтим проведена предварительная статистическая обработка по даннымвремени миграциис помощью программы MSExcel. Полученные данные свидетельствуют о достаточной степени надежности (достоверности) обнаружения глицина и кислоты янтарной(табл.2).
Таблица 2
Статистическая обработка данных времени миграции глицина и кислоты янтарной
|
Глицин |
Кислота янтарная |
||
|
Время миграции (t), мин |
Метрологические характеристики |
Время миграции (t), мин |
Метрологические характеристики |
|
3,35 3,32 3,35 3,33 3,37 3,34 |
SD=0,018 RSD=0,52% |
7,68 7,78 7,93 8,13 8,18 8,10 |
SD=0,204 RSD=2,56% |
В оптимальных условиях анализа было проведено количественное определение глицина и кислоты янтарной в экспериментальной серии таблеток «Гинкготропил-форте». Результаты количественного определения глицина и кислоты янтарной приведены в табл.3.
Таблица 3
Результаты количественного определения глицина и кислоты янтарной в таблетках экспериментальной серии от 27.11.14
|
Масса таблеток, г |
Глицин |
Кислота янтарная |
||||
|
Sx |
Х, г/табл |
Характеристики |
Sx |
Х, г/табл |
Характеристики |
|
|
0,2131 0,2096 0,2109 0,2137 0,2082 0,2090 |
22,97 22,67 22,38 22,83 22,15 22,19 |
0,097 0,097 0,096 0,097 0,098 0,098 |
Хср= 0,097 г/табл. SD = 0,001 RSD= 0,77% |
25,06 24,98 26,34 26,28 25,95 26,39 |
0,019 0,019 0,020 0,020 0,021 0,020 |
Хср= 0,020 г/табл. SD = 0,001 RSD= 3,79% |
Полученные данные свидетельствуют о приемлемойвоспроизводимости результатов анализа.
Заключение
Установлены оптимальные условия и разработана методика качественного и количественного определения глицина и кислоты янтарной при совместном присутствии в разрабатываемом препарате «Гинкготропил-форте» с использованием капиллярного электрофореза. Относительное стандартное отклонение результатов количественного определения не превышает 1 % для глицина и 4% для кислоты янтарной.
Рецензенты:Лазарян Д. С., д.фарм.н., профессор,зав. кафедрой фармацевтической и токсикологическойхимии ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск;
Кодониди И. П., д.фарм.н., доцент кафедры органической химии ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Библиографическая ссылка
Крылов Н.Н., Сенченко С.П., Компанцева Е.В., Шевченко А.М. РАЗРАБОТКА МЕТОДИКИ ОПРЕДЕЛЕНИЯ ГЛИЦИНА И КИСЛОТЫ ЯНТАРНОЙ В ТАБЛЕТКАХ НООТРОПНОГО ДЕЙСТВИЯ МЕТОДОМ КАПИЛЛЯРНОГО ЭЛЕКТРОФОРЕЗА // Современные проблемы науки и образования. 2015. № 4. ;URL: https://science-education.ru/en/article/view?id=20954 (дата обращения: 12.05.2026).



