Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
MORPHOLOGICAL CHANGES IN THE INNER NUCLEAR LAYER NEURONS AS A RESULT OF THE PHOTOINDUCED RETINAL DAMAGE
Цель исследования
Изучить морфологические и ультраструктурные изменения нейронов внутреннего ядерного слоя сетчатки крыс при воздействии света высокой интенсивности в динамике.
Материал и методы исследования
Изучены сетчатки 40 беспородных половозрелых белых крыс-самцов. На крыс 1-й группы (n=20) воздействовали в течение 6 часов люминесцентными лампами ЛБ-40, имеющими максимум излучения в желто-зеленой области спектра. Для освещения использовалась специальная установка из прямоугольных рефлекторов с вмонтированными в них лампами, освещающая клетку с 5 сторон. Освещенность животных составляла 6000 лк. В качестве контрольной группы использовали интактных крыс (n=20). Все животные содержались в условиях искусственного светового режима: 12 ч день, 12 ч ночь, с интенсивностью дневного освещения 25 лк. Декапитацию производили под эфирным наркозом через 1, 7, 14, 30 сут после светового воздействия, в аналогичные сроки производили взятие контрольного материала.
Для электронной микроскопии центральные участки задней стенки глаза фиксировали в растворе, содержащем смесь 4%-ного параформальдегида и 0,5%-ного глютаральдегида на 0,2 М какодилатном буфере (рН 7,4). Материал постфиксировали в 2%-ном растворе четырехокиси осмия и заливали в эпон. Полутонкие срезы окрашивали толуидиновым синим, ультратонкие - контрастировали уранилацетатом и цитратом свинца, просматривали и фотографировали в электронном микроскопе JEM–7А. На полутонких срезах сетчатки производили подсчет пикноморфных биполярных, амакринных и горизонтальных ассоциативных нейронов на 200 соответствующих клеток. На электронных микрофотографиях внутреннего ядерного слоя определяли удельную площадь органелл ассоциативных нейронов. Измерения проводили с помощью открытой квадратной тестовой решетки с шагом 5 мм при увеличении 10000.
Статистическую обработку результатов проводили методами вариационной статистики. Для оценки достоверности различий при сравнении средних величин использовали непараметрический критерий Манна-Уитни.
Результаты исследования и их обсуждение
На 1-е сутки после светового воздействия наблюдается достоверный рост процентного содержания пикноморфных ассоциативных нейронов (рис. 1), а также клеток со светлым типом деструкции, на ультраструктурном уровне характеризующийся снижением содержания органелл. Так, удельная площадь митохондрий в таких клетках снижалась в 1,5 раза, гранулярной эндоплазматической сети в 2,3 раза, комплекса Гольджи в 1,4 раза (контроль 15,58±2,08%; 26,79±2,41%; 2,71±0,13% соответственно; р<0,05). Максимум деструктивных изменений в нейронах внутреннего ядерного слоя зарегистрирован к 7-м суткам после освещения, когда процентное содержание пикноморфных нейронов возрастает относительно контрольного значения до 21,00±1,29% (контроль 1,85±0,13%; p<0.05; рис. 1). Пик деструкции ассоциативных нейронов совпадает с очаговым выпадением наружных слоев сетчатки вследствие массовой гибели нейросенсорных клеток и пигментоцитов [2; 5].
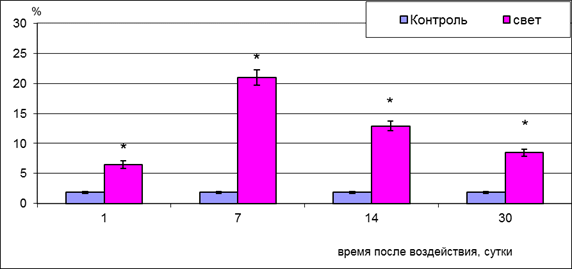
Рис. 1. Процентное содержание пикноморфных нейронов внутреннего ядерного слоя сетчатки крыс при световом воздействии
Примечание: статистически достоверные отличия (p<0.05) отмечены * - при сравнении с контролем.
Экспериментальное воздействие высокоинтенсивного света на сетчатку приводит к глубокому обесцвечиванию ретиналя и развитию процессов окисления в наружных сегментах и мембранах органелл внутренних сегментов фоторецепторов. При этом пигментоциты, находясь в тесном контакте с наружными сегментами нейросенсорных клеток, подвергаются мощной атаке свободными радикалами и при повреждении сами становятся индукторами активных форм кислорода [4]. Вероятно, срыв механизмов антиоксидантной защиты приводит к распространению свободных радикалов и продуктов пероксидации во внутренние слои сетчатки, что вызывает повреждение мембранных органелл, восприимчивых к окислению.
Активизация свободнорадикального окисления и перекисного окисления липидов вызывает также деструкцию высокомембранных структур синаптических контактов наружного сетчатого слоя. В отдельных участках сетчатки он полностью отсутствует, что прерывает трехнейронную цепь и опосредованно вызывает деструкцию нейронов внутреннего ядерного слоя. Деструкция нейронов II порядка во многом зависит от степени поражения нейросенсорных клеток и объясняется потерей синаптического входа от них и невозможностью выхода трофических факторов и медиаторов [7; 10]. На 14-30-е сутки количество пикноморфных нейронов снижается до 12,9±0,79% и 8,45±0,56% соответственно (контроль 1,85±0,13%; p<0.05). Данная динамика, возможно, связана с фагоцитозом деструктивных нейронов радиальной глией, о чем косвенно можно судить по наличию в цитоплазме радиальных глиоцитов остаточных телец (рис. 2). В эти сроки внутренний ядерный слой представлен клетками со светлым типом деструкции, а также гипертрофированными отростками радиальной глии (рис. 3), вероятно, осуществляющими защиту сохранившихся нейронов.
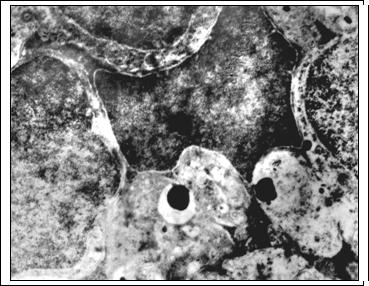
Рис. 2. Остаточные тельца в цитоплазме радиального глиоцита через 14 суток после светового воздействия. Я - ядро радиального глиоцита; О - остаточные тельца. Ув. 6500
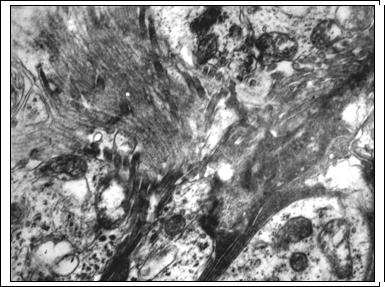
Рис. 3. Глиальная пролиферация во внутреннем ядерном слое через 14 суток после освещения. ОРГ - отростки радиальной глии; А - ассоциативные нейроны. Ув. 8000
Реакция ассоциативных нейронов и радиальных глиоцитов в ответ на световое воздействие в целом схожа с процессами, происходящими в сетчатке при различных нейродегенеративных состояниях. Процесс ремоделирования сетчатки напоминает ответ центральной нервной системы на деафферентацию или травму и включает, главным образом, гибель нейронов, миграцию глиальных популяций и неосинаптогенез [7]. Обращает на себя внимание тот факт, что распределение радиальных глиоцитов во внутреннем ядерном слое происходит неравномерно, основная часть их ядер сконцентрирована у витреального края этого слоя и находится в непосредственном контакте с телами амакринных нейронов. Отмечено, что большая часть этих глиоцитов при световом воздействии подвержена деструкции. Как известно, глия обеспечивает нормальное функционирование нейронов, а ее гибель, косвенно, инициирует деструкцию нейронов. Так, например, радиальные глиоциты участвуют в метаболизме нейротрансмиттера глутамата, который в больших концентрациях обладает нейротоксичностью и индуцирует апоптотическую гибель нейронов [3; 9].
Среди ассоциативных нейронов наиболее подвержены деструкции амакринные нейроны и наименее - горизонтальные (рис. 4). Так, количество пикноморфных амакринных нейронов на 7-е сут после светового воздействия достигает 26,6±1,26%, биполярных 17,4±0,69% и горизонтальных 13,6±1,24%, что значимо отличается от таковых в контроле (1,05±0,12%, 0,8±0,08%, 0% соответственно p<0.05).
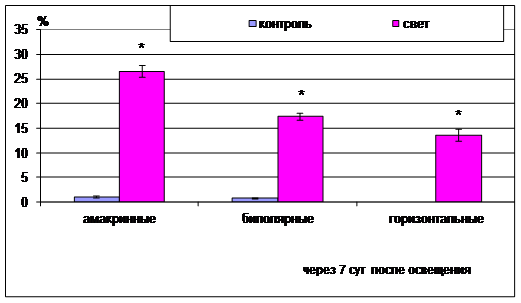
Рис. 4. Процентное содержание пикноморфных ассоциативных нейронов (амакринных, биполярных и горизонтальных) при высокоинтенсивном световом воздействии
Выраженные морфологические и функциональные изменения амакринных и биполярных нейронов с сокращением числа дендритов, прорастанием аксонов, потерей нейронами глутаматных рецепторов развиваются также и при ряде других нейродегенеративных заболеваний сетчатки. Деструкция нейросенсорных клеток на начальном этапе развития заболеваний приводит к увеличению синаптической активности в биполярных и амакринных нейронах, следствием чего является истощение и перераспределение пула нейромедиаторов [6]. Вероятно, именно увеличение функциональной активности амакринных и биполярных нейронов лежит в основе большего их повреждения при воздействии света высокой интенсивности.
Выводы
Таким образом, при световом воздействии наиболее подвержены деструктивным изменениям амакринные и наименее – горизонтальные нейроны внутреннего ядерного слоя. Максимальное содержание пикноморфных нейронов наблюдается на 7-е сутки после воздействия, одновременно с очаговым выпадением наружных слоев сетчатки. В поздние сроки содержание деструктивно измененных нейронов достоверно снижается вследствие их фагоцитоза радиальными глиоцитами.
Рецензенты:
Солонский А.В., д.м.н., руководитель лаборатории нейробиологии ФГБУ «Научно-исследовательский институт психического здоровья» СО РАМН, г. Томск.
Мустафина Л.Р., д.м.н., профессор кафедры гистологии, эмбриологии и цитологии ГОУ ВПО «Сибирский государственный медицинский университет» Минздрава России, г. Томск.
Библиографическая ссылка
Варакута Е.Ю., Логвинов С.В., Жданкина А.А., Потапов А.В., Герасимов А.В., Аникина Е.Ю., Свердева Ю.О. МОРФОЛОГИЧЕСКИЕ ИЗМЕНЕНИЯ НЕЙРОНОВ ВНУТРЕННЕГО ЯДЕРНОГО СЛОЯ ПРИ ФОТОИНДУЦИРОВАННОМ ПОВРЕЖДЕНИИ СЕТЧАТКИ // Современные проблемы науки и образования. 2015. № 3. ;URL: https://science-education.ru/en/article/view?id=20201 (дата обращения: 17.05.2026).



