Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
FUTURE PROSPECTS OF LIPOGEL (THIOCTIC ACID GEL) APPLICATION FOR RHEUMATOID ARTHRITIS
Ревматоидный артрит представляет собой аутоиммунное воспалительное заболевание суставов, в качестве центрального элемента клиники которого выступает суставной синдром воспалительного характера, который проявляется артралгией и утренней скованностью. С целью стабильного адекватного обезболивания, которое остается неизменно важной целью терапии заболевания, применяют нестероидные противовоспалительные препараты (НПВП). Однако, их длительный прием неизменно сопровождается побочными эффектами, в частности, патологией желудочно-кишечного тракта, печени, почек, нарушениями кроветворения и зрения, артериальной гипертензией, обусловленной ретенцией натрия, и другими [3]. Более того, нередко перед клиницистами встает необходимость отхода от системного приема НПВП в связи с коморбидными состояниями, к примеру, язвой желудка. При этом введение НПВП в организм в виде свечей или парентерально не снижает риска развития побочных эффектов. Решением этой проблемы, безусловно, является назначение противовоспалительных препаратов в виде мазевых, кремовых или гелевых форм, поскольку при этом достигается как высокая биодоступность в суставных и периартикулярных тканях, так и практически полное отсутствие резорбтивных побочных эффектов.
Тиоктовая кислота представляет собой амфифильное соединение с высокой антиоксидантной активностью, нашедшее клиническое применение для лечения заболеваний печени, полинейропатий, дислипидемий. Нами ранее было установлено наличие у тиоктовой кислоты противовоспалительных свойств при пероральном и местном применении [4]. На сегодняшний день в Государственном реестре лекарственных средств Минздрава России насчитывается около 40 препаратов с тиоктовой кислотой [7]. На фармацевтическом рынке она представлена преимущественно пероральными формами (таблетки, покрытые оболочкой, и капсулы по 25, 300 и 600 мг), растворами для инфузий и концентратами для их приготовления и, реже, ректальными суппозиториями (в комплексе с кокарбоксилазой и рибофлавином для комплексной терапии гипоксических и иммунодефицитных состояний, интоксикаций и гипотрофии у детей). Однако лекарственных форм для локального применения с тиоктовой кислотой в Российской Федерации не зарегистрировано. Нами совместно с технологами лекарственных средств Насыбуллиной Н.М. и Зверевой Н.М. ранее был разработан 1% гель с тиоктовой кислотой, наиболее весомым преимуществом которого явилось то, что активное вещество практически полностью высвобождается из него в течение суток [1,6]. Возможность однократного применения данного геля по сравнению с необходимостью наносить гели с НПВП 3-4 раза в сутки значительно повышает комплаенс у пациентов.
Цель исследования. Оценить влияние применения 1% геля тиоктовой кислоты в сравнении с 1% гелем диклофенака натрия на течение адъювантного артрита крыс.
Материал и методы исследования
План настоящего исследования был представлен на экспертизу и одобрен Локальным этическим комитетом Казанского государственного медицинского университета. В экспериментах использовались 66 беспородных нелинейных половозрелых крыс обоего пола в возрасте 3-5 месяцев, массой 200-250г (патоморфологическому исследованию подверглись 37 из них). Воспалительную реакцию моделировали путем субплантарного введения в правую заднюю лапу крысы 0,1мл полного адъюванта Фрейнда (ПАФ, Sigma) [5, 8]. Животные с моделированным артритом были разделены на получавших лечение 1% гелем тиоктовой кислоты, 1% гелем диклофенака натрия, гелевой основой и нелеченных. Также присутствовала интактная группа. 1% гель липоевой кислоты и 1% гель диклофенака натрия (выбранный в качестве референс-препарата в эквитоксичной дозе) наносились на обе задние лапы (в количестве 0,1мл на лапу) с 12 по 25-й дни эксперимента однократно, осторожно втирались в течение 30 секунд и покрывались защитной повязкой из пластыря с марлей.
Выраженность воспалительной реакции оценивалась на 0, 3, 6, 10, 15, 20, 25-й дни эксперимента в динамике. В качестве базового способа оценки эффективности исследуемых веществ был выбран онкометрический метод, позволяющий оценить выраженность воспалительного отека лап по объему вытесненной жидкости при комнатной температуре. Каждый замер повторялся двукратно. Верификацию данных проводили с помощью патоморфологического исследования, методология которого подробно была описана нами ранее [2].
Полученные результаты обрабатывали статистически с использованием пакета прикладных программ Statistica 6.0 для Windows с вычислением средней арифметической, ошибки средней, t-критерия Стьюдента, Т-критерия Уилкоксона, U-критерия Манна-Уитни; критерием достоверности различий явилось значение Р<0,05.
Результаты исследования и их обсуждение
Выраженный отек, развившийся в месте введения адъюванта Фрейнда в правую заднюю лапу, регистрировался уже на 3-й день и представлял собой первичную воспалительную реакцию. С течением времени первичная воспалительная реакция немного уменьшалась, но неуклонно нарастала генерализация процесса в виде воспаления суставов других лап, хвоста, изменений кожи. Это явление, названное вторичной иммунологической реакцией, оценивалось по отеку левой задней лапы и стало достоверно регистрироваться с 11-го дня эксперимента. Вторичная иммунологическая реакция, возникающая при адъювантном артрите, используется исследователями по всему миру в качестве доступной и репрезентативной модели ревматоидного артрита человека [9].
Объем лап животных контрольной группы, которым наносилась гелевая основа, не отличался от такового у животных контрольной группы, не получавших лечения, ни в динамике, ни к концу эксперимента. Нанесение гелевой основы не влияло на структуру суставов и периартикулярных тканей по сравнению с животными контрольной группы.
Влияние гелей тиоктовой кислоты и диклофенака натрия на выраженность воспаления в задних лапах крыс представлено на рисунке 1.
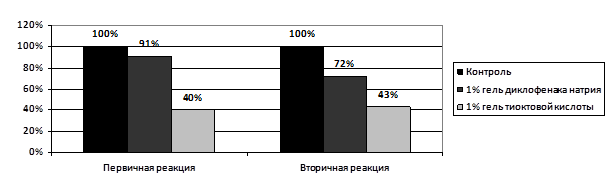
* - Р < 0,05 по сравнению с контрольной группой
** - Р < 0,05 по сравнению с группой диклофенака натрия
Рис. 1. Влияние 1% гелей тиоктовой кислоты (липогеля) и диклофенака натрия на первичную воспалительную и вторичную иммунологическую на 25-е сутки после введения адъюванта, в процентах по отношению к контролю.
Как видно из рисунка 1, нанесение геля диклофенака натрия не оказывало достоверного влияния на выраженность первичной воспалительной реакции, но уменьшало вторичную иммунологическую реакцию на 28%, что вероятно, связано с уменьшением частоты применения геля до одного раза, вместо рекомендуемых 2-3 раз в сутки. Применение 1% геля тиоктовой кислоты привело к снижению первичной воспалительной реакции на 60%, что достоверно превышало эффективность геля диклофенака натрия, а вторичной иммунологической реакции на 57%, что также достоверно превосходило эффективность референс-препарата при однократном применении в сутки.
Местное применение как диклофенака натрия, так и тиоктовой кислоты приводило к выраженному уменьшению воспаления. Однако, применение геля тиоктовой кислоты по сравнению с диклофенаком натрия имело определенные преимущества в отношении влияния на кожный покров (рисунок 2) и хрящевые структуры (рисунок 3).
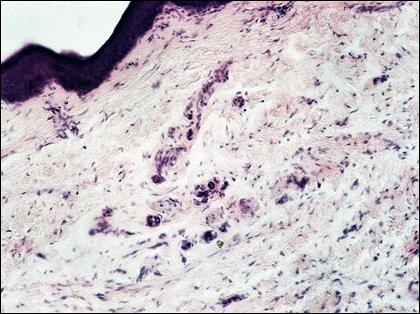
Рис. 2. Состояние кожного покрова при местном нанесении геля тиоктовой кислоты на 25-й день после введения полного адъюванта Фрейнда. Окраска гематоксилином и эозином. х 200.
Как видно из рисунка 2, при местном применении тиоктовой кислоты кожный покров имел обычную гистологическую структуру, лишь в единичных случаях в дерме сохранялись небольшие лимфогистиоцитарные инфильтраты. Как видно из рисунка 3, хрящевая поверхность сустава в группе, животных, которым наносился гель с тиоктовой кислоты, была гладкой, с четко определяемыми зонами и неизмененными хондроцитами.
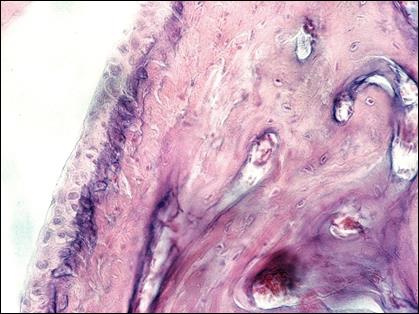
Рис. 3. Состояние хряща в результате курсового нанесения геля тиоктовой кислоты. Окраска гематоксилином и эозином. х 400.
Кроме того, в этой группе отсутствовали явления остеопороза (рисунок 4) и разрастания синовиальной оболочки с формированием паннуса (рисунок 5).
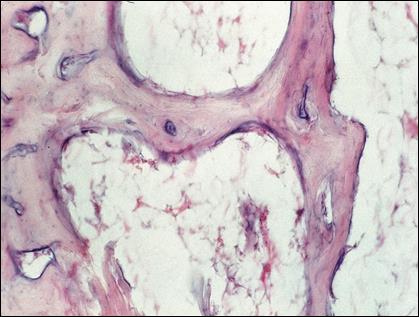
Рис. 4. Состояние костной ткани у крыс с адъювантным артритом, леченных гелем тиоктовой кислоты в течение 14 дней. Окраска гематоксилином и эозином. х 200.
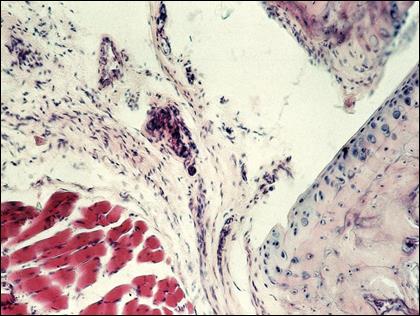
Рис. 5. Состояние синовиальной оболочки у крыс с адъювантным артритом, леченных гелем тиоктовой кислоты в течение 14 дней. Окраска гематоксилином и эозином. х 200.
Как видно из рисунка 4, подлежащая костная ткань была представлена компактной костью с наличием небольших грубоволокнистых фрагментов балочного строения. Синовиальная оболочка в целом имела нормальное гистологическое строение. Только в единичных случаях сохранялись явления умеренного отека и незначительная очаговая лимфогистиоцитарная инфильтрация (рис. 5).
Таким образом, на основании исследования морфологических образцов с окраской их гематоксилином и эозином, можно сделать вывод, что гель тиоктовой кислоты при курсовом местном применении предупреждает разрушение костной и хрящевой ткани, а также разрастание синовиальной оболочки и кожные проявления, характерные для адъювант-индуцированного артрита крыс.
Заключение
Курсовое применение 1% геля тиоктовой кислоты достоверно уменьшает отек лап, разрастание синовиальной ткани и явления остеопороза, восстанавливает структуру хряща, а также устраняет кожные проявления адъювантного артрита.
Получен патент (RU 2 519 330 C2) на изобретение «Композиция для наружного применения, обладающая противовоспалительной, анальгетической, антиревматоидной и антибактериальной активностью и способ ее получения» от 31.10.2011 года [6] и ОАО «Татхимфармпрепараты» выпущена опытная партия 1% липогеля (1% гель тиоктовой кислоты). Ожидается, что на фоне применения липогеля пациентам с ревматоидным артритом удастся, как минимум, снизить дозу принимаемых ими НПВП и значительно улучшить качество жизни, так как липогель будет обладать хорошей переносимостью, высокой эффективностью и безопасностью.
Рецензенты:
Зиганшин А.У., д.м.н., профессор, заведующий кафедрой фармакологии с курсами фармакогнозии и ботаники фармацевтического факультета ГБОУ ВПО «Казанский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Казань;
Хафизьянова Р.Х., д.м.н., профессор, профессор кафедры фармакологии ГБОУ ВПО «Казанский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Казань.
Библиографическая ссылка
Залялютдинова Л.Н., Анисимов А.Н., Иманаева А.Я., Цыплаков Д.Э., Гайнетдинова А.Н. ПЕРСПЕКТИВЫ ПРИМЕНЕНИЯ ЛИПОГЕЛЯ (1% ГЕЛЯ ТИОКТОВОЙ КИСЛОТЫ) ДЛЯ ТОПИЧЕСКОЙ ТЕРАПИИ РЕВМАТОИДНОГО АРТРИТА // Современные проблемы науки и образования. 2014. № 6. ;URL: https://science-education.ru/en/article/view?id=16849 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.16849



