Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
СLINICAL EVALUATION OF WOUND HEALING PROCESS IN THE MUCOSA OF THE ORAL CAVITY USIHG A POLYMER GRAFT
Актуальным вопросом хирургической стоматологии, в основном имплантологии и пародонтологии, а так же ортопедической и ортодонтической стоматологии является достижение функциональных и высокоэстетичных результатов, что особенно важно для, воссоздания естественной улыбки, когда между коронкой зуба и десной достигается полная гармония. Дефицит зоны прикрепленной десны, наличие рубцовых изменений, тканевой рецессии мягких тканей полостирта, опухолей и опухолевидных образований требуют хирургического лечения, от качества которого зависит эффективность комплексного лечения пациента. Контуры межзубных мягких тканей, так же как цвет, текстура и количество кератинизированной ткани, являются очень значимыми элементами эстетики как при ортопедическом лечении, так и в протезировании на имплантатах.
Результаты хирургического вмешательства в полости рта зависят от методики ведения послеоперационной раны и не всегда являются удовлетворительными. Заживление открытых раневых поверхностей происходит посредством вторичного натяжения. Результатом травматического воздействия и постоянного бактериального загрязнения раны является изменение объемов тканей в послеоперационной области и формирование деформирующей рубцовой ткани [6]. Успех зубной имплантации, высокий показатель приживления имплантатов и их функционирование, ортопедическое лечение с помощью коронок и мостовидных протезов, а также эффективность терапии при лечении воспалительных заболеваний пародонта во многом зависят от адекватного состояния мягких тканей краевого пародонта и наличия уровня прикрепленной десны [4].
В большинстве случаев после проведения хирургических вмешательств на пародонтальных карманах также не удается добиться гарантированного успеха регенерации утраченных структур [7], причем послеоперационная рецессия десны, которая отмечается в 30 - 65% случаев, создает как функциональные, так и косметические проблемы для пациентов. В частности, возникающие рецессии десны являются причиной повышенной чувствительности оголенных шеек зубов и ретенции зубного налета, который оказывается важным фактором дальнейшей потери зубодесневого прикрепления. По мнению D. Hoelscher и A. Simons (1994) [10], многие неудачи зубной имплантации напрямую связаны с проблемами мягких тканей, что может проявляться в форме послеоперационной рецессии либо гиперплазии десны, переимплантита с одновременной потерей кости в зоне прилегания к имплантату и последующего обнажения резьбы на теле имплантата [11].
Для восстановления утраченных тканей в области преддверия и маргинальной десны в стоматологии используются различные хирургические методы лечения. Наиболее распространенным и качественным является метод использования свободного небного лоскута (свободный десневой трансплантат, свободный соединительнотканный трансплантаты). Это позволяет добиться хороших результатов, однако имеет определенные недостатки, так как связано с трудностями выбора донорских участков, соответствующих необходимым требованиям и необходимостью проведения дополнительной операции в донорской области [8,9]. Использование свободного соединительнотканного трансплантата (СТТ) в пародонтологии и имплатологии незаменимо, как с функциональной, так и с эстетической точки зрения. С момента первого описания этой методики (Edel 1974), расширились показания к ее использованию, а также увеличилось количество модификаций.
В результате проводимого лечения, чаще всего страдает донорская зона, которая является источником соединительнотканного трансплантата. Период ее заживления является крайне болезненным и неприятным для пациента, поэтому в некоторых случаях хирурги продолжают применять в качестве защитной раневой повязки йодоформные турунды, что является самым доступным и дешевым методом [12]. Но имеет посредственные результаты, так как удалять ее приходится на 4-5 день, что является причиной ухудшения состояние грануляционной ткани, ее кровоточивость сохраняется до конца 2 недели, а окончательную эпителизацию раны отмечают только на 2 месяце после операции. Кроме того, йодоформная турунда у большинства пациентов вызывает неприятные вкусовые ощущения и даже тошноту с рвотой. Известно, что кроме защиты раны, повязка должна активно влиять на процессы заживления, благодаря очистке раны и созданию микроклимата, способствующего заживлению и поддержанию раны в покое [3].
Цель исследования - разработка способа послеоперационного ведения раны на слизистой оболочке полости с целью оценки течения раневого процесса и заживления раны в динамике.
Материалы и методы
В настоящее время большой интерес у нас вызывают данные об использовании синтетических материалов, которые позволяют изолировать в послеоперационном периоде донорскую область, тем самым защитить раневую поверхность и оптимизировать процесс регенерации раны. Искусственные материалы не обладают антигенной чужеродностью и позволяют закрыть любые по форме дефекты, невзирая на особенности строения и формы челюстно-лицевой области. Интраоперационная модуляция легче и занимает меньше времени, исключается возможность заражения реципиента инфекциями, трансплантат не подвергается резорбции, отторжению или некротизации. Такие материалы выпускаются промышленными предприятиями в необходимом количестве и не требуют наличия специального оборудования для заготовки и хранения [1]. Трансплантат не подвергается резорбции. Такие материалы выпускаются промышленными предприятиями в необходимом количестве и не требуют наличия специального оборудования в стационаре для заготовки и хранения [2]. Для создания перевязочного средства отвечающего требованиям полифункциональности, необходима разработка подходящей структуры перевязочного материала и технологии его получения. Вышесказанное невозможно без всестороннего исследования физико-химических, в том числе, реологических характеристик полимерных растворов и анализа влияния технологических параметров на эффективность процесса регенерации. Были разработаны основные требования, предъявляемые к искусственным препаратам: быть нетоксичным, неаллергенным, неканцерогенным; препятствовать развитию и быть барьером для проникновения инфекции; не вызывать иммунных реакций и не травмировать грануляционную ткань в ране; обладать гемостатическим и антисептическим действием; стимулировать репаративные процессы; предотвращать плазмотерапию не нарушать электролитный баланс; адсорбировать раневой экссудат, препятствовать его скоплению под покрытием; легко накладываться и сниматься без хирургических вмешательств; иметь удобную форму и легко стерилизоваться; быть дешевым и доступным; подвергаться биодеградации в ране без образования токсических продуктов; не менять своих свойств и структуры при хранении.
Наиболее распространенным в использовании в различных отраслях хирургии и в стоматологии является синтетический материал. Нами используется синтетическая полимерная мембрана «Реперен» (производится на предприятии «Репер НН» г. Н.Новгород, Россия), которая представляет собой пространственно сшитый полимер из олигомеров метакрилового ряда. Известно, что особенностью синтеза данного полимера является одностадийная технология изготовления готового изделия методом фронтальной фотополимеризации в квазизамкнутых формах, задающих геометрию и размеры формируемого изделия. Данная технология, во-первых,позволяет осуществить одностадийное производство изделия (мономер → изделие), что исключает попадание инородных примесей (в традиционных технологиях это происходит на стадии полимер → изделие). Во-вторых, технология фронтальной полимеризации с предельно малым шагом волны позволяет произвести полную полимеризацию мономера в полимер без остаточного количества, что выгодно отличает данную технологию от традиционной методики термической полимеризации (рег. удостоверение №ФС 0103200614786—06 от19.12.2006). В хирургической практике для закрытия дефектов донорской зоны на небе мы используем пластины Реперен для пластики ТМО размером 4,5х5 см с кривизной радиуса 140, толщиной 0,4 мм. Имплантаты стерилизуются окисью этилена и выпускаются в стерильной упаковке. Реперен для ТМО представляет собой мягкую, эластичную прозрачную пленку, на наружной поверхности которой нанесена сетка (ребра жесткости для предотвращения прорезывания нити при подшивании), а внутренняя поверхность ее идеально гладкая (степень шероховатости — порядка нанометров).
Методика ведения послеоперационной раны с использованием полимерной мембраны. В качестве клинического исследования нами проводилась традиционная методика забора свободного соединительнотканного трансплантата на небе, но с закрытием донорской зоны полимерной мембраной Реперен. Существенных отличий в проведении операции забора трансплантата нет. С помощью градуированного пародонтального зонда определяли необходимую длину трансплантата, изготавливали шаблон. Необходимый размер трансплантата определялся протяженностью зоны недостаточной прикрепленной десны, с учетом его дальнейшей усадки, которая считается равной 35% (Февралева А.Ю., 2007; Лапина С.Л., 2009). Под инфильтрационной анестезией с небольшим содержанием вазоконстриктора проводили забор свободного соединительнотканного трансплантата с помощью скальпеля с лезвием №15, на твердом небе от клыка до второго моляра верхней челюсти, отступя от десневого края 3-4 мм. Во время операции проводился тщательный гемостаз донорского участка (рис.1). Далее края стерильной упаковки после обработки 70% спиртом обрезают, с помощью стерильных пинцетов извлекают Реперен из упаковки. Ножницами вырезают имплантат необходимого размера и формы, укладывают на дефект в донорской области с перекрытием краев раны (рис.2) и фиксируют шовным материалом «Vicryl 5-0» на атравматичной игле узловыми швами (рис. 3).
Рис.1.Забор трансплантата
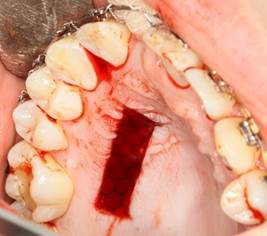
Рис. 2. Реперен уложен на дефект с перекрытием краев раны
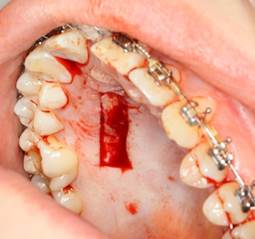
Рис. 3. Реперен фиксирован швами
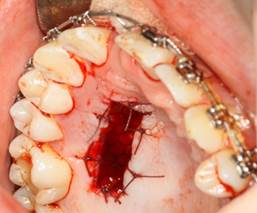
Рис. 4. 3-и сутки после операции
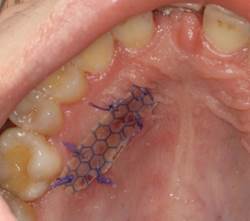
В послеоперационный период пациенту рекомендовали соблюдать гигиену полости рта и делать ротовые ванночки с физиологическим раствором после каждого приема пищи и щадящий режим питания в течение первой недели после операции. Швы, фиксирующие мембрану Реперен, снимали на 7-ые сутки.
Результаты и обсуждения
Из 33 прооперированных пациентов с использованием в послеоперационном периоде полимерного материала осложнений в виде воспалительной реакции не наблюдалось, что, по нашему мнению, связано с возможностью микродренирования раны под мембраной и возможностью ее фиксации без последующего движения по ране. Оценка клинических изменений на этапах постоперационного лечения проводилась в 1-ые, 3-и, 5-ые и 7-ы сутки. Незначительный болевой синдром у всех пациентов с использованием полимерного трансплантата проявлялся на 3-и сутки, далее увеличения интенсивности болевых ощущений не наблюдалось, как это обычно бывает при открытом ведении донорской зоны. Увеличение болевого симптома с 4 по 10 сутки при открытом ведении донорской зоны обуславливается тем, что заживление раны на небе происходит в результате вторичного натяжения, когда максимальные болевые ощущения присутствуют на этапах гранулирования раны, а стихание происходит во время эпителизации дефекта. Также мы оценивали интенсивность эпителизации под мембраной, которая на 25% была интенсивнее. Степень динамики у пациентов с использованием Реперена и при традиционном лечении разная. Сетчатая структура пластины Реперен позволяет не мешать регенерации тканей и способствует ранней эпителизации послеоперационной раны, которая стимулирует быстрое образование соединительной ткани. Обеспечивается стабильный контакт тканей, осуществляется постоянное микродренирование послеоперационного пространства, имевшие место постоянная травматизация и кровоточивость донорского участка при использовании классической методики, отсутствует при использовании пластин и, не осложненное течение репаративных процессов завершается формированием гладкого рубца (рис. 5).
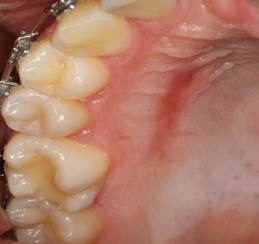
Рис. 5. Рана после снятия мембраны
Заключение. Полимерные имплантаты Реперен удобны в практическом применении и позволяют закрыть дефекты различные по форме. Материал полностью отвечает современным требованиям, предъявляемым к имплантатам. Является биологически инертным, отсутствует токсическое воздействие на окружающие ткани, что выгодно отличает данный полимерный материал от широко применяющихся в настоящее время производных метилметакрилата (Протакрил, Палокос); не вызывают на себя воспалительной реакции и в дальнейшем не резорбируется. Полимерная мембрана представляет собой мягкую, эластичную прозрачную плёнку, на одну поверхность которой нанесена сетка (рёбра жёсткости для предотвращения прорезывания нити при подшивании), а другая поверхность идеально гладкая (степень шероховатости порядка нанометров) [5]. Данный материал полностью соответствует критериям установленным еще в конце ХХ века, но обладает и дополнительными преимуществами: высокая биостабильность и биосовместимость, устойчивость к воздействию биологически активных жидкостей, хорошая адгезия к ране, отсутствие движения протеза за счет своей сетчатой структуры, отсутствие травматического воздействия при приеме пищи, снижение болевого синдрома. Пластичность материала, наряду с достаточной прочностью позволяет быстро моделировать эндопротез, лишенный теплопроводности и являющийся биостабильным.
Рецензенты:
Жулев Е.Н., д.м.н., профессор, зав. кафедрой ортопедической стоматологии, ГБОУ ВПО Нижегородская государственная медицинская академия Минздрава России, г. Нижний Новгород;
Казарина Л.Н., д.м.н., профессор, зав. кафедрой пропедевтической стоматологии, ГБОУ ВПО Нижегородская государственная медицинская академия Минздрава России, г. Нижний Новгород.
Библиографическая ссылка
Дурново Е.А., Мочалова Д.А., Беспалова Н.А., Янова Н.А., Клочков А.С., Рунова Н.Б. КЛИНИЧЕСКАЯ ОЦЕНКА ТЕЧЕНИЯ РАНЕВОГО ПРОЦЕССА НА СЛИЗИСТОЙ ОБОЛОЧКЕ ПОЛОСТИ РТА ПРИ ИСПОЛЬЗОВАНИИ ПОЛИМЕРНОГО ТРАНСПЛАНТАТА // Современные проблемы науки и образования. 2014. № 6. ;URL: https://science-education.ru/en/article/view?id=15932 (дата обращения: 19.05.2026).



