Содержание в слоевище лишайников биологически активных веществ (БАВ) обусловливает довольно широкое их использование в официальной и народной медицине для лечения болезней желудочно-кишечного тракта, органов дыхания, инфекционных заболеваний кожи, эндокринных нарушений, также применение их в качестве иммуномодулирующих, противоопухолевых, гепатопротекторных и детоксикационных препаратов [8, 9]. Несмотря на то, что лишайниковые вещества обладают широким спектром лекарственных свойств, включая противомикробные, противомикотические, противовирусные, противовоспалительные, обезболивающие, жаропонижающие, антипролиферативные и цитотоксические, их терапевтический потенциал еще недостаточно изучен, что сдерживает широкое производство на их основе фармацевтических препаратов и применение в медицине.
Активное вещество биопрепаратов на основе лишайникового сырья, разработанных и производимых в лаборатории механохимических биотехнологий Северо-Восточного федерального университета – лишайниковые β-олигосахариды, способны связывать различные по природе вредные вещества (тяжелые металлы (ТМ) и радионуклиды, карбонильные соединения и фенолы, молочную кислоту и др. органические соединения) и выводить их из организма[1-4, 6,7].
Вместе с тем, первым требованием, предъявляемым к самому биосырью – слоевищам лишайников – является их экологическая чистота, так как известно, что нативные талломы, произрастающие на площадях загрязненных тяжелыми металлами и/или радионуклидами способны их эффективно сорбировать и накапливать[10].
Целью данной работы является проведение анализа содержания токсичных (Pb, Hg, Cd, Fe, As), биогенных (I, Se, Ca, Mg, P, K, Na, Li) элементов и радионуклидов (137Cs и 90Sr) в талломах лишайников р.Cladoniaи определение некоторых биологически активных веществ методом хроматографии.
Материал и методы исследований
Объектом исследования служили лишайники рода Cladonia, произрастающиев ряде районов Якутии, в местах, предполагаемых для сбора лишайникового сырья с целью последующего биотехнологического передела. Для оценки биобезопасности сырья определяли содержание в них ряда токсичных (в том числе ТМ), биогенных элементов, а также радионуклидов цезия и стронция в Алданском, Мегино-Кангаласском, Верхневилюйском районах и в окрестностях г. Якутска (рис.1).
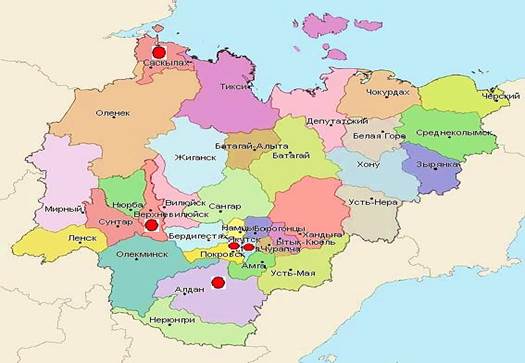
Рис.1. Районы сбора лишайников в Республике Саха (Якутия)•
Содержание радионуклидов цезия и стронция определяли с помощью гамма-бета-спектрометрического комплекса УСК «Гамма плюс» с программным обеспечением «Прогресс» для испытаний проб продовольствия на соответствие требованиям критериев радиационной безопасности[5].
Лишайниковое сырье, собранное в Анабарском районе, в 150 км севернее п.Сааскылах, анализировалось с использованием метода атомно-эмиссионной спектрометрии с индуктивно-связанной плазмой.
Поскольку в отечественной фармакопее отсутствует общая статья по определению ТМ в лекарственном растительномсырье, мы брали за основу СанПин 2.3.2. 1078-01 от 14.11.2001/22.03.02.
При исследовании БАВ предварительно был составлен список определяемых соединений для оценки содержания физиологически активных компонентов: арбутин, галловая кислота, коричная кислота, хлорогеновая кислота, кверцетин, рутин, урсоловая кислота, байкалин, байкалеин, кемпферол, лютеолин, скутелларин, дельфинидин, апигенин, изорамнетин, гиперозид. Среди этих веществ имеются флавоноиды, органические кислоты, полифенольные соединения и т.п.Для каждого из перечисленных соединений была проведена оптимизация условий масс-спектрометрического определения для режима тандемного масс-детектирования в режиме регистрации отрицательных ионов. Были подобраны ионные переходы, потенциал декластеризации и энергия соударений в камере столкновений. Также получены спектры хроматограмм в УФ диапазоне (230 – 400 нм).В качестве неподвижной фазы при анализе проб использовали колонку с обращено-фазовым сорбентом AcclaimRSLC, длиной 150 мм, внутренним диаметром 2.1 мм, размером зерна сорбента 3 мкм, фирмы «Thermo». При хроматографическом разделении использовали программу градиентного элюирования.
Пробоподготовка заключалась в приготовлении трех различных экстрактов тремя растворителями – метиловым спиртом, этилацетатом и дихлорметаном. Полученные экстракты высушивали в вакуумном роторном испарителе и снова растворяли в 2 мл метилового спирта. Затем экстракты отфильтровали, разбавляя в 10 раз водой.
Кроме того, определяли летучие компоненты исследуемого образца методом газовой хроматографии с масс-спектрометрическим детектированием.
В работе использовали газовый хроматомасс-спектрометр GCMS-2010 Ultra фирмы Shimadzu (Япония). Разделение проводили на колонке ZB-5 MS 30м × 0,25 мм, с использованием градиентного режима нагрева: 0-2 мин – 40°С, 2–28 мин 40–300°С, 28-34 мин – 300°С. Сканирование проводили в диапазоне m/z 15–400 Да. Температура инжектора –250°С, температура источника ионизации –250°С, температура интерфейса –250°С, напряжение на детекторе –400 еВ. Ввод пробы осуществляли в двух режимах: ввод 0.5 мл нагретого (80°С, 10 мин) пара над образцом порошка растительного происхождения с добавкой 1 мл метанола и 1 мкл жидких экстрактов CH2Cl2, EtOAc и MeOH из этого порошка, разбавленных в 100 раз в CH2Cl2.
Результаты и обсуждение
Полученные данные по содержанию токсичных (Pb, Hg, Cd, Fe, As), биогенных (I, Se, Ca, Mg, P, K, Na, Li) элементов в талломах лишайников р.Cladonia, по сравнению с ПДК для соответствующих элементов в пищевых продуктах, представлены на рис.2, по содержанию 137Cs и 90Sr - на рис.3.
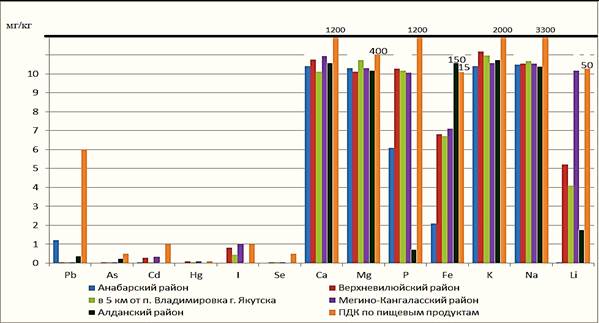
Рис.2. Содержание токсичных (Pb, Hg, Cd, Fe, As), биогенных (I, Se, Ca, Mg, P, K, Na, Li) элементов в пробах слоевищ лишайников р.Cladonia взятых в пяти районах Якутии, по сравнению с ПДК
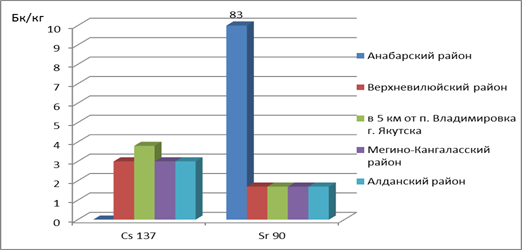
Рис.3. Содержание 137Cs и 90Sr в пробах слоевищ лишайников р.Cladonia взятых в четырех районах Якутии. ПДК для цезия 200 Бк/кг, для стронция - 100 Бк/кг
Наибольшее содержание 90Sr - до 83 Бк/кг (ПДК ≤ 100 Бк/кг), отмеченное в Анабарском районе объясняется сбором сырья непосредственно на месте проведения горно-добывающих работ.
В ходе предварительных экспериментов по определению БАВ в образце были обнаружены следующие соединения, которые представлены в таблице 1.
Таблица 1
Химические вещества, обнаруженные в экстрактах
|
Содержание в колбе, мкг |
||||||
|
Гиперозид |
Кверцетин |
Лютеолин |
Галловая кислота |
Урсоловая кислота |
Хлорогеновая кислота |
|
|
MeOH экстр. |
0,15 |
0,06 |
0,02 |
16 |
108 |
0,04 |
|
EtOAc экстр. |
0,04 |
0,04 |
0,01 |
12 |
9 |
0 |
|
СН2Сl2 экстр. |
<ПО |
<ПО |
<ПО |
<ПО |
<ПО |
<ПО |
Также в экстрактах присутствовала коричная кислота в следовых количествах. Не найдены арбутин, байкалин, байкалеин, кемпферол, скутелларин, дельфинидин, апигенин, изорамнетин, вогонин, рутин. Однако сопоставление УФ и МС/МС спектров позволяют судить о том, что в данном образце содержатся дополнительные неидентифицированные соединения. Их идентификация требует дополнительных исследований.
Наибольшее извлечение целевых компонентов показал вариант экстракции с использованием метанола (рис. 4).
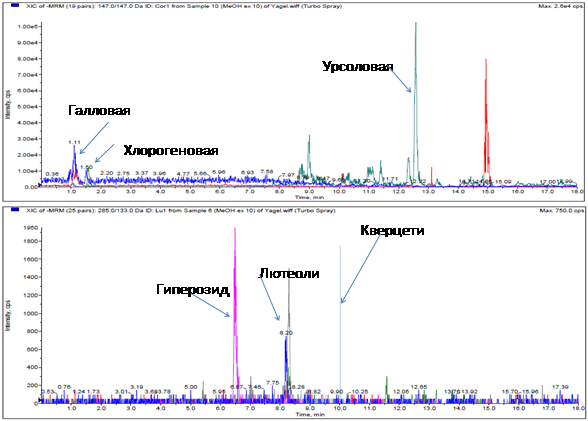
Рис. 4. ХроматограммыМеОН экстракта с извлечением ионных переходов обнаруженных соединений
В экстракте EtOAc было обнаружено сравнительно меньшее число летучих компонентов (около 20). Из них характерными для исследуемого образца являются предельные кислоты и их эфиры. Экстракция CH2Cl2 и MeOH позволяет выделить намного больше (около 100) летучих компонентов из исследуемого объекта. Основными компонентами CH2Cl2 и MeOH экстрактов являются предельные углеводороды и спирты. Кроме того в CH2Cl2 обнаружен ароматический спирт - 2,4-диизобутил-фенола.
Выводы
Результаты исследования свидетельствуют о том, что содержание токсичных элементов и радионуклидов не превышает соответствующих ПДК. Кроме того, лишайники р.Cladonia могут служить источником биогенных элементов – особенно Ca, Mg, P, K, Na и микродоз LiI, Se.
Химические ГХ-МС профили исследованных экстрактов типичны для растительных объектов, однако следует отметить отсутствие летучих производных фурана, что косвенно свидетельствует об отсутствии в образце больших количеств моно- и дизамещенных сахаридными остатками органических компонентов. Исследованный образец растительного сырья не содержит больших количеств среднелетучих органических соединений сложной структуры, таких как, например, незамещенные сапонины и сесквитерпены. Перспективы исследования химического состава образца принадлежат методам жидкостной хроматографии, позволяющей идентифицировать и определять нелетучие физиологически активные компоненты.Методом ВЭЖХ-МС в образцах экстрактов обнаружили галловую кислоту, коричную кислоту, хлорогеновую кислоту, кверцетин, рутин, урсоловую кислоту, лютеолин и гиперозид. Однако сопоставление УФ и МС/МС спектров позволяют судить о том, что в данном растении содержатся дополнительные неидентифицированные соединения. Их идентификация требует дополнительных исследований.
Рецензенты:
Охлопкова А.А., д.т.н., профессор, зав. кафедрой "Высокомолекулярные соединения и органическая химия" Института естественных наук ФГАОУ ВПО «Северо-Восточный федеральный университет им. М.К. Аммосова», г. Якутск.
Николаев А.Н., д.б.н., директор Института естественных наук ФГАОУ ВПО «Северо-Восточный федеральный университет им. М.К. Аммосова», г. Якутск.
Библиографическая ссылка
Аньшакова В.В., Аньшакова В.В., Степанова А.В., Смагулова А.Ш. ХИМИЧЕСКИЙ АНАЛИЗ ЛИШАЙНИКА КАК ПОТЕНЦИАЛЬНОГО БИОСЫРЬЯ // Современные проблемы науки и образования. 2014. № 6. ;URL: https://science-education.ru/en/article/view?id=15430 (дата обращения: 21.04.2026).



