Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
STUDY OF FACTORS AFFECTING THE CORROSION OF ELECTRICAL EQUIPMENT OPERATING I N AGGRESSIVE ENVIRONMENTS
Введение
В настоящее время коррозия ежегодно приводит к миллиардным убыткам, причем основной ущерб, причиняемый ею, заключается не только в потере металла как такового (в мире до 20 % металла в год уходит именно в коррозионные отходы), но и в разрушении дорогостоящих изделий и оборудования. Еще больший ущерб наносят косвенные потери при простоях оборудования при замене прокорродировавших деталей и узлов, нарушении технологических процессов.
В США, по данным NACE, ущерб от коррозии, включая затраты на борьбу с ней, составляют 3,1 % ВВП ($276 млрд в год), в Германии – 2,8 % ВВП. В пределах 2–4 % ВВП находится этот показатель и в других развитых странах. При этом потери металла, включающие вышедшие из строя металлические конструкции, изделия, оборудование, составляют 10–20 % годового производства. В нашей стране нет официальной статистики, которая бы отражала экономический ущерб от коррозии, но, по некоторым оценкам, он составляет не менее 5 % от ВВП [2].
Эти цифры делают необходимым всестороннее изучение коррозии, которое, в свою очередь, служит основой для разработки методов борьбы с коррозионными процессами.
Проблема коррозионной стойкости конструкционных материалов до сих пор является весьма актуальной для современной промышленности. Принимая во внимание размеры ущерба от коррозии и колоссальное число различных металлов и их сплавов, а также коррозионноагрессивных сред, очевидно, что в этой области науки еще долго будет существовать обширное поле для исследований.
В частности, практика эксплуатации электрооборудования цехов физико-химической очистки воды на птицеперерабатывающих предприятиях показывает, что оно подвержено преждевременному разрушению в результате быстрого окисления медных контактов оборудования, что нежелательно сказывается на работе всего комплекса очистки и приводит к быстрому выводу оборудования из строя. Причиной этой проблемы может служить агрессивная среда, в которой происходит эксплуатация данного оборудования.
В атмосферных условиях медь отличается высокой коррозионной стойкостью. На сухом воздухе поверхность меди практически не меняется. А при контакте с влажным воздухом образуется тонкая защитная пленка, состоящая из оксидов меди и ее чистой закиси. В воде и нейтральных растворах солей медь обладает также достаточной устойчивостью, которая заметно снижается при доступе кислорода и окислителей [4].
Цель исследования
Целью настоящей статьи является определение качественного состава продуктов коррозии медных контактов электрооборудования и разработка рекомендаций по его эксплуатации в условиях агрессивной среды.
Результаты исследований и их обсуждение
Одними из важнейших факторов, влияющих на скорость коррозии, являются влажность воздуха и содержание в нем различных примесей. В связи с этим для установления причин окисления медных контактов электрооборудования были проведены исследования в цехе физико-химической очистки воды (ФХО) птицеводческого предприятия, направленные на изучение состава воздуха рабочей зоны, технической воды и продуктов коррозии медных контактов [5].
Для установления состава воздуха были отобраны пробы воздуха рабочей зоны операторской (1 этаж) и зоны флотации (2 этаж) цеха ФХО технической воды. Количественный химический анализ воздуха приведен в таблице № 1.
Таблица 1
Количественный химический анализ воздуха рабочей зоны
|
Место отбора пробы |
Определяемые показатели |
Единицы измерения |
Результаты исследований, характеристика погрешности |
|
Рабочая зона оператора очистных сооружений (операторская) |
Аммиак |
мг/м3 |
менее 1 |
|
Дигидросульфид |
мг/м3 |
менее 5 |
|
|
Хлор |
мг/м3 |
менее 0,5 |
|
|
Формальдегид |
г/м3 |
менее 0.01 |
|
|
Гидрохлорид |
мг/м3 |
менее 3 |
|
|
Диоксид серы |
мг/м3 |
2.2±0.5 |
|
|
Зона флотации |
Аммиак |
мг/м3 |
1,1+0.25 |
|
Гидрохлорид |
мг/м3 |
менее 3 |
|
|
Диоксид серы |
мг/м3 |
2,1+0.5 |
|
|
Дигидросульфид |
мг/м3 |
менее 5 |
|
|
Формальдегид |
мг/м3 |
менее 0,01 |
|
|
Хлор |
мг/м3 |
менее 0,5 |
Полученные данные (табл. 1) свидетельствуют о наличии в составе воздуха рабочей зоны следующих компонентов: аммиака, сероводорода (дигидросульфида), хлора, хлороводорода (гидрохлорида), диоксида серы, которые относятся к числу коррозионноактивных газов. Согласно правовой и нормативной документации [3] среда, в зоне которой происходит работа электрооборудования, является среднеагрессивной, что способствует коррозии медных контактов.
Для выявления всех факторов, влияющих на состав атмосферы рабочей зоны цеха ФХО воды, был проведен анализ технической воды, поступающей на очистку из цеха убоя птицы (проба № 1) и после цикла флотационной очистки (проба № 2). Результаты представлены в таблице № 2.
Таблица 2
Результаты анализа проб воды
|
Наименование определяемых компонентов |
Единицы измерения |
Результаты анализа |
|
|
Проба № 1 |
Проба № 2 |
||
|
Водородный показатель |
рН |
6,95 ± 0,20 |
6,27 ± 0,20 |
|
Хлорид-ион |
мг/дм3 |
456,5 ±45,7 |
461,5 ± 46,2 |
|
Сульфаты |
мг/дм3 |
356 ± 64 |
593 ± 107 |
|
Аммоний-ион (по азоту) |
мг/дм3 |
27,9 ±5,9 |
18,4 ± 3,8 |
|
Фосфат-ион |
мг/дм3 |
2,55 ± 0,36 |
0,16 ± 0,03 |
|
Сульфид-ионы |
мг/дм3 |
0,008 ± 0,003 |
0,023 ± 0,006 |
|
Железо общее валовое |
мг/дм3 |
29,6 ± 3,0 |
5,10 ± 0,51 |
|
Цинк |
мг/дм3 |
0,188 ± 0,039 |
0,195 ± 0,041 |
|
Медь |
мг/дм3 |
0,0059 ± 0,0024 |
0,0048 ± 0,0019 |
|
Фенолы |
мг/дм3 |
0,035 ± 0,011 |
0,446 ± 0,138 |
Полученные результаты (табл. 2) показывают содержание в составе технической воды хлорид – и сульфид – ионов, обладающих корродирующими свойствами, присутствие которых в атмосфере влажного воздуха значительно способствует увеличению скорости коррозии.
Проведенные исследования по установлению состава воздуха рабочей зоны и технической воды позволяют выявить причины коррозии медных контактов электрооборудования
В соответствии с ISO 11357 проведен качественный анализ окисленных образцов медных контактов в различных зонах цеха ФХО технической воды. Определение проводили методом дифференциальной сканирующей калориметрии и термогравиметрического анализа (ДСК и ТГ) на синхронном термоанализаторе марки STA449F3 Jupiter фирмы NETZSCH. Результаты испытаний представлены на рисунках 1–3.
На основе полученных данных установили, что в составе продуктов коррозии содержатся следующие компоненты:
• сульфид меди (II) CuS (температура разложения > 450°С);
• сульфид меди (I) Cu2S (температура разложения 1129°С);
• оксид меди (II) CuО (температура разложения > 800°С);
• оксид меди (I) Cu2О (температура разложения 1242°С);
• хлорид меди (II) CuCl2 (температура разложения 596°С);
• хлорид меди (I) CuCl (температура разложения 1212°С).
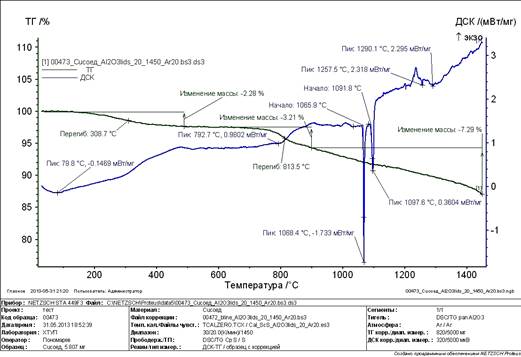
Рисунок 1. Кривая ДСК и ТГ образцов медных контактов электрооборудования цеха ФХО технической воды
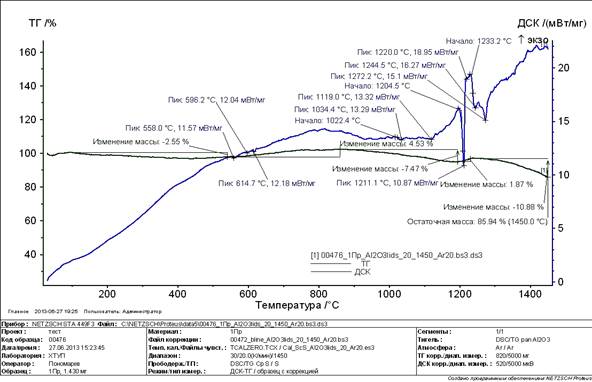
Рисунок 2. Кривая ДСК и ТГ опытного образца № 2 (площадка напорно-реагентного флотатора)
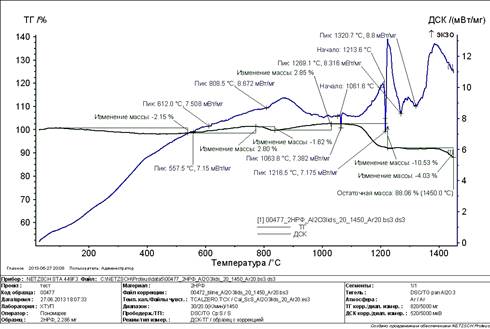
Рисунок 3. Кривая ДСК и ТГ опытного образца № 3 (рабочая зона оператора)
Установленный качественный состав продуктов коррозии медных контактов электрооборудования и анализ научной литературы позволяют предположить механизм протекающих процессов.
В атмосферных условиях в отличие от многих других металлов медь не подвергается коррозии, так как на ее поверхности образуется тонкий ровный слой (пленка) продуктов коррозии, не содержащий никаких агрессивных соединений, способных при каких-либо условиях разрушать металл. Коррозия меди в атмосферных условиях - процесс самопроизвольно затухающий, так как продукты коррозии защищают поверхность металла от внешней среды. Но медь становится неустойчивой в таких средах:
- сера, сероводород, некоторые другие соединения серы;
- окислительные кислоты, аэрированные неокислительные (также угольная), горячий, холодный концентрат H2SO4:
Cu + 2H2SO4 → CuSO4 + SO2↑ + 2H2O - горячий концентрат,
Cu + H2SO4 → CuO + SO2↑ + H2O - холодный концентрат;
- растворы окислительных солей тяжелых металлов (Fe2(SO4)3, FeCl3);
- аэрированные воды, агрессивные воды (с низким содержанием ионов магния, кальция, высоким - кислорода, углекислого газа);
- амины, NH4OH (содержащим кислород).
В ходе исследования было установлено, что атмосфера, в которой происходит эксплуатация электрооборудования, содержит аммиак, сероводород (дигидросульфид), хлор, хлороводород (гидрохлорид), диоксид серы, которые относятся к числу коррозионно-активных газов и значительно влияют на скорость атмосферной коррозии меди. Перечисленные газы, попадая в плёнку влаги на поверхности корродирующего металла, увеличивают ее электропроводность и гигроскопичность продуктов коррозии (например, SO3, HCl), действуют как депассиваторы (например, HCl, SO2) или комплексообразователи (NH3), а также как катодные деполяризаторы (SO2, Cl2):
2HSO3- + 2H+ + 2e = S2O42- + 2H2O,
Cl2 + 2e = 2Cl- .
По данным, приведённым в научно-технической литературе, известно, что сера и ее соединения - сернистый ангидрид (SO2), сероводород (H2S), меркаптаны или тиоспирты и т.д. являются достаточно агрессивными, коррозионно-активными веществами. Наиболее активным компонентом при высокотемпературной газовой коррозии является сероводород. Он даже более опасен, чем диоксид серы. Сухой сернистый газ в любой концентрации (до 10 %) оказывает на медь незначительное действие. Его активность остается низкой до тех пор, пока относительная влажность воздуха не достигает 63 %. При более высокой влажности увеличение концентрации сернистого газа вызывает заметное увеличение коррозии.
Сероводород при низкой влажности вызывает лишь незначительное потускнение меди, но при повышении влажности в его присутствии коррозия очень резко усиливается, поэтому считается, что из многих металлов медь наряду с железом и магнием является наименее стойкой в смеси воздуха с сероводородом. Интенсивную коррозию меди под действием сероводорода в присутствии паров воды связывают с высокой скоростью электрохимических процессов. Однако, по-видимому, большую роль в этом играют также особенности продуктов коррозии (Cu2S). Они образуют на поверхности металла пленку, которая в присутствии кислорода и паров воды неустойчива: через 15-35 дней после образования в результате окисления сульфида меди она изменяет цвет, ее объем резко увеличивается, она растрескивается и осыпается. Поэтому образующиеся под действием сероводорода наслоения продуктов коррозии могут расти до большой толщины, не предохраняя металл от дальнейшей коррозии. Иными словами, пленки, состоящие из сульфида меди, не обладают защитными свойствами. Некоторые авторы отмечают, что присутствие сульфидов в окисных пленках лишает эти пленки защитных свойств.
Также медь вступает в реакцию с растворами аммиака и хлористого аммония, содержащимися в атмосфере рабочей зоны эксплуатации электрооборудования. В воде и нейтральных растворах солей медь обладает достаточной устойчивостью, которая может снижаться при доступе кислорода и окислителей.
В нейтральных хлоридных средах предложен следующий стадийный механизм растворения меди c двумя возможными маршрутами ионизации:
Сu0 + nCl- → CuCln1-n + е
Cu0 → Cu+ + e
-----------------------------------
Cu+ + nCl- → CuCln1-n
Хлорид меди при взаимодействии с влагой окисляется и гидролизуется, превращаясь в зеленую основную хлорную медь - атакамит: рыхлое вещество характерного ярко-зеленого цвета. Разрушение может идти с большой скоростью. Ускоряется коррозия меди в горячей воде при солесодержании воды более 300 мг/л и концентрации хлоридов более 20 мг/л.
При содержании в воде хлоридов свыше 30 мг/л основные карбонаты меди переходят в более растворимые основные хлориды СuСl2 • ЗСuО • ЗН2O с рыхлой, пористой структурой, что способствует развитию коррозии. Наличие в воздухе паров очень летучей соляной кислоты также вызывает активную коррозию меди.
Заключение
Проведенные исследования позволили установить причину, вызывающую коррозию медных контактов электрооборудования цеха физико-химической очистки воды на птицеперерабатывающем предприятии: эксплуатация оборудования в среднеагрессивной среде, что является недопустимым, так как медь в этих условиях подвержена сильной коррозии. В связи с этим, в целях предотвращения коррозионного разрушения медных контактов электрооборудования представляется целесообразным уменьшение агрессивности среды и повышение антикоррозионных свойств медных контактов путём нанесения неметаллических лаковых покрытий, удовлетворяющих следующим требованиям: низкая влаго- и кислородопроницаемость, высокие механические характеристики, высокая и стабильная во времени адгезия покрытия к металлу, стойкость к катодному отслаиванию, хорошие диэлектрические характеристики, устойчивость покрытия к тепловому старению [1].
Рецензенты:
Медяник Н.Л., д.т.н., профессор, зав. кафедрой химии ФГБОУ ВПО «Магнитогорский государственный технический университет им. Г.И. Носова», г. Магнитогорск.
Стеблянко В.Л., д.т.н., профессор ФГБОУ ВПО «Магнитогорский государственный технический университет им. Г.И. Носова», г. Магнитогорск.
Библиографическая ссылка
Чупрова Л.В., Муллина Э.Р., Ершова О.В., Мишурина О.А. ИССЛЕДОВАНИЕ ФАКТОРОВ, ВЛИЯЮЩИХ НА КОРРОЗИЮ ЭЛЕКТРООБОРУДОВАНИЯ, ЭКСПЛУАТИРУЕМОГО В УСЛОВИЯХ АГРЕССИВНОЙ ОКРУЖАЮЩЕЙ СРЕДЫ // Современные проблемы науки и образования. 2014. № 2. ;URL: https://science-education.ru/en/article/view?id=12987 (дата обращения: 15.05.2026).



