Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
VIDEOBRONCHOSCOPICAL METHODS IN A COMBINED TREATMENT OF ACUTE PURULENT DESTRUCTIVE PROCESSES LUNGS AND PYOPNEUMOTHORAX
Введение
Лечение острых гнойных деструктивных заболеваний легких остается актуальной проблемой гнойной торакальной хирургии, это обусловлено возрастанием частоты заболеваний, их осложнений, тяжести течения, частым переходом процесса в хронический, а также высокой летальностью [2, 4].
Лечение больных с острыми деструктивными заболеваниями легких в настоящее время является комплексным, включающим массивную антибактериальную терапию, дренирование гнойных полостей, санацию бронхиального дерева, криоплазменно-антиферментную терапию, плазмаферез и др.[5]
Эмпиема плевры и пиопневмоторакс являются одним из наиболее частых и тяжелых осложнений гнойных деструктивных заболеваний легких [8]. При анализе данных о 3005 больных абсцессами и гангренами легких, эмпиема плевры и пиопневмоторакс возникли у 33,3% пациентов [2, 3]. Абсцессы лёгких осложнялись эмпиемой плевры в 8-11% случаев, а гангрена - в 55-90% [3, 8].
Одной из причин перехода в хронический процесс острого абсцесса легких является образование бронхоплеврального свища [9].
Наличие бронхиального свища затрудняет лечение, препятствуя созданию вакуума, необходимого для расправления легкого, и делает невозможной санацию полости пиопневмоторакса, что приводит к необходимости хирургического вмешательства [1].
В последние годы, благодаря видеобронхоскопической технологии, появились новые возможности в совершенствовании методов дренирования гнойных полостей легких и санации бронхиального дерева у больных острым абсцессом и гангреной легких [7, 9, 10].
При выборе методов местного лечения острого абсцесса и гангрены легкого важно учесть характер и выраженность нарушений дренажной функции бронхов.
В связи с этим целью настоящей работы явилась повышение эффективности комплексного лечения острого абсцесса и гангрены легкого и пиопневмоторакса путем применения санационной фибробронхоскопии и клапанной бронхоблокации.
Материалы и методы
В основу положены данные о 320 больных острым абсцессом и гангреной легких, в том числе осложнившихся пиопневмотораксом.
Все больные получали комплексное лечение, включающее адекватное опорожнение гнойных полостей и их санацию (пункции и дренирование плевральной полости промывание её антисептиками), антибактериальную терапию (цефалоспорины III-IV поколения, фторхинолоны, карбапенемы и др.), коррекцию микроциркуляторных нарушений, детоксикационную терапию, коррекцию нарушений гемостаза
Эффективность видеоброонхоскопической санации бронхов изучалась у 210 больных, из которых у 60 пациентов она проводилась и у 150 пациентов – не применялась. Обе эти группы были сопоставимы по характеру процесса, его локализации, полу, возрасту, тяжести заболевания.
Эффективность бронхоблокации при пиопневмотораксе с бронхоплевральной фистулой изучена у 110 больных. Они были разделены на 2 группы. В первую группу вошли 43 (39,1%) больных, в лечении которых применялась клапанная бронхоблокация. Во вторую группу вошли 67 (60,9%) пациентов, у которых бронхоблокация не применялась. По характеру процесса, его локализации, полу, возрасту, тяжести заболевания обе группы были сопоставимы.
Статистическая обработка полученных данных осуществлена с использованием программы Microsoft Offis Exel 2007. Статистическая значимость различий между средними величинами определяли с помощью критерия Стьюдента (t). Статистически значимыми принимались различия p<0,05.
Результаты и обсуждение
Проведенные исследования у больных с острым абсцессом и гангреной легких показали, что бронхи, непосредственно дренирующие полость распада, претерпевали существенную патогистологическую перестройку. Крайней степени этих изменений являлась тотальное разрушение стенки бронха. В большинстве случаев в покровном эпителии определялось выраженное слущивание клеток, оголение базальной мембраны, дистрофические изменения и снижение количества бокаловидных клеток. Базальная мембрана была умеренно склерозирована, утолщена. В собственной пластинке и подслизистой основе отмечалось полнокровие микрососудов, часто с блокированием просвета фибрином, а также большое количество клеточных инфильтратов, с преобладанием при острых абсцессах легких лимфоцитов и макрофагов, а при гангрене легких – нейтрофильных гранулоцитов.
В крупных бронхах расположенных проксимально, вне непосредственной связи с областью деструкции, морфологическая реорганизация была менее выражена. В них отмечались структурные изменения преимущественно по типу катаральной и склерозирующей форм бронхита. В покровном эпителии бронхов преобладали дистрофические изменения (в 68,6% наблюдений), участки оголения базальных клеток (65,7%), дезинтеграция эпителиоцитов с увеличением межклеточных пространств (60%), пролиферация бокаловидных клеток и гнездное изменение функциональной активности эпителиоцитов. Базальная мембрана эпителия в большей части наблюдений была неравномерно нерезко утолщена (в среднем 4,8±0,16мкм). Подэпителиальная инфильтрация характеризовалась очаговым характером, в составе клеточных инфильтратов определялись, как мононуклеары, так и нейтрофильные гранулоциты. Склеротические изменения собственной пластинки отмечались в 62,9% наблюдений.
Такая структурная перестройка крупных бронхов нарушает дренажную функцию бронхов и предшествует развитию гнойно-деструктивных заболеваний легких. Важно отметить, что у тех больных, где визуально эндоскопически слизистая оболочка была без изменений, морфологическое исследование бронхобиопсий выявило преобладание дистрофически-атрофических процессов.
С целью уменьшения воспалительных изменений в бронхиальном дереве у больных острым абсцессом и гангрены легкого применены видеоэндоскопическая селективная транстрахеобронхиальная катетеризация полости острого абсцесса легкого и посегментарно-субсегментарная санация бронхов.
Видеоэндоскопическая селективная транстрахеобронхиальная катетеризация полости острого абсцесса лёгкого осуществлялась под наркозом. Трахея интубировалась жёстким тубусом фирм Фриделя или Шторц. Фибробронхоскопом находился дренирующий бронх на уровне субсегментарного деления и проводилась предварительная санация бронхиального дерева антисептическими растворами. Жёсткий тубус выводился в подсвязочное пространство и под видеоконтролем трахея пунктировалась ниже перстневидного хряща иглой, не повреждая перешеек щитовидной железы, через которую потом вводился катетер-микроирригатор в просвет трахеи. Игла извлекалась. Катетер захватывался гибкими биопсийными щипцами и устанавливался в дренирующий бронх. Установив катетер, приступали к проточной санации полости абсцесса с одновременной аспирацией его содержимого через фибробронхоскоп. При правильном нахождении дренирующего полость абсцесса бронха и точном проведении в него катетера, введение растворов шприцом происходили свободно, без особых усилий с видимым оттоком содержимого полости. Правильность установки катерера-микроирригатора подтверждалось рентгенологически (рисунок 1, 2). Свободный наружный конец катетера фиксировался швом на коже шеи.
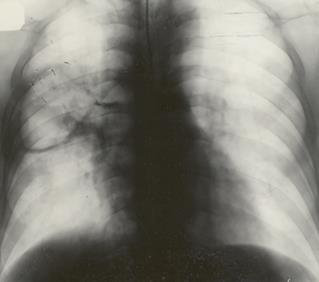
Рисунок 1. Катетер - микроирригатор установлен в полость деструкции в S6 правого лёгкого (прямая проекция).
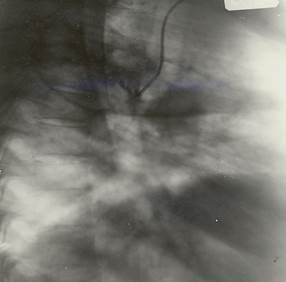
Рисунок 2. Катетер-микроирригатор установлен в полость деструкции в S6 (правый боковой снимок)
В последующем через катетер проводилась санация полости абсцесса антисептиками с введением антибактериальных препаратов согласно чувствительности микрофлоры в течение 10-14 дней. При регулярном промывании полости абсцесса через установленный катетер увеличивалось активное откашливание, значительно улучшался дренаж. При введении и создании высокой постоянной концентрации антибактериальных препаратов полость быстро очищалась, воспаление стихало.
Санационная фибробронхоскопия при гнойной деструкции легких состояла из трёх этапов: местная анестезия, введение фибробронхоскопа, осмотр и санация трахеобронхиального дерева.
Целью подготовки больного явилось безопасное и эффективное проведение санационной фибробронхоскопии. Подготовка включала общие и местные меры.
Общая подготовка заключалась в коррекции функциональных нарушений органов и систем, прежде всего, кровообращения, со стороны которой можно ожидать наиболее серьёзные осложнения. В случае беспокойства больного или запланированной массивной санации – ограничивались премедикацией, проводимой перед процедурой: 1 мл-1% раствора димедрола.
Местную анестезию начинали с анемизации верхних дыхательных путей: орошение ротоглотки раствором лидокаина 10% в виде аэрозоли, в спрей-упаковке. На первом этапе во время спокойного вдоха производили орошение языка, нёбных душек и язычка мягкого нёба тремя дозами аэрозоли лидокаина 10%. Выжидали в течение 30-40 секунд и после этого проводили второй этап: на глубоком вдохе орошали тремя дозами аэрозоли лидокаина 10% на корень языка, надгортанник, черпало-надгортанные складки и голосовые связки. Перерыв между первым и вторым этапами обусловлен тем, что при первом попадании на слизистую оболочку ротоглотки аэрозоли лидокаина возникает неприятное жжение, которое проходит через 30-40 секунд. После этого следующие три дозы лидокаина 10% на глубоком вдохе полностью обеспечивали обезболивание в области голосовой щели, включая слизистую оболочку подсвязочного пространства и нередко до границы средней третьи трахеи. После анестезии ротоглотки, через 1-2 минуты, под визуальным контролем через канал фибробронхоскопа проводили одномоментное введение шприцом 6 мл 2% раствора лидокаина, орошая карину и главные бронхи. По истечении 2 минут приступали непосредственно к фибробронхоскопии.
Умеренное и большое количество мокроты в просвете бронхов препятствует хорошему проникновению анестетика в слизистую. Поэтому проводили аспирацию и предварительную санацию для очищения слизистой оболочки главных, долевых бронхов и сегментарных устьев, после чего дополнительно орошали 6,0 мл 2% раствора лидокаина каждую сторону бронхиального дерева. Этим добивались тщательного обезболивания главных зон (бифуркация трахеи, шпоры долевых, сегментарных и субсегментарных бронхов), что позволило более детально проводить санацию. После данной анестезии во время фибробронхоскопии больные вели себя спокойно, у них в течение 10-20 минут был подавлен кашлевой рефлекс, что позволяло за указанное время проводить адекватную санацию бронхиального дерева, а также избежать гипоксию.
Введение фибробронхоскопа осуществляли через рот в положении больного сидя или лёжа, используя для предохранения аппарата ротоблокатор. Данный метод введения имеет свои преимущества – лёгкость выполнения и атравматичность, а также позволяет свободно и быстро извлекать аппарат и вводить его повторно, при необходимости промывать канал. Часто у больных бывает искривление носовой перегородки, затрудняющей свободное проведение аппарата. При введение фибробронхоскопа через рот не травмируется слизистая носового хода. Для адекватной санации использовались фибробронхоскопы «Olympus» BF XT40, BF 1Т20 с аспирационными каналами 2,2 мм, 2,4 мм, диаметр наружной части тубуса – 5,9 мм и 6,2 мм. Наружный диаметр аппаратов не позволял свободно проходить через носовые ходы. Недостатками этого метода можно считать: риск повреждения тубуса зубами больного, а также контакт аппарата с флорой полости рта.
Всем больным санационная фибробронхоскопия проводилась в положении сидя. Больные самостоятельно держали лоток на полотенце под подбородком для сплёвывания слюны и мокроты.
Фибробронхоскоп вводили через рот по спинке языка к язычку мягкого нёба. Далее, чуть сгибая дистальную часть аппарата вниз, входили в ротоглотку. Аппарат ложился на надгортанник, по средней линии, между черпало-надгортанными складками, находясь в проекции голосовой щели. На вдохе фибробронхоскоп плавно продвигался между голосовыми связками через основание треугольника, который они образуют. Продвижение аппарата не форсировалось, дабы не травмировать голосовые связки.
Общепринятый метод санационной фибробронхоскопии под местной анестезией в клинике модифицирован. Процедура начиналась с аспирации содержимого бронхов с помощью электровакуумного отсоса с хорошим разрежением через канал фибробронхоскопа. Аспирация, как и санация, начиналась с более поражённой стороны. После аспирации проводились инстилляции через канал фибробронхоскопа раствора физиологии или фурацилина, подогретых до температуры тела в количестве до 8-10 мл за одно введение в главные и долевые бронхи для удаления мокроты с поверхности слизистой оболочки. Предварительная санация продолжалась до очищения поверхности слизистой оболочки бронхов от слизисто-гнойной мокроты, до уровня устьев сегментарных бронхов. Объём вводимого промывного раствора доходил до 80,0 мл. После чего следовала дополнительная анестезия 2% раствором лидокаина по 6,0 мл в каждое бронхиальное дерево при наличии мокроты с обеих сторон. В дальнейшем проводилась непосредственно санационная фибробронхоскопия.
Наличие слизисто-гнойной или гнойной мокроты было показанием к, когда фибробронхоскоп вводился в каждый сегментарный бронх, и проводилась инстилляция антисептиков в количестве 10-20 мл за одно введение.
После общей санации бронхиального дерева проводилась проточная санация полости деструкции легкого через ранее установленный катетер-микроирригатор.
Основываясь на данных рентгенологического обследования и наличие в дренирующем бронхе катетера, катетер постепенно продвигали в дистальном направлении бронха до упора и начинали проточную санацию. При проточной санации хорошо отмывалось содержимое полости. Когда вводимый раствор отмывал мокроту с помощью активной аспирации, эвакуировалось содержимое бронхов через инструментальный канал. Просвет между инструментальным каналом фибробронхоскопов «Оlimpus» BF XT40, BF 1T20 и катетером позволял проводить постоянную аспирацию промывных вод бронхов. Для хорошей санации бронхиального дерева под местной анестезией использовалось 120 мл и до 800 мл антисептического раствора. Проточная санация полости деструкции заканчивалась тщательной аспирацией промывных вод из просвета бронхов, включая субсегменты, что предотвращала кратковременные подъемы температуры тела до 38-39°. По катетеру в деструктивную полость легкого вводились антибактериальные средства согласно чувствительности микрофлоры.
Оценка бронхиального содержимого по данным фибробронхоскопии показала, что удельный вес слизисто-гнойной мокроты до лечения среди больных основной группы был меньше
на 23,4% (р<0,01), чем в группе сравнения.
Различия частоты других по характеру видов содержимого бронхов до лечения между основной группой и группой сравнения были статистически не значимыми.
Проведенное лечение в основной группе больных привело к уменьшению частоты гнойного содержимого в бронхах на 18,4% (р<0,05), слизисто-гнойного содержимого – на 23,3% (р<0,01). В целом число больных в это группе без содержимого в бронхах увеличилось на 30% (р<0,001).
В группе сравнения статистически значимых изменений по характеру содержимого в бронхиальном дереве не произошло.
После лечения число больных без патологического содержимого в бронхах в основной группе стало больше, чем в группе сравнения на 23,4% (р<0,001), а число больных гнойной мокротой – меньше на 23,6% (р<0,001).
По данным фибробронхоскопии до лечения характер слизистой оболочки бронхов в обеих анализируемых группах был одинаковым.
После лечения в основной группе больных с отеком и диффузной гиперемией 2 и 3 степеней слизистой оболочки бронхов изменении такой степени исчезли, хотя до лечения они отмечались у 60% больных. Число больных с бледно-розовой слизистой оболочкой увеличилось на 41,7% (р<0,001), а очаговой гиперемией 1 степени – на 20% (р<0,01).
У больных группы сравнения число больных с отеком и диффузной гиперемией 3 степени после лечения уменьшилось на 28,8% (р<0,001). При этом выросло число лиц с отеком и диффузной гиперемией 1 степени на 11,7% (р<0,05). Количество больных с бледно-розовой слизистой оболочкой бронхов увеличилось лишь на 11,7% (р<0,05).
У больных, у которых применялась в лечении посегментарно-субсегментарная санация бронхиального дерева при острых гнойных деструкциях легких количество осложнений было меньше, чем в группе сравнения на 30,0% (р<0,001), прежде всего за счет легочных кровотечений – на 9,0% (р<0,01), серозного плеврита – на 3,3% (р<0,05), контрлатеральной пневмонии – на 6,0% (р<0,01).
В основной группе больных реже на 58,0%, чем в группе сравнения пришлось применять методы хирургического дренирования и вскрытия гнойников в грудной полости и флегмоны груди.
У больных основной группы реже на 18,6% (р<0,01) выполнялось дренирование плевральной полости, на 35,0% (р<0,001) – плевральная пункция.
В основной группе больных реже на 9,0% (р<0,05), чем в группе сравнения в комплексном лечении применялись оперативные вмешательства.
Пневмонэктомия и лобэктомия выполнялись только в группе сравнения, соответственно у 3,3% и 4,7% (р<0,01).
Из 21 больных группы сравнения, у которых выполнялись операции, послеоперационные осложнения возникли у 11 (52,4%) пациентов, в том числе эмпиема плевры (3 случая; 2,0%), внутриплевральное кровотечение (3 случая; 2,0%), несостоятельность культи бронха (2 случая; 1,3%), остеомиелит ребра (2 случая; 1,3%), нагноение послеоперационной раны (1 случай; 0,7%).
В основной группе больных было прооперировано всего 3 больных. Послеоперационных осложнений у них не отмечено.
Полное выздоровление у больных основной группы было достигнуто у 36,7% больных (таблица 1), а у пациентов группы сравнения – на 27,4% реже (р<0,001). Переход процесса в хронический в основной группе наблюдался реже на 12% (р<0,01). Летальность в основной группе была меньше, чем в группе сравнения на 8,3% (р<0,01).
Таблица 1. Исходы лечения больных острым абсцессом и гангреной легких
|
Исход лечения |
Все больные |
Группа больных |
|||||
|
основная |
сравнения |
Р |
|||||
|
абс. число |
% |
абс. число |
% |
абс. число |
% |
||
|
Полное выздоровление |
36 |
17,1 |
22 |
36,7 |
14 |
9,3 |
<0,001 |
|
Клиническое выздоровление (пневмосклероз) |
76 |
36,2 |
22 |
36,7 |
54 |
51,9 |
<0,05 |
|
Клиническое выздоровление (ОПП) |
31 |
14,8 |
7 |
11,7 |
24 |
16,0 |
>0,1 |
|
Улучшение |
26 |
12,4 |
6 |
10,0 |
20 |
13,3 |
>0,05 |
|
Переход процесса в хронический |
25 |
11,9 |
2 |
3,3 |
23 |
15,3 |
<0,01 |
|
Летальность |
18 |
7,6 |
1 |
1,7 |
15 |
10,0 |
<0,01 |
|
Всего: |
210 |
100,0 |
60 |
100,0 |
150 |
100,0 |
|
Клапанная бронхоблокация ”свищевого” бронха у больных с пиопневмотораксом применена в комплексном лечении 43 пациентов (первая группа). Для клапанной бронхоблокации использовался эндобронхиальный обратный клапан конструкции А.В. Левина.
Локализация бронхоплевральных свищей чаще всего была в нижних долях правого и левого легких (таблица 2). По их локализации обе группы были сопоставимы.
Таблица 2. Локализация бронхоплеврального свища у больных с пиопневмотораксом
|
Локализация бронхоплеврального свища |
Все больные (n–110) |
Группа больных |
|||||
|
первая (n-43) |
вторая (n–67) |
Р > |
|||||
|
абс. число |
% |
абс. число |
% |
абс. число |
% |
||
|
Справа |
|||||||
|
Верхняя доля |
3 |
2,7 |
2 |
4,6 |
1 |
1,5 |
0,05 |
|
Средняя доля |
8 |
7,3 |
5 |
11,6 |
3 |
4,5 |
0,05 |
|
Промежуточный бронх |
10 |
9,1 |
3 |
7,0 |
7 |
10,4 |
0,05 |
|
Нижняя доля |
44 |
40,0 |
18 |
41,9 |
26 |
38,8 |
0,05 |
|
Культя главного бронха |
5 |
4,5 |
1 |
2,3 |
4 |
6,0 |
0,05 |
|
Слева |
|||||||
|
Верхняя доля |
7 |
6,4 |
3 |
7,0 |
4 |
6,0 |
0,05 |
|
Нижняя доля |
33 |
30 |
11 |
25,6 |
22 |
32,8 |
0,05 |
Включение в комплексное лечение острого пиопневмоторакса клапанной бронхоблокации «свищевого» бронха способствовало увеличению частоты ликвидации остаточной плевральной полости на 39,7% (р<0,001), уменьшало частоту инфильтрации и деструкции легочной ткани на 47,1% (р<0,001), снижению длительности пребывания в стационаре – на 8,3 койко-дня (р<0,05).
На 18-21 день наблюдения с момента бронхоблокации боль в груди в этой группе отмечалась реже на 22,7% (р<0,02), кашель – на 22,6% (р<0,02), чаще наблюдалось удовлетворительное состоянии – на 32,8% (р<0,001), выше уровень гемоглобина – на 11,73 г/л (р<0,01), показатель гематокрита – на 3,19% (р<0,02).
Результаты лечения оценивались следующим образом (таблица 3)
- полное выздоровление - достижение полного клинического эффекта в лечении пиопневмоторакса: закрытие полости и ликвидацию бронхиального свища, отсутствие выраженных клинико-рентгенологических последствий заболевания;
- клиническое выздоровление - отсутствие клинических проявлений заболевания, закрытие полости пиопневмоторакса с ликвидацией бронхоплеврального сообщения, сохранение значимых пневмоцирротических изменений и выраженные фибринозных наложений на париетальной плевре;
- улучшение - купирование острого воспалительного процесса и формирование хронической эмпиемы плевры с бронхоплевральным свищом;
- летальный исход – в период пребывания в стационаре.
Таблица 3. Результаты комплексного лечения пациентов с пиопневмотораксом
|
Результат |
Все больные (n–110) |
Группа больных |
|||||
|
первая (n-43) |
вторая (n–67) |
Р |
|||||
|
абс. число |
% |
абс. число |
% |
абс. число |
% |
||
|
Полное выздоровление |
41 |
37,3 |
22 |
51,2 |
19 |
28,4 |
<0,05 |
|
Клиническое выздоровление |
32 |
29,1 |
15 |
34,9 |
17 |
25,3 |
>0,05 |
|
Улучшение |
34 |
29,1 |
5 |
11,6 |
27 |
40,3 |
<0,001 |
|
Летальный исход |
5 |
4,5 |
1 |
2,3 |
4 |
5,9 |
>0,05 |
В результате комплексного лечения пиопневмоторакса у пациентов основной группы полное и клиническое выздоровление наступало чаще, чем в группе сравнения на 32,4% (р<0,001), в том числе полное выздоровление – на 22,8% (р<0,05).
Заключение
При применении в комплексном лечении посегментарно-субсегментарной санации бронхов количество осложнений у больных острым абсцессом и гангреной легких уменьшилось на 30%, частота применения оперативных методов лечения уменьшалась на 9,0%, увеличивалось число больных с полным выздоровлением – на 27,4% и уменьшалась частота перехода процесса в хронический на 12,0%, а летальность снижалась на 8,3%.
Использование клапанной бронхоблокации у больных пиопневмотораксом с бронхиальным свищем увеличивало число лиц с полным выздоровлением на 28,8%, частоту ликвидации остаточной плевральной полости – на 39,7%, уменьшало частоту инфильтрации и легочной деструкции – на 47,1%.
Рецензенты:
Лубянский В.Г., д.м.н., профессор, зав. кафедрой госпитальной хирургии, ГБОУ ВПО АГМУ Минздрава России, г. Барнаул.
Цеймах Е.А., д.м.н., профессор, зав. кафедрой оперативной хирургии и топографической анатомии, ГБОУ ВПО АГМУ Минздрава России, г. Барнаул.
Библиографическая ссылка
Капитулин С.Ю., Сыздыкбаев М.К., Куртуков В.А., Шойхет Я.Н. ВИДЕОБРОНХОСКОПИЧЕСКИЕ МЕТОДЫ В КОМПЛЕКСНОМ ЛЕЧЕНИИ ОСТРЫХ ГНОЙНЫХ ДЕСТРУКТИВНЫХ ПРОЦЕССОВ ЛЁГКИХ И ПИОПНЕВМОТОРАКСА // Современные проблемы науки и образования. 2013. № 6. ;URL: https://science-education.ru/en/article/view?id=10759 (дата обращения: 27.04.2026).



