Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
KINETICS OF TUNGSNET DISULFIDE NANOPOWDER SYNTHESIS UNDER SELF-PROPAGATING HIGH TEMPERATURE SYNTHESIS CONDITIONS
Введение
В последние годы наблюдается повышенный интерес к наноразмерным дихалькогенидам переходных металлов, в частности, к получению и исследованию физико-химических свойств наноразмерного дисульфида вольфрама. Это обусловлено как многообразием методов получения, так и морфологией и свойствами получаемых продуктов. Наносферические частицы дисульфида вольфрама, полученные гидротермальным методом [11], при добавлении в масло обладают лучшими трибологическими свойствами по сравнению с микронным порошком WS2. Сульфидирование нанопроволочек оксида вольфрама в токе сероводорода позволяет получить частицы дисульфида игольчатой структуры [10]. Каталитические свойства наночастиц WS2, полученные в результате разложения тетратиовольфрамата аммония, исследовались в работе [9]. В ряде работ показана возможность получения наноразмерных частиц дисульфида вольфрама, обладающих высокими трибологическими свойствами, методом самораспространяющегося высокотемпературного синтеза (СВС) при давлении аргона 3 МПа из наночастиц вольфрама и элементарной серы [1, 7]. В то же время остается малоизученной кинетика процесса взаимодействия исходных реагентов в условиях протекания СВС наноразмерного дисульфида вольфрама. Таким образом, целью настоящей работы является исследование кинетики взаимодействия нанопорошка вольфрама и элементарной серы в режиме самораспространяющегося высокотемпературного синтеза.
Материалы и методы исследования
Полученные методом электрического взрыва [3] и прошедшие пассивацию наночастицы вольфрама со средним размером 60 нм, смешивались с фракцией дисперсной серы не более 45 мкм. Полученная шихта компактировалась в цилиндрические образцы, которые загружались в реактор для проведения СВ-синтеза [1]. Предотвращение уноса серы через боковую поверхность образца осуществлялось за счет запрессовки его в стеклянную обойму. Инициирование процесса взаимодействия реагентов осуществлялось с помощью нагревательной спирали, соединенной с источником постоянного тока. Измерение скорости распространения волны горения проводилось на основании видеозаписи процесса синтеза с помощью скоростной видеокамеры. Количество повторений экспериментов по определению скорости горения для каждого образца составляло три. Давление аргона в реакторе варьировалось от 0,5 до 4,0 МПа, избыток серы в шихте изменялся в пределах от 0 до 20% мас. с шагом 5% мас. Для определения температуры горения использовались вольфрам-рениевые термопары из сплавов ВР-5 и ВР-20, горячий спай которых помещался в нижней части образцов.
Результаты исследования и их обсуждение
Полученная с помощью видеокамеры последовательность фотографий процесса взаимодействия прессованной стехиометрической смеси из электровзрывного нанопорошка вольфрама и элементарной серы при давлении аргона 3 МПа представлена на рисунке 1. За начальную стадию (t = 0 с) была принята стадия нагрева образца с помощью нихромовой спирали (кадр №1). На следующем кадре запечатлен момент зажигания верхнего слоя цилиндрического образца, сопровождающийся яркой вспышкой, расплавлением элементарной серы в поверхностном слое и ее испарением. После стадии инициирования следует стадия протекания экзотермической реакции (кадры №3-8) нанопорошка вольфрама с серой. Образующиеся после прохождения видимого фронта горения продукты синтеза увеличиваются в объеме в 2-3 раза, но так как расширение в радиальном направлении ограничено стенками стеклянной обоймы, то оно идет в осевом направлении вверх. Скорость горения рассчитывалась как отношение высоты таблетки ко времени полного реагирования, начиная с момента зажигания и заканчивая моментом затухания видимого фронта горения.

Рисунок 1 ‒ Фотографии процесса горения стехиометрической смеси нанодисперсного порошка вольфрама с серой (P = 3 МПа.)
Зависимость изменения скорости горения нанопорошка вольфрама с серой в интервале давлений аргона 0,5-4,0 МПа представлена на рисунке 2. Видно, что с увеличением давления скорость горения возрастает с 0,1 до 0,3 см/с. Это обусловлено тем, что увеличение давления ведет к возрастанию температуры кипения серы, более интенсивному взаимодействию горячих паров серы с поверхностью наночастиц металла, меньшему уносу серы из зоны реакции и способствует лучшей диффузии серы сквозь слои образующегося сульфида.
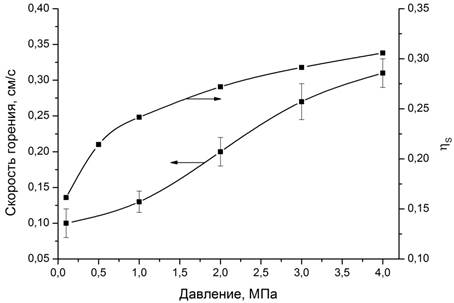
Рисунок 2 – Зависимость скорости горения и степень превращения ηs стехиометрической смеси нанопорошка вольфрама с серой от давления аргона
Согласно [5], горение в системах с легкоплавким реагентом описывается элементарной моделью горения 2-го рода. К таким системам можно отнести смесь дисперсного вольфрама с серой, при этом скорость горения вольфрама с серой определяется расчетной степенью превращения ηs и температурой Ts на поверхности, отделяющей участки смеси с жидким и газообразным компонентами и характеризующейся условиями ηs < 1, Ts < Tmax, где Tmax – максимальная температура горения. Температура этой поверхности в смеси W+S равна температуре кипения серы, зависящей от давления. Степень превращения на поверхности определяется по формуле:
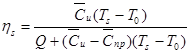 , (1)
, (1)
где ![]() ,
, ![]() – средняя теплоемкость исходных веществ и продуктов в интервале температур T0 – Ts и определяется по выражению
– средняя теплоемкость исходных веществ и продуктов в интервале температур T0 – Ts и определяется по выражению 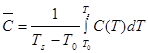 ; Q – тепловой эффект реакции, рассчитанный на 1 моль продукта. Значение теплового эффекта образования дисульфида вольфрама, по данным [8], составляет ‒ 240,8 кДж/моль.
; Q – тепловой эффект реакции, рассчитанный на 1 моль продукта. Значение теплового эффекта образования дисульфида вольфрама, по данным [8], составляет ‒ 240,8 кДж/моль.
Для стехиометрической смеси вольфрама с серой степень превращения будет определяться температурой Ts и средней теплоемкостью компонентов. Температура кипения серы в зависимости от давления определялась интерполированием значений, представленных в [4, 6]. Рассчитанные значения степени превращения ηS представлены на рисунке 2. Как показано в [2], при синтезе наноразмерного дисульфида молибдена при давлении аргона более 4,0 МПа наблюдается резкое увеличение скорости горения без существенного увеличения степени превращения, что делает нецелесообразным проведение синтеза при большем давлении аргона.
На втором этапе исследовалось влияние избытка серы в шихте на скорость горения и степень превращения реагентов при постоянном давлении газа. Давление аргона в реакторе для синтеза всех образцов было выбрано 3 МПа. Зависимость скорости и максимальной температуры горения от избытка серы представлена на рисунке 3.
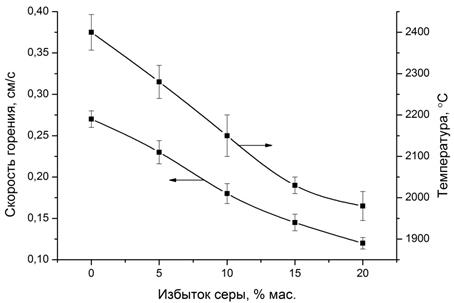
Рисунок 3 – Зависимость скорости и максимальной температуры горения от избытка серы в смеси с нанопорошком вольфрама (P = 3 МПа)
Увеличение избытка серы приводит к снижению скорости и максимальной температуры горения нанопорошка вольфрама с серой вследствие разбавления избыточной серой, что ведет к расходованию выделяемого в процессе синтеза дисульфида тепла на плавление и испарение избыточной серы, согласно уравнению (2):
![]() (2)
(2)
где Qстех. – тепловой эффект реакции; nSстех., nMeстех. – массовые доли исходных веществ в стехиометрическом соотношении; C(S)‒ средняя теплоемкость серы; nSост. – массовая доля остаточной серы; Qкип(S), Qисп(S) – теплота кипения и испарения серы соответственно.
При этом степень превращения на поверхности ηs при постоянном давлении будет определяться изменением теплового эффекта (рисунок 4).
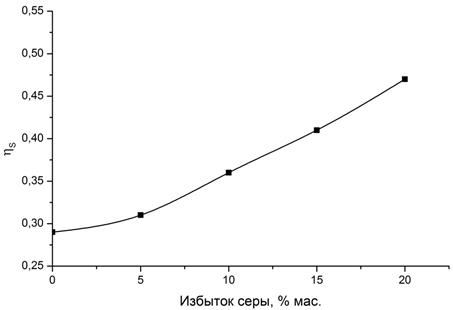
Рисунок 4 – Зависимость степени превращения реагентов при СВС дисульфида вольфрама от избытка серы в шихте (P = 3 МПа)
Для моделей горения 2-го рода скорость горения определяется следующим уравнением [5]:
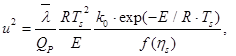 (3)
(3)
где ![]() – эффективное значение теплопроводности; QP ‒ тепловой эффект реакции; k0 и E – предэкспоненциальный фактор и энергия активации реакции соответственно.
– эффективное значение теплопроводности; QP ‒ тепловой эффект реакции; k0 и E – предэкспоненциальный фактор и энергия активации реакции соответственно.
При TS = Tкип = const выражение (3) будет иметь вид ![]() . Зависимость
. Зависимость ![]() на основании рисунков 3-4 для системы W+S аппроксимируется выражением
на основании рисунков 3-4 для системы W+S аппроксимируется выражением ![]() (рисунок 5, а), что соответствует параболическому закону окисления [5].
(рисунок 5, а), что соответствует параболическому закону окисления [5].
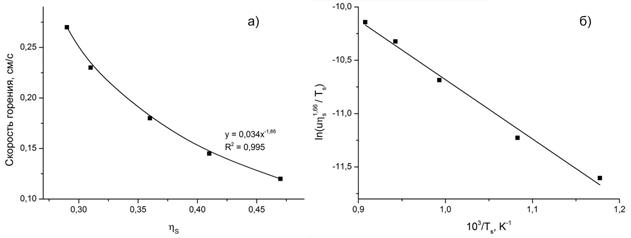
Рисунок 5 ‒ Зависимость скорости горения от степени превращения (а) и зависимость ln(u·f(ηs)/Ts) от 1/Ts (б) при СВС дисульфида вольфрама (P = 3 МПа)
Полученная зависимость скорости горения нанопорошка вольфрама с серой от давления (рисунок 2) для модели горения 2-го рода равносильна зависимости от температуры Ts кипения серы, что при известном кинетическом законе взаимодействия и расчетном значении ηs, позволяет, согласно [2], определить энергию активации процесса по углу наклона прямой, построенной в координатах ![]() . Найденное значение энергии активации для системы W+S на основании зависимости, приведенной на рисунке 5, б, составляет 90,1 кДж/моль, что, согласно ранее полученным значениям энергии активации процесса синтеза сульфидов молибдена, железа и цинка [2, 4] говорит о переходной области протекания процесса, осложненной диффузией серы через слои образующихся сульфидов. Таким образом, исходя из значения энергии активации, процесс синтеза наноразмерного дисульфида вольфрама зависит также от степени уплотненности шихты в исходной таблетке, т.е. от эффективной площади контакта между наночастицами вольфрама и элементарной серы.
. Найденное значение энергии активации для системы W+S на основании зависимости, приведенной на рисунке 5, б, составляет 90,1 кДж/моль, что, согласно ранее полученным значениям энергии активации процесса синтеза сульфидов молибдена, железа и цинка [2, 4] говорит о переходной области протекания процесса, осложненной диффузией серы через слои образующихся сульфидов. Таким образом, исходя из значения энергии активации, процесс синтеза наноразмерного дисульфида вольфрама зависит также от степени уплотненности шихты в исходной таблетке, т.е. от эффективной площади контакта между наночастицами вольфрама и элементарной серы.
Выводы
Увеличение давления синтеза до 4 МПа приводит к возрастанию скорости горения при СВ-синтезе наноразмерного дисульфида вольфрама до 0,3 см/с.
Увеличение избытка серы в шихте с 0 до 20% мас. при давлении 3 МПа снижает скорость горения нанопорошка вольфрама с серой с 0,27 до 0,12 см/с вследствие снижения максимальной температуры горения и общего торможения реакции, вызванного расходованием теплоты на нагрев и испарение избыточной серы.
Зависимость скорости горения от расчетной степени превращения ηS при взаимодействии нанопорошка вольфрама с элементарной серой описывается уравнением ![]() , что соответствует параболическому закону окисления.
, что соответствует параболическому закону окисления.
Значение энергии активации процесса взаимодействия нанопорошка вольфрама с серой составляет 90,1 кДж/моль, что указывает на одновременное лимитирование скорости процесса за счет химической реакции и диффузии серы через слои образующихся сульфидов.
Рецензенты:
Сваровский А.Я., д.т.н., профессор Северского технологического института Национального исследовательского ядерного университета «МИФИ», г. Северск.
Погребенков В.М., д.т.н., профессор, заведующий кафедрой технологии силикатов и наноматериалов Института физики высоких технологий НИ ТПУ, г. Томск.
Библиографическая ссылка
Иртегов Ю.А., Ажгихин М.И., Коробочкин В.В. КИНЕТИКА ПРОЦЕССА СИНТЕЗА НАНОРАЗМЕРНОГО ДИСУЛЬФИДА ВОЛЬФРАМА В УСЛОВИЯХ САМОРАСПРОСТРАНЯЮЩЕГОСЯ ВЫСОКОТЕМПЕРАТУРНОГО СИНТЕЗА // Современные проблемы науки и образования. 2013. № 5. ;URL: https://science-education.ru/en/article/view?id=10677 (дата обращения: 23.05.2026).



