Введение
Рубцы, являясь следствием повреждений целостности кожных покровов, таких как обширные механические травмы, глубокие ожоги, хирургические операции и тяжелые формы воспалительных дерматозов, представляют собой серьезную проблему не только медицинского, но и социального характера [1]. Высокая распространенность их среди населения обусловлена повсеместной бытовой травматизацией, а также авариями на производстве. В последние годы отмечается увеличение числа обращений в медицинские учреждения по поводу рубцов. Важно отметить, что проблема формирования рубцов выходит далеко за рамки эстетического дефекта [2]. Гипертрофические и келоидные рубцы имеют ряд клинических проявлений, таких как зуд, боль, парестезии, что зачастую в значительной степени снижает качество жизни пациентов [3]. Локализуясь вблизи суставов, рубцы, представленные разрастанием грубых коллагеновых волокон, могут сокращать объем движения в суставе, формируя тем самым контрактуры. Таким образом, наличие клинических симптомов, проявляющихся физическим дискомфортом, а также провоцирующих негативный психологический фон у пациента, дает право говорить о рубцах как о комплексной проблеме, требующей системного подхода к лечению и реабилитации [4]. Однако высокий запрос на эффективную коррекцию рубцов, имеющийся как у пациентов, так и у врачей-специалистов, до сих пор не удовлетворен в полной мере, что требует дальнейшего изучения данного вопроса и проведения дополнительных исследований. Современная медицина предлагает широкий спектр способов лечения рубцов, от неинвазивных методик до радикального лечения путем иссечения патологического участка в ходе хирургической операции [5]. Однако одним из наиболее эффективных методов лечения данной патологии, показавшим хорошие результаты, остается воздействие высокоинтенсивным лазерным излучением.
Благодаря высокой эффективности, малоинвазивности и возможности индивидуального подбора параметров лечения, лазерная терапия является одним из наиболее распространенных методов лечения рубцов различного генеза. Основной механизм терапевтического воздействия высокоинтенсивного лазерного излучения базируется на явлении селективного фототермолиза, позволяющего прицельно воздействовать на целевые хромофоры [6]. Для достижения более качественной терапии для различных видов рубцов был разработан перечень лазерных систем: аблятивные лазеры (СО2, эрбиевые лазерные системы) применяют для фракционного вапоризирования тканей рубца; неаблятивные лазерные системы (диодные, неодимовые лазерные системы) – для более глубокого воздействия на дерму в обход влияния на эпидермис; импульсные лазеры на красителях в основном используют для коагуляции сосудов, питающих гипертрофические или келоидные рубцы, ограничивая их дальнейшую пролиферацию [7–9]. Комплексная терапия лазерными системами направлена на ограниченную травматизацию и локальную активацию репаративных процессов в дерме, приводящих к ее реорганизации [10, 11]. Основными процессами, формирующими благоприятный исход терапии, являются стимуляция активности клеток фибробластического дифферона, регресс сформированного неорганизованного коллагенового матрикса и синтез нового коллагена с тенденцией к восстановлению нативной конфигурации волокон. Одновременно при коагуляции избыточного капиллярного русла происходит уменьшение кровообращения в месте воздействия, а также снижение скорости патологического роста соединительной ткани. Таким образом, воздействуя на патофизиологические процессы, формирующие рубцовый дефект, лазерная терапия помогает не просто камуфлировать эстетический дефект, а решает проблему глубоким ремоделированием тканей [12].
Однако, несмотря на эффективность проведения терапии и большое количество различных методик и протоколов лечения, остается большой пласт методологических проблем, связанных с оценкой результатов, верификацией степени эффективности. Традиционно оценка состояния рубцового дефекта проводится путем физикального обследования, данных осмотра в рамках субъективных шкал, таких как шкала оценки рубцов наблюдателем POSAS или модифицированная Ванкуверская шкала. Однако, несмотря на их высокую клиническую значимость для динамического контроля состояния рубца как врачами, так и самими пациентами, данные шкалы позволяют оценить лишь макроскопические видимые изменения (цвет, плотность, рельеф, васкуляризация) и зависят от субъективного восприятия лица, проводящего оценку. В результате положительная динамика, наблюдаемая in vivo, не находит точного количественного отображения, а также не отражает структурно-клеточные изменения в ходе лечения. Таким образом, складывается ситуация, в которой положительный эффект наиболее часто применимого метода лечения оценивается по большей части при помощи субъективных шкал без уделения внимания контролю изменений на клеточно-тканевом уровне. Противоречие в вопросе верификации эффективности методики проводимой терапии подчеркивает актуальность изучения новых протоколов оценки динамики микроскопических изменений, призванных закрыть пробелы в вопросах контроля качества оказания медицинской помощи.
В качестве методики, используемой для преодоления методологического разрыва, наиболее вероятно использование гистологического исследования микропрепаратов рубца [13]. Гистологические исследования широко применяются в дерматологической практике как в диагностических целях, так и для оценки результатов проведенного лечения. Данная методика может по праву считаться «золотым стандартом» оценки микроскопических изменений, так как позволяет в полной мере оценить архитектонику внеклеточного матрикса, соотношение и количественный состав клеточно-дифферонного компонента дермы, а также другие морфометрические характеристики тканей исследуемых образцов. В контексте данного исследования морфометрия является ключевой методикой определения динамики параметров дермы, таких как глубина, процент содержания неорганизованного коллагена, удельная площадь участков импрегнации экзогенным пигментом. Особенно актуально применение данной методики для изучения рубцов, содержащих импрегнацию, для фиксации количественного параметра размерности их площади. Таким образом, гистоморфометрический анализ ткани не только позволяет констатировать факт положительной динамики, но и дает возможность детально описать, за счет каких механизмов произошли те или иные изменения.
Цель исследования – оценка динамики архитектоники межклеточного матрикса дермы рубцов кожи до и после проведения высокоинтенсивной лазерной терапии.
Для достижения целей в ходе работы были поставлены следующие задачи: произвести биопсию материала для последующего приготовления гистологических препаратов; выполнить морфометрический анализ показателей дермы до и после проведения лазерной терапии; провести статистический анализ полученных данных для выявления статистически значимых различий; сформировать выводы об эффективности проведения лазерной терапии для лечения рубцов с гистологической точки зрения. Гипотеза исследования базируется на тезисе о положительном статистически значимом сдвиге морфометрических параметров дермы рубцов в результате проведения лазерной терапии, который свидетельствует о ее более организованном и зрелом состоянии. Научная новизна работы заключается в комплексной оценке параметров дермы с применением различных методик гистологического окрашивания. Практическая значимость полученных результатов состоит в представлении фундаментальных основ лечения рубцовых дефектов различной этиологии при помощи лазерных систем, направленных на достижение того или иного результата.
Материал и методы исследования
Для исследования проводили забор биоптата у пациентов, поступивших в клинику кожных и венерических болезней с диагнозом «посттравматические рубцы кожи лица». Все пациенты подписывали добровольное согласие. Курс высокоинтенсивного лазерного воздействия выполнялся при помощи следующих лазерных аппаратов: «Fotona SP Dynamis», Fotona StarWalker® MaQX и Q-MASTER PLUS Q-SWITCHED LONG PULSED ND:YAG LASER. Забор биоптата проводился в очаге поражения и в подбородочной области (после чего пациентам накладывали косметический шов). Биопсийный материал фиксировали в 10%-ном нейтральном забуференном формалине до 24 ч, потом проводили через процессор карусельного типа Microm TP120-3 в девяти емкостях с абсолютизированным изопропиловым спиртом по 2,5 ч в каждой и в трех емкостях с расплавленным парафином при температуре 58–60°С в течение 2,5 ч в каждой. Затем материал заливали в парафин с использованием заливочной станции Microm EC350-1. Готовые блоки охлаждали на специальном столике Microm EC 350-2, окрашивали гематоксилином, эозином и кислым фуксином в сочетании с пикриновой кислотой по методу Ван-Гизона для визуализации коллагеновых волокон экстрацеллюлярного матрикса по стандартной методике.
Из каждого парафинового блока было изготовлено по 10 гистологических срезов. Изготовленные срезы изучали в светлом поле с использованием цифрового сканера микропрепаратов 3DHISTECH PANNORAMIC Midi. Полученные цифровые изображения микропрепаратов обрабатывались в лицензионной программе 3DHISTECH «SLIDE VEWER» с использованием опций, позволяющих производить подсчет удельной площади, оценивать длину выделенных объектов, а также осуществлять изменение цвето-графических показателей установленных маркеров. В ходе проведения морфометрического исследования измерялись следующие параметры: глубина дермы от базальной мембраны эпидермиса до гиподермы; процентное соотношение площади, занимаемой неорганизованными пучками коллагеновых волокон, к организованной части межклеточного матрикса на отдельно взятом участке. Также на препаратах посттравматических рубцов, имеющих импрегнацию, исследовались размер участков скопления пигмента, глубина и широта зоны его распределения. Полученные данные подвергались статистической обработке с использованием программы STATISTIKA 10.0. Для каждого исследуемого показателя выбиралось 10 размерных параметров, на основе которых вычислялась медиана, Q1(25%) и Q3(75%), IQR.
Результаты исследования и их обсуждение
Для проведения анализа архитектоники соединительной ткани рубцов была оценена динамика изменения толщины слоя дермы, а также изменение соотношения визуально не организованных волокон межклеточного матрикса на единицу площади ткани.
Полученные результаты представлены отдельно для рубцов, имеющих признаки посттравматической импрегнации, и для рубцов, свободных от пигмента. Также в ходе исследования производились замеры указанных показателей в интактной дерме (рис.1 и 2).
|
|
|
|
|
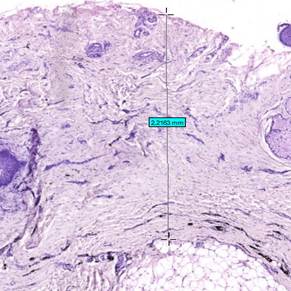
Рис.1. Измерение глубины слоя дермы рубца до проведения лазерной терапии. Окраска: гематоксилин + эозин. Ув. х5. Примечание: составлен авторами по результатам данного исследования
|
|
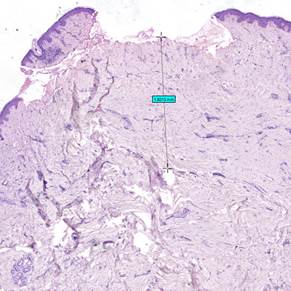
Рис.2. Измерение глубины слоя дермы рубца после проведения лазерной терапии Окраска: гематоксилин + эозин. Ув. х5. Примечание: составлен авторами по результатам данного исследования |
Полученные данные продемонстрировали стойкую тенденцию к уменьшению толщины дермы на препаратах посттравматических рубцов с элементами импрегнации (табл.1) [13]. Так, в паре препаратов №1 при сравнении выявилось снижение толщины дермы на 28,84%, что явилось статистически значимым изменением (p=0,005). Схожая картина наблюдалась в паре №3: регресс толщины дермы составил 30,4% (p=0,005). В паре №2, несмотря на тенденцию к снижению толщины дермы, статистически значимых различий получено не было (p=0,074).
Таблица1
Толщина дермы рубцов у пациентов с посттравматическими рубцами кожи лица
|
№п/п |
Медиана, мкм |
Q1 (25%), мкм |
Q3 (75%), мкм |
IQR |
∆,% |
p-критерий# |
p-критерий* |
|
1 |
2384,6 |
2164,7 |
2558,1 |
393,4 |
26,8
|
0,005
|
0,092 |
|
1' |
1744,6 |
1539,8 |
1799,3 |
259,5 |
0,168 |
||
|
2 |
996,45 |
825 |
1097,8 |
272,8 |
27,9
|
0,074
|
0,005 |
|
2' |
718,9 |
486,5 |
822,9 |
336,4 |
0,074 |
||
|
3 |
715,75 |
702,4 |
738,2 |
35,8 |
30,4
|
0,005
|
0,005 |
|
3' |
498,15 |
454,9 |
500,3 |
45,4 |
0,0044 |
||
|
4 |
1281,5 |
1113,5 |
1333,7 |
220,2 |
50,2
|
0,005
|
0,0044 |
|
4' |
638,5 |
535,5 |
772,1 |
236,6 |
0,0044 |
||
|
5 |
800,9 |
726,5 |
814,4 |
87,9 |
25,9
|
0,005
|
0,0044 |
|
5' |
593,6 |
528,9 |
683,7 |
154,8 |
0,005 |
||
|
Контроль |
1847,2 |
1664 |
1925,4 |
261,4 |
|
|
|
|
Среднее значение ∆, % |
|
|
|
32,2 |
|
|
Примечание:
1–5 – препараты до проведения терапии; 1'–5' – препараты после проведения терапии;
# – критерий значимости изменений после проведения ВИЛТ;
* – критерий значимости изменений морфометрических показателей в сравнении с показателями интактной кожи;
∆,% – относительное изменение показателя после лечения в процентах.
Составлена авторами на основе полученных данных в ходе исследования
Препараты, не имеющие импрегнации, исследовались по схожему алгоритму (пары №4 и5). Наибольший регресс толщины дермы наблюдался в паре препаратов №4 и составил 50,17% (p=0,005). Изменения в паре №5 также являются статистически значимыми (p=0,005) и составляют 25,88%.
На препаратах, окрашенных кислым фуксином и пикриновой кислотой по методу Ван-Гизона (рис.3 и 4).
|
|
|
|
|
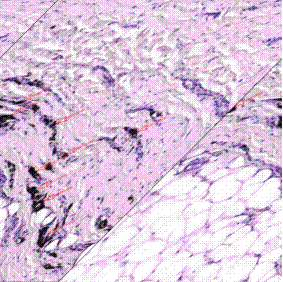
Рис.3. Коллагеновые пучки в дерме рубца до проведения лазерной терапии. Окраска: кислый фуксин + пикриновая кислота (по методу Ван-Гизона). Ув.: 5. Желтыми стрелками показаны дефекты архитектоники в виде визуально неорганизованных утолщенных волокон коллагена. Примечание: составлен авторами по результатам данного исследования
|
|
Рис.4. Коллагеновые пучки в дерме рубца после проведения лазерной терапии. Окраска: кислый фуксин + пикриновая кислота (по методу Ван-Гизона). Ув.: |
Для выявления коллагеновых волокон в экстрацеллюлярном матриксе было оценено и проанализировано соотношение участков визуально организованных пучков волокон коллагена и визуально анизотропных участков. Данные, полученные в ходе исследования процентной доли, занимаемой визуально неорганизованным коллагеном от произвольной площади дермы, представлены в табл.2. Подобный метод подсчета позволяет нивелировать особенности индивидуального течения формирования рубцов. Таким образом, наиболее яркие результаты динамики исследуемого показателя наблюдаются в случаях 1 и 3 в группе с импрегнацией. В паре №1 процент снижения составил 56,5% (p=0,005), в паре №2 – 61,1% (p=0,005), в паре №3 также наблюдается снижение процентного соотношения на 56% (p=0,004), что является статистически значимой динамикой во всех случаях.
Таблица2
Процентное соотношение неорганизованного коллагена в дерме рубцов у пациентов с посттравматическими рубцами кожи лица
|
№п/п |
Медиана, мкм |
Q1 (25%), мкм |
Q3 (75%), мкм |
IQR |
∆,% |
p-критерий# |
p-критерий* |
|
1 |
55,207 |
46,845 |
68,842 |
21,997 |
56,5
|
0,005
|
0,0051 |
|
1' |
24,042 |
16,609 |
26,435 |
9,8256 |
0,0069 |
||
|
2 |
61,134 |
46,509 |
72,745 |
26,236 |
61,1
|
0,005
|
0,0051 |
|
2' |
23,786 |
19,977 |
28,333 |
8,3561 |
0,0069 |
||
|
3 |
67,669 |
61,771 |
72,736 |
10,965 |
56,0
|
0,004
|
0,0051 |
|
3' |
29,779 |
25,792 |
36,192 |
10,4 |
0,0125 |
||
|
4 |
56,734 |
47,526 |
63,166 |
15,639 |
51,9
|
0,005
|
0,0051 |
|
4' |
27,278 |
24,377 |
32,034 |
7,6574 |
0,0069 |
||
|
5 |
68,055 |
59,396 |
74,516 |
15,12 |
67,3
|
0,005
|
0,0051 |
|
5' |
22,266 |
19,97 |
29,011 |
9,041 |
0,0218 |
||
|
Контроль |
13,106 |
10,5 |
14,146 |
3,6459 |
|
|
|
|
Среднее значение ∆, % |
|
|
|
|
58,56 |
|
|
Примечание:
1–5 – препараты до проведения терапии; 1'–5' – препараты после проведения терапии;
# – критерий значимости изменений после проведения ВИЛТ;
* – критерий значимости изменений морфометрических показателей в сравнении с показателями интактной кожи.
∆,% – относительное изменение показателя после лечения в процентах.
Составлена авторами на основе полученных данных в ходе исследования
Препараты, не имеющие импрегнации, исследовались по схожему алгоритму (табл.2). Наибольший регресс толщины дермы наблюдался в паре препаратов №4 и составил 50,17% (p=0,005). Изменения в паре №5 также являются статистически значимыми (p=0,005) и составляют 25,88%.
Во второй группе препаратов (пары №4 и №5) динамика изменения процентного соотношения визуально неорганизованного коллагена в дерме рубцов без импрегнации свидетельствует о высокой эффективности терапии. Так, в паре образцов №4 процент регресса составил 51,9% (p=0,005), что близко к показателям, полученным при лечении рубцов с импрегнацией. В паре №5 зафиксированы самые высокие результаты терапии – 67,2% (p=0,005).
При анализе данных, полученных при оценке влияния терапии высокоинтенсивным лазерным излучением, была выявлена явная тенденция к восстановлению изотропной конфигурации пучков коллагеновых волокон в межклеточном веществе дермы рубцов с импрегнацией экзогенным пигментом и дермы рубцов без импрегнации.
Еще одним числовым показателем, исследуемым на препаратах дермы посттравматических рубцов, была динамика удельной площади участков импрегнации (табл.3). Оценивались наиболее крупные участки импрегнации (рис.5).
|
|
|
|
Рис.5. Участки импрегнации в дерме рубца до проведения лазерной терапии Окраска: гематоксилин + эозин; красными стрелками указаны наиболее крупные участки импрегнации. Ув. х10. Примечание: составлен авторами по результатам данного исследования
|
|
Участки импрегнации были распределены на три группы: крупные, средние и малые. При оценке данного параметра размерности устанавливались относительно полученных данных для каждого препарата индивидуально для нивелирования индивидуальной изменчивости образцов и широких границ вариативности размера частиц пигмента.
Таблица3
Качественная характеристика изменения размеров участков импрегнации
|
№п/п |
Площадь малых участков, мкм² |
Площадь средних участков, мкм² |
Площадь крупных участков, мкм² |
|||
|
|
До ВИЛТ |
После |
До ВИЛТ |
После |
До ВИЛТ |
После ВИЛТ |
|
1 |
281,70±32,34 |
170,83±118,3 |
956,20±99,14 |
0 |
7230,77±555,42 |
0 |
|
2 |
456,30±55,97 |
78,57±14,83 |
693,27±47,84 |
137,50±8,99 |
1132,57±257,08 |
311,00±97,21 |
|
3 |
22,07 |
6,03 |
100,03±26,36 |
32,57 |
249,27±3,05 |
0 |
Примечание: составлена авторами на основе полученных данных в ходе исследования
Морфометрический анализ показал наибольшее уменьшение количества пигмента в дерме за счет деструкции и элиминации наиболее крупных участков импрегнации. Уменьшение площади крупных участков составило: в паре №1 – 100%; в паре №2 – 72,5%; в паре №3 – 100%. Аналогичная тенденция зафиксирована для средних и малых по площади участков импрегнации.
Площадь средних участков уменьшилась в паре №1 на 100%, в паре №2 – на 80,2%, в паре №3 – на 67,5%. Для малых участков уменьшение площади, занимаемой участками импрегнации, составило: для пары №1 – 39,4%; для пары №2 – 82,8%; для пары №3 – 72,7%. Важно отметить, что в паре №1 терапия привела к полному исчезновению средних и крупных патологических структур, что свидетельствует о высокой эффективности примененного метода воздействия именно на грубые, сформированные дефекты внеклеточного матрикса.
Таким образом, морфометрический анализ препаратов дермы рубцов с импрегнацией однозначно демонстрирует, что высокоинтенсивная лазерная терапия приводит к значительному уменьшению площади и последующему исчезновению участков импрегнации в дерме как посттравматических рубцов, так и рубцов с исходной импрегнацией, что морфологически проявляется в ремоделировании и оптимизации структуры соединительной ткани, что находит свое подтверждение в литературе [14, 15].
Заключение
Проведя анализ данных, полученных в ходе гистоморфометрического исследования, можно сделать вывод об эффективности применения высокоинтенсивной лазерной терапии в рамках терапии посттравматических рубцов, что подтверждается динамикой параметров дермы, фиксируемых на тканевом уровне. Основными изменениями являются изменения в межклеточном матриксе, а именно изменение толщины дермы, соотношения визуально организованных пучков коллагеновых волокон и участков ткани, сохранивших нативную архитектонику. Также об эффективности воздействия свидетельствует значимый регресс площади скопления экзогенного пигмента. Однако ряд ограничений исследования, таких как небольшая выборка исследуемого материала и субъективная оценка некоторых параметров, формируют потребность в продолжении и развитии исследований в вопросах гистоморфометрической оценки терапии посттравматических рубцов.
Конфликт интересов
Финансирование
Библиографическая ссылка
Шанина Н.А., Патрушев А.В., Коняев Г.В. РЕМОДЕЛИРОВАНИЕ РУБЦОВОЙ ТКАНИ В ПРОЦЕССЕ ЛЕЧЕНИЯ С ПРИМЕНЕНИЕМ ЛАЗЕРНЫХ ТЕХНОЛОГИЙ // Современные проблемы науки и образования. 2026. № 3. ;URL: https://science-education.ru/ru/article/view?id=34499 (дата обращения: 10.06.2026).
DOI: https://doi.org/10.17513/spno.34499




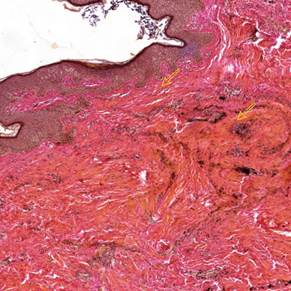
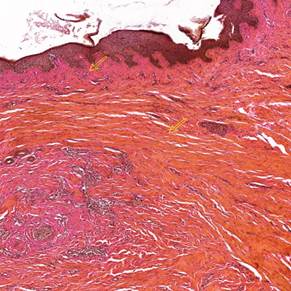
 5. Желтыми стрелками показаны сосочковый слой (верхняя стрелка) и сетчатый слой (нижняя стрелка), восстановившиеся после курса лазерной терапии.Примечание: составлен авторами по результатам данного исследования
5. Желтыми стрелками показаны сосочковый слой (верхняя стрелка) и сетчатый слой (нижняя стрелка), восстановившиеся после курса лазерной терапии.Примечание: составлен авторами по результатам данного исследования