Введение
В мире каждый год выявляют более 325 тысяч новых случаев меланомы кожи - одной из наиболее агрессивных онкологических патологий с низкой 5-летней выживаемостью при метастатическом варианте [1]. Стандартная таргетная терапия пациентов с мутациями BRAF включает комбинацию ингибиторов дабрафениба и траметиниба. Несмотря на высокую первичную эффективность, у 40–60% пациентов развивается резистентность к терапии в течение первых 12 месяцев [2]. Соответственно, этот факт делает актуальным поиск дополнительных молекулярных маркеров ответа на терапию у пациентов с мутациями BRAF.
Вариации числа копий генов (CNV) являются важным механизмом активации онкогенных сигнальных путей MAPK и PI3K, способствующим развитию резистентности к таргетной терапии [3]. В работе Кутилина Д. С. и соавторов [4] было показано, что у больных меланомой кожи с мутацией V600E в гене BRAF и отрицательным ответом на терапию ингибиторами протеинкиназ статистически значимо (p<0,001) повышено число копий генов BRAF, SOS1, KRAS, MEK1, ERK2 и PI3K в опухолевой ткани, что может свидетельствовать об активации сигнального пути RAS-RAF-MEK-ERK у данных пациентов независимо от наличия или отсутствия мутаций в гене BRAF. Эти данные имеют большое значение для развития персонализированной медицины, однако несколько ограничены использованием в исследовании тканевых биоптатов.
Традиционная молекулярная диагностика основана на анализе ДНК из тканевых образцов, полученных при инвазивной биопсии. Внеклеточная ДНК (внДНК), к которой относится ядерная и митохондриальная ДНК из соматических и опухолевых клеток, подвергшихся апоптозу или некрозу, ДНК из клеток крови, вирусная и бактериальная ДНК [5], циркулирующая в плазме крови, открывает возможности для малоинвазивного мониторинга опухолевого генома и прогнозирования ответа на терапию [6].
Исходя из описанного выше целью исследования стало изучение возможности использования показателя копийности ключевых генов сигнальных путей MAPK и PI3K во внеклеточной ДНК (внДНК) плазмы крови для прогнозирования эффективности терапии ингибиторами BRAF/MEK.
Материалы и методы исследования
Дизайн исследования
Проспективное одноцентровое исследование включало 100 пациентов с гистологически подтверждённой меланомой кожи III–IV стадии и выявленной мутацией BRAF V600E/K, а также 25 условно здоровых доноров крови (без онкопатологии). Все пациенты получали комбинированную терапию дабрафенибом (150 мг per os 2 раза в сутки) и траметинибом (2 мг per os 1 раз в сутки). Через 12 недель терапии проводили оценку ответа по критериям RECIST 1.1. Пациенты были разделены на 2 группы:
· группа 1 (чувствительные) - 62 пациента с полным или частичным ответом (CR/PR);
· группа 2 (резистентные) - 38 пациентов с прогрессированием заболевания (PD) или стабилизацией (SD).
Выделение внеклеточной ДНК
Забор крови проводили до начала терапии в вакуированные пробирки с EDTA. Плазму отделяли центрифугированием в течение 20 мин. при 1600 g, затем проводили повторное центрифугирование супернатанта при 16 000 g в течение 10 мин. Внеклеточную ДНК выделяли из 4 мл плазмы с использованием набора QIAamp Circulating Nucleic Acid Kit (Qiagen, Германия) согласно протоколу производителя. Концентрацию ДНК оценивали на спектрофлуориметре.
Определение копийности генов
С опорой на работу Кутилина Д. С. и соавторов [4] для исследования была выбрана панель генов BRAF, KRAS, MEK1, ERK2, SOS1 и PI3K. Копийность генов определяли методом количественной ПЦР в режиме реального времени с использованием красителя EvaGreen® (Biotium, США) на термоциклере Bio-Rad CFX96. В качестве референсных генов использовали ACTB и GAPDH. С использованием базы данных NCBI GenBank (www.ncbi.nlm.nih.gov/genbank) и онлайн-инструмента Primer-BLAST (www.ncbi.nlm.nih.gov/tools/primer-blast) были разработаны последовательности синтетических олигонуклеотидов, в том числе для референсных локусов (табл.).
Перечень синтетических олигонуклеотидов (праймеров) для определения числа копий генов
|
Ген |
Праймер (5'->3') |
|
SOS1 |
F: CCTCTTTGGCTGCTGACAT |
|
KRAS |
F:TGTGTGACATGTTCTAATATAGTCACATTA |
|
BRAF |
F: TCCCTCTCAGGCATAAGGTA |
|
MEK1 |
F: CAGCTTCAGCTGTGGTTTCT |
|
ERK2 |
F: TGGCTACACCTTCGACATCC |
|
PI3K |
F: CCTCTTGCTGTTTCACCA |
|
ACTB |
F: CATGTACGTTGCTATCCAGC |
|
GAPDH |
F: CCTGAACGGGAAGCTCАC R: GCAGGTTTTTCTAGACGGCAT |
Примечание: составлено авторами на основе полученных данных в ходе исследования.
Амплификация каждого образца осуществлялась в 3 повторах. При этом усредненные данные по каждому локусу нормализовались относительно усредненного показателя референсных генов: ΔC(t)=C(t)(среднее геометрическое гена мишени) – C(t)(среднее геометрическое референсных генов). Копийность гена (rCN) вычисляли по формуле rC=Е-ΔΔC(t), где Е - эффективность реакции амплификации, рассчитанная по формуле E=10-1/h, где h - коэффициент уравнения C(t) = h•log P0 + b, полученного путем линейной аппроксимации экспериментальных данных (Е=1,99). Далее вычисляли среднее геометрическое rCп для образцов внДНК пациентов и rCNу для образцов внДНК условно здоровых доноров по каждому генетическому локусу и рассчитывали кратность изменения (fold change, FC) копийности генов: FC = rCNпациентов/rCNусловно здоровых [7].
Статистический анализ
Статистическую обработку данных проводили в программе Statistica 10.0. Для сравнения групп применяли U-критерий Манна - Уитни. Различия считали статистически значимыми при p<0,05. Для визуализации общего профиля копийности генов у всех пациентов была построена тепловая карта, где по оси X отображены гены, а по оси Y - пациенты, сгруппированные по ответу на терапию. Для определения наиболее значимых маркеров чувствительности к терапии был применен лассо-пенализованный регрессионный анализ с использованием пакета scikit-learn в Python. В модели в качестве зависимой переменной использовался ответ на терапию (1 = чувствительный, 0 = резистентный), а в качестве независимых переменных - копийность каждого гена. Модель настраивалась с использованием 10-кратной кросс-валидации для оптимизации параметра регуляризации α.
Работа выполнена с использованием научного оборудования ЦКП НМИЦ онкологии МЗ РФ (регистрационный номер 3554742, https://ckp-rf.ru/catalog/ckp/3554742/).
Результаты исследования и их обсуждение
У всех 100 пациентов до начала терапии во внеклеточной ДНК плазмы крови была подтверждена мутация BRAF V600E (n=92) или V600K (n=8). Через 12 недель терапии объективный ответ (CR/PR) зафиксирован у 62 пациентов (62%), отсутствие ответа/прогрессирование - у 38 пациентов (38%).
Анализ копийности генов во внеклеточной ДНК выявил статистически значимые различия между группами. У пациентов с резистентностью к терапии наблюдалось достоверное увеличение копийности: гена BRAF в 2,1 раза (p<0,001), гена KRAS в 2,4 раза (p<0,001) и гена PI3K (PIK3CA) в 3,5 раза (p<0,001) по сравнению с внДНК группы чувствительных к терапии пациентов (рис. 1).
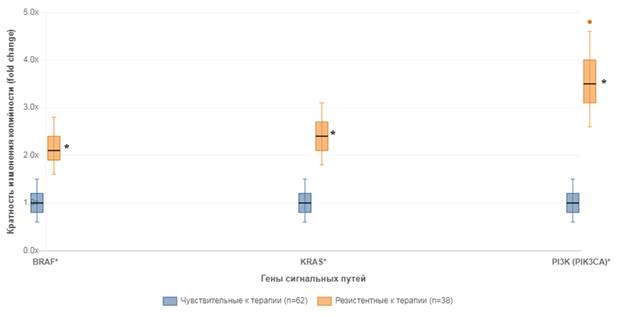
Рис. 1. Сравнение относительной копийности генов BRAF, KRAS и PI3K во внеклеточной ДНК плазмы крови у пациентов с различным ответом на терапию ингибиторами BRAF/MEK (на графике box-plot представлены значения FC, нормализованные относительно копийности генов во внДНК условно здоровых доноров); * - статистически значимые отличия относительно группы с клинически значимым ответом на терапию (p<0,001). Составлено авторами по результатам данного исследования
Повышенная копийность гена BRAF (в 2,1 раза) у резистентных пациентов может приводить к гиперэкспрессии мутантного белка BRAF V600E/K, что создает избыток мишени для ингибиторов. Даже при частичной блокаде активности киназы оставшаяся фракция мутантного белка способна поддерживать активацию сигнального пути MAPK на уровне, достаточном для выживания опухолевых клеток [8]. Этот механизм резистентности аналогичен описанному в исследованиях устойчивости к таргетной терапии при других онкологических заболеваниях, где амплификация целевого гена компенсирует ингибирование его активности [9].
Увеличение копийности гена KRAS (в 2,4 раза) представляет собой альтернативный механизм активации сигнального пути MAPK. KRAS является ключевым узлом передачи сигнала от рецепторов факторов роста к эффекторным киназам. Амплификация этого гена может приводить к конститутивной активации не только каскада RAS-RAF-MEK-ERK, но и параллельных путей, включая PI3K/AKT [10]. Это особенно важно, поскольку даже при эффективной блокаде мутантного BRAF активированный KRAS способен запускать сигнальную трансдукцию через другие члены семейства RAF (ARAF, CRAF), обеспечивая байпасную активацию пути [11].
Наиболее выраженное увеличение копийности наблюдалось для гена PI3K (PIK3CA) (в 3,5 раза), что указывает на критическую роль пути PI3K/AKT/mTOR в развитии резистентности к ингибиторам BRAF/MEK. Сигнальный путь PI3K функционирует параллельно с каскадом MAPK и регулирует ключевые процессы клеточной выживаемости, метаболизма и пролиферации. Активация PI3K может компенсировать блокаду пути MAPK, поддерживая жизнеспособность опухолевых клеток и способствуя прогрессированию заболевания [12].
Полученные данные демонстрируют чёткую корреляцию между копийностью генов во внеклеточной ДНК плазмы крови и эффективностью таргетной терапии меланомы кожи ингибиторами BRAF/MEK.
Тепловая карта (рис. 2) демонстрирует общую картину копийности генов у всех пациентов, сгруппированных по ответу на терапию. Первые 62 пациента представляют группу чувствительных к терапии, а последующие 38 - резистентных. Заметно, что в группе резистентных пациентов наблюдается более высокая копийность всех исследуемых генов, особенно PI3K, которая достигает значений до 3.5-4.0 fold change.
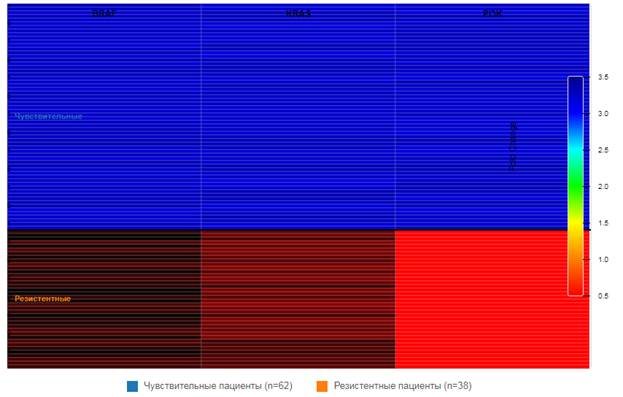
Рис. 2. Тепловая карта относительной копийности генов BRAF, KRAS и PI3K у 100 пациентов с меланомой кожи. Пациенты сгруппированы по ответу на терапию: первые 62 пациента - чувствительные к терапии, последующие 38 - резистентные. Составлено авторами по результатам данного исследования
Визуализация позволяет легко выявить паттерны копийности, характерные для разных групп пациентов. В группе чувствительных пациентов копийность генов в основном колеблется в пределах 1.0-1.5 fold change, тогда как в группе резистентных пациентов значения гораздо выше, особенно для PI3K и KRAS. Это подтверждает гипотезу о том, что повышенная копийность генов сигнальных путей MAPK и PI3K ассоциирована с резистентностью к терапии.
Лассо-пенализованный регрессионный анализ (рис. 3) был применен для определения наиболее важных маркеров чувствительности к терапии. В модели в качестве зависимой переменной использовался ответ на терапию (1 = чувствительный, 0 = резистентный), а в качестве независимых переменных - копийность каждого гена.

Рис. 3. Коэффициенты лассо-регрессионной модели, показывающие вклад каждого гена в предсказание ответа на терапию.
Составлено авторами по результатам данного исследования
Результаты показывают, что ген PI3K (PIK3CA) имеет наибольший положительный коэффициент регрессии (0.85), что указывает на его ключевую роль в развитии резистентности к терапии. Следующим по значимости является ген BRAF (коэффициент 0.72), который активирует RAS и запускает сигнальный каскад MAPK. Ген KRAS также имеет значимый положительный коэффициент (0.45), что подтверждает его роль в резистентности. Отрицательные коэффициенты (не представлены в данном случае) указывали бы на гены, чье повышение копийности ассоциировано с чувствительностью к терапии. В проведенном исследовании все значимые гены демонстрируют положительную корреляцию с резистентностью, что соответствует предыдущим наблюдениям. Лассо-регрессия также показала, что ERK2 имеет наименьший коэффициент (0.18), что указывает на его меньшую значимость для предсказания ответа на терапию по сравнению с другими генами. Это может быть связано с тем, что ERK2 является конечным эффектором в сигнальном каскаде MAPK, и его активность может быть более специфичной для определенных типов мутаций BRAF.
Использование внеклеточной ДНК плазмы крови в качестве источника для молекулярного анализа обладает рядом преимуществ по сравнению с традиционной тканевой биопсией. Во-первых, метод является полностью малоинвазивным и может повторяться в динамике для мониторинга ответа на терапию и раннего выявления развития резистентности [13]. Во-вторых, внеклеточная ДНК отражает геномную гетерогенность опухолевого процесса в целом, включая все метастатические очаги, что особенно важно при меланоме с её высокой склонностью к диссеминации [14]. В-третьих, анализ внДНК позволяет преодолеть проблему пространственной и временной гетерогенности опухоли, которая часто ограничивает прогностическую ценность единичной тканевой биопсии [15]. Данное исследование подтверждает, что определение копийности генов во внеклеточной ДНК может служить надёжным прогностическим маркером эффективности таргетной терапии.
Выявленные закономерности открывают возможности для оптимизации тактики лечения пациентов с меланомой кожи. Пациенты с повышенной копийностью генов BRAF, KRAS или PI3K во внеклеточной ДНК до начала терапии могут быть отнесены к группе высокого риска развития первичной резистентности к ингибиторам BRAF/MEK. Для таких пациентов целесообразно рассмотреть альтернативные стратегии лечения, включая:
1) комбинированную терапию с ингибиторами как пути MAPK, так и PI3K/AKT/mTOR;
2) иммунотерапию ингибиторами контрольных точек (анти-PD-1, анти-CTLA-4);
3) участие в клинических исследованиях новых таргетных препаратов.
Таким образом, рутинное определение копийности генов во внеклеточной ДНК может стать важным компонентом персонализированного подхода к лечению меланомы, позволяя избежать неоправданного назначения препаратов пациентам с низкой вероятностью ответа.
Заключение
В ходе проведенного исследования у пациентов с меланомой кожи и резистентностью к терапии ингибиторами BRAF/MEK выявлено статистически значимое увеличение копийности генов BRAF (в 2,1 раза), KRAS (в 2,4 раза) и PI3K (в 3,5 раза) во внеклеточной ДНК плазмы крови по сравнению с пациентами, чувствительными к терапии. Повышенная копийность данных генов ассоциирована с активацией сигнальных путей MAPK и PI3K независимо от мутационного статуса BRAF, что обусловливает развитие резистентности к таргетной терапии. Тепловая карта и лассо-регрессионный анализ подтверждают, что PI3K и BRAF являются наиболее значимыми маркерами резистентности, что делает их ключевыми кандидатами для дальнейших исследований и потенциальными мишенями для комбинированной терапии. Определение копийности генов BRAF, KRAS и PI3K во внеклеточной ДНК плазмы крови представляет собой перспективный малоинвазивный метод прогнозирования эффективности терапии и персонализации лечения меланомы. Внедрение рутинного анализа CNV указанных генов в клиническую практику позволит оптимизировать выбор терапевтической стратегии и избежать её неэффективности.
Конфликт интересов
Финансирование
Библиографическая ссылка
Зварич А.М., Колесников В.Е., Захарова Н.А., Хохлова О.В., Озеркова Е.А., Дашкова И.Р., Кутилин Д.С. ПОКАЗАТЕЛЬ КОПИЙНОСТИ ГЕНОВ ВО ВНЕКЛЕТОЧНОЙ ДНК ПЛАЗМЫ КРОВИ КАК МАЛОИНВАЗИВНЫЙ МАРКЕР ДЛЯ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ТЕРАПИИ МЕЛАНОМЫ КОЖИ // Современные проблемы науки и образования. 2026. № 3. ;URL: https://science-education.ru/ru/article/view?id=34495 (дата обращения: 10.06.2026).
DOI: https://doi.org/10.17513/spno.34495



