Нарушение функции анастомоза и отводящей петли может быть следствием некорректно выполненной операции: относительно высоко наложенного анастомоза, его малых или избыточных размеров, деформации и сужения приводящей или отводящей петли вблизи соустья [8]. Эти изменения выявляют при рентгенологическом исследовании. В литературе имеются данные о применении эхографии в распознавании острой кишечной непроходимости, в диагностики нарушений эвакуации приводящей петли они единичные [7, 8].
Целью исследования явилось создание способа энтеро-энтероанастомоза при гастрэктомии, снижающего риск развития синдрома приводящей петли, острого панкреатита.
Материал и методы исследования
С 1992 года по 2011 год в хирургическом отделении Областного онкологического диспансера г. Пензы выполнено 569 гастрэктомий по поводу рака желудка. Показаниями к такой операции были: 1) распространенная опухоль средней и верхней третей желудка, а также субтотальное и тотальное поражение органа; 2) мультифокальное поражение органа; 3) ситуации, в которых по объему и локализации поражения желудка технически возможна его резекция, но необходимая лимфаденэктомия требует полного удаления органа. Всем больным произведена стандартная диссекция в объеме D2.
Мы провели сравнительный анализ гастрэктомий у 72 больных раком желудка. Применяли гастрэктомию с наложением муфтообразного пищеводно-кишечного анастомоза в модификации Сигала.
Средний возраст больных в группах составил 61,2±8,7 год. Среди больных были 42,3 % женщины и 57,7 % мужчины. При изучении гистологического строения опухолей заметно преобладание аденокарциномы разной степени дифференцировки - 86,2 % наблюдений.
Пациенты были разделены на 2 группы в зависимости от способа наложения энтеро-энтероанастомоза при гастрэктомии. Между группами не было выявлено значимых различий по полу, возрасту, характеру сопутствующей патологии. 1 группа - 42 пациента, оперированных традиционным методом, энтеро-энтероанастомоз по Braun. 2 группа - 30 пациентов, оперированных предложенным способом наложения энтеро-энтероанастомоза при гастрэктомии. (Способ энтеро-энтероанастомоза при гастрэктомии / А. Л. Чарышкин, В. Ю. Гудошников. Решение о выдаче патента от 23.11.2011 г. по заявке № 2010154844, приоритет от 31.12.10), разработано на кафедре факультетской хирургии Института медицины экологии и физической культуры Ульяновского государственного университета (ИМЭиФК УлГУ). Заключение этического комитета ИМЭиФК УлГУ от 12.11.2009 г. проведение клинических исследований по применению способа энтеро-энтероанастомоза при гастрэктомии, предполагаемая эффективность и безопасность научно обоснованы. Все пациенты давали информированное добровольное согласие на медицинское вмешательство. Производилась гастрэктомия с наложением позадиободочного эзофагоэнтероанастомоза (рис. 1) по Сигалу. Под брыжейкой поперечноободочной кишки на расстоянии примерно 60 см от эзофагоэнтероанастомоза, ниже связки Трейца 3 на 3-4 см формировали энтеро-энтероанастомоз.
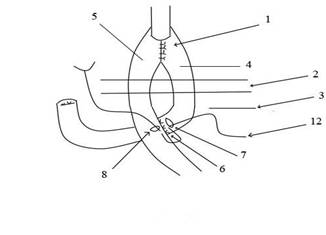
Рисунок 1. Формирование энтеро-энтероанастомоза (1 - эзофагоэнтероанастомоз, 2 - поперечноободочная кишка, 3 - связка Трейца, 4 - приводящая петля тонкой кишки, 5 - отводящая петля тонкой кишки, 6 - наружный ряд задней губы энтеро-энтероанастомоза, 7 - отверстие в поперечном направлении на приводящей петле 4 тонкой кишки, 8 - отверстие в поперечном направлении на отводящей петле 5 тонкой кишки)
Особенности разработанного энтеро-энтероанастомоза заключаются в следующих оригинальных этапах формирования анастомоза: 1. Энтеротомию проводят поперечно, путем рассечения серозной оболочки приводящей и отводящей петли тонкой кишки на расстоянии 18-20 мм, затем мышечный, подслизистый и слизистый слои (рис.2) вскрываются точечным проколом 2-3 мм, при этом слизистый слой расширяется зажимом в поперечном направлении, до 18-20 мм. 2. Энтеро-энтероанастомоз формируется таким образом, что из слизистого и подслизистого слоев отводящей петли тонкой кишки образуются створки арефлюксного клапана (рис. 2), а серозные оболочки приводящей и отводящей петель тонкой кишки точно и надежно сопоставляются друг с другом, обеспечивая герметичность соустья.
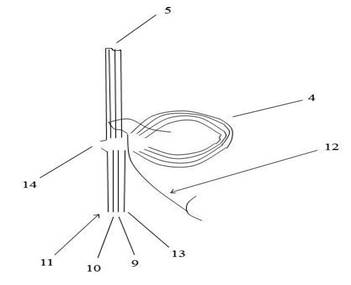
Рисунок 2. Формирование внутреннего ряда арефлюксного энтеро-энтероанастомоза
9 - мышечный слой отводящей петли 5 тонкой кишки, 10 - подслизистый слой отводящей петли 5 тонкой кишки, 11 - слизистый слой отводящей петли 5 тонкой кишки, 12 - синтетическая рассасывающаяся нить, 13 - серозная оболочка отводящей петли 5 тонкой кишки, 14 - створки арефлюксного клапана
Полученные результаты формирования арефлюксного энтеро-энтероанастомоза изучали с помощью ультразвукового (УЗИ), эндоскопического и рентгенологического методов исследования.
При сравнении полученных параметров нами использовался t-критерий Стьюдента для независимых парных выборок и х2-тест. Достоверными признавались различия с уровнем доверительной вероятности не менее 95 % с учетом поправки Бонферрони для множественных сравнений.
Результаты исследования и их обсуждение
Клинические проявления синдрома приводящей петли наблюдались в первой группе у 3 (7,1 %) пациентов, на R-скопии и R-граммах у данных больных наблюдали рефлюкс контрастного вещества (сульфат бария) из отводящей петли в приводящую, во второй группе клиники синдрома приводящей петли не было.
Ультразвуковое исследование в первые двое суток послеоперационного периода достоверных различий в размерах приводящей петли в обеих группах не выявило. УЗИ признаки на 3, 5, 10 сутки после операции показали следующие результаты.. Увеличение диаметра приводящей петли свыше 2,5 см и толщины ее стенки свыше 3 мм соответствуют УЗИ признакам кишечной непроходимости [6], данные размеры выявлены у 26 пациентов (61,9 %) в первой группе и у 3 пациентов (10 %) во второй группе, при этом диаметр и толщина стенки отводящей петли в обеих группах были меньшего размера. В первой группе больных диаметр приводящей петли составлял 3,2±0,6 см, толщина стенки 3,4±0,2 мм, во второй группе соответственно 1,6±0,4 см, толщина стенки 2,1±0,2 мм, различия достоверны (p<0,05). У пациентов с диаметром приводящей петли свыше 2,5 см при выполнении УЗИ наблюдали рефлюкс жидкости из отводящей петли в приводящую.
Во 2-ой группе парез кишечника наблюдался у 3 (10 %) больных, в 1-ой группе у 26 (61,9 %) человек. Парез кишечника достоверно чаще встречался в 1-ой группе и купировался на 7,4 ± 0,4 сутки послеоперационного периода, во второй группе на 3,5 ± 0,3 сутки. Тошнота и рвота купировались на 4,8 ± 0,5 сутки в группе сопоставления и на 2,3 ± 0,3 сутки в группе исследования, диспептические явления достоверно купировались раньше во второй группе.
Повышение амилазы крови отмечалось у 13 (30,9 %) больных 1-ой группы и у 3 (10 %) больных 2-ой группы. Уровень амилазы крови снижался и нормализовался на 6,5 ± 0,3 сутки в первой группе, во второй группе на 3 сутки.
Осложнения чаще встречались в первой группе пациентов: синдром приводящей петли - у 3 пациентов (7,1 %), острый панкреатит - у 10 (23,8 %), панкреонекроз - у 3 пациентов (7,1 %), пневмония - у 3 пациентов (7,1 %).
Во всех наблюдениях при панкреонекрозе были выполнены релапаротомия, холецистостомия, санация и дренирование брюшной полости.
Во второй группе пациентов синдрома приводящей петли не было, острый панкреатит у 3 пациентов (10 %), пневмония - у 1 пациента (3,3 %).
Гнойные осложнения возникли у 9 (21,4 %) больных (нагноение раны, абсцессы брюшной полости) 1-ой группы, и у 3 (10 %) больных 2-ой группы.
Послеоперационная летальность в первой группе составила 7,1 %. Причины послеоперационной летальности: острая сердечно-сосудистая недостаточность - у 2 больных (4,7 %), панкреонекроз - у 1 больного (2,4 %). Послеоперационной летальности во второй группе не было.
Ультразвуковое исследование у больных после гастрэктомии позволяет выявить на раннем этапе нарушения эвакуации из приводящей петли, следить за динамикой и прогнозировать течение.
Мы считаем в большинстве наблюдений нарушения эвакуации из приводящей петли у больных после гастрэктомии с энтеро-энтероанастомозом, по Braun, в послеоперационном периоде были функционального характера и вызваны изменениями нейрогенной и гуморальной стимуляции двенадцатиперстной и тощей кишки, нарушениями их координированной деятельности, рефлюксом содержимого отводящей петли в приводящую. Эти нарушения приводили к снижению перистальтики вплоть до ее полного отсутствия и развития эвакуаторных нарушений.
Таким образом, формирование арефлюксного энтеро-энтероанастомоза у больных после гастрэктомии позволяет исключить повреждения продольной и поперечной мускулатуры тонкой кишки, формируется клапанная функция устья энтеро-энтероанастомоза и при прохождении перистальтической волны препятствует рефлюксу кишечного содержимого в приводящую петлю, что снижает риск развития нарушения эвакуации приводящей петли и количество ранних послеоперационных осложнений.
Рецензенты:
Белый Л.Е., д.м.н., профессор кафедры госпитальной хирургии ФГБОУ ВПО «Ульяновский государственный университет», г. Ульяновск.
Смолькина А.В., д.м.н., профессор кафедры госпитальной хирургии ФГБОУ ВПО «Ульяновский государственный университет», г. Ульяновск.
Библиографическая ссылка
Чарышкин А.Л., Гудошников В.Ю. СПОСОБ ХИРУРГИЧЕСКОЙ ПРОФИЛАКТИКИ РАННИХ ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ ПРИ ГАСТРЭКТОМИИ // Современные проблемы науки и образования. – 2012. – № 2. ;URL: https://science-education.ru/ru/article/view?id=5510 (дата обращения: 26.04.2024).



