Красный плоский лишай (КПЛ) – хроническое воспалительное заболевание кожи и слизистых оболочек, реже поражающее ногти и волосы, типичными элементами которого являются папулы [1]. Заболевание является мультифакторным, иммуноопосредованным, характеризуется хроническим рецидивирующим течением, полиморфизмом клинических проявлений и возможностью опухолевой трансформации, торпидностью к проводимой традиционной терапии [2]. В литературе описаны случаи развития плоскоклеточного рака в хронических очагах КПЛ аногенитальной области и в пищеводе преимущественно при гипертрофической форме заболевания.
Первые упоминания о болезни относятся к 1860 г., когда австрийский дерматолог Фердинанд Гебра описал заболевание «как зудящие узелки темно-красного цвета», ввел термин «leichen ruber», что в переводе с древнегреческого означает: leichen – «ползти, лизать» и с латинского ruber – «красный» [3]. Английским дерматологом Э. Вильсоном в 1869 г. предложен термин «leichen ruber planus» (от латинского planus – «плоский») – красный плоский лишай, который используется и по настоящее время. Еще одним из заслуживающих внимания открытий стала изоморфная феномен-реакция, характеризующаяся поражением кожи и слизистой оболочки в виде длинных линий в ответ на травму, описанная Г. Кёбнером в 1872 г. [4].
КПЛ был описан более 150 лет назад; несмотря на это, данное заболевание по-прежнему остается важной проблемой у клиницистов различных специальностей в связи с тем, что его клиническое распознавание представляет определенные трудности из-за разнообразия клинических проявлений и нередко атипичного течения.
В Российской Федерации заболеваемость КПЛ среди лиц в возрасте 18 лет и старше в 2014 г. составила 12,7 случаев на 100 000 человек. По данным мировой литературы распространенность КПЛ варьирует от 0,5% до 4% от общей численности населения, при этом у 60–75% больных отмечается изолированное поражение слизистой оболочки полости рта (СОПР), у 50% – кожи, одновременное поражение и кожи, и слизистой оболочки встречается у 25% больных [5], среди общей заболеваемости СОПР на долю КПЛ приходится 30–35% [6]. КПЛ может локализоваться и на других слизистых оболочках: половых органов, заднего прохода, конъюнктивы, желудка, уретры, пищевода, частота встречаемости поражений данных локализаций составляет 20–25% [7]. Наиболее часто заболеванием страдают женщины в возрасте 40–60 лет [8]. Ученые во главе с David A. Katzka, проанализировав истории болезни и данные гистологических заключений пациентов с жалобами на дисфагию международной клиники «Мэйо» американского штата Миннесота с 2000 по 2010 гг., выявили 27 случаев рубцовой стриктуры пищевода, обусловленной поражением слизистой оболочки КПЛ [9].
До настоящего времени этиология красного плоского лишая остается неизвестной. Как зарубежные, так и отечественные исследователи схожи во мнении о том, что заболевание носит аутоиммунный характер. Одной из самых распространенных теорий является предположение о том, что экспрессия неидентифицированного антигена кератиноцитами базального слоя кожи и слизистой оболочки активирует миграцию в него Т-лимфоцитов, в ответ на это формируется неконтролируемый иммунный ответ с воспалительной реакцией. Выделяют 6 форм поражения СОПР при КПЛ: 1) типичная встречается в 45% случаях; 2) экссудативно-гиперемическая – в 25%; 3) эрозивно-язвенная – в 23%; 4) буллезная – в 3%; 5) гиперкератотическая – в 2%; 6) атипичная – в 2%. Стадии заболевания подразделяют на острую и хроническую. При типичной форме острая стадия характеризуется возникновением новых папул, при экссудативно-гиперемической усиливаются гиперемия и экссудация, при эрозивно-язвенной форме появляются новые эрозии, уже имеющиеся увеличиваются в размере. Незначительная травма слизистой оболочки провоцирует появление свежих элементов – положительный симптом Кёбнера. В хронической – симптом Кёбнера отрицательный, элементы могут исчезать, но затем возникать вновь, но заболевание при этом не прогрессирует [10]. Длительно существующие высыпания склонны к атрофии тканей, которая в свою очередь вызывает ряд различных осложнений в зависимости от локализации поражения КПЛ [11]. При поражении пищевода самой распространенной жалобой является дисфагия [10], степень которой варьирует от 2 до 3 баллов. В международной классификации болезней красный плоский лишай имеет код L43, непроходимость (стриктура) пищевода – K22.2.
Диагноз устанавливается на основании клинического и гистологического обследования. Материал для биопсии рекомендуется брать из ороговевающих областей, так как эрозии лишены эпителия, что затрудняет микроскопическое исследование. Как дополнительный метод диагностики может применяться реакция прямой иммунофлюоресценции, при которой диагностируются обильные скопления фибрина, в тельцах Сиватта – IgM, реже – IgA, IgG и компонент комплемента. В зарубежных публикациях указывается, что при поражении слизистой оболочки пищевода гистологическое исследование является обязательным с целью исключения малигнизации [3]. Материал для гистологического исследования берется с помощью биопсии при проведении эзофагогастроскопии (ЭГДС), которую рекомендуется выполнять после рентгеноскопии пищевода с контрастным веществом [4]. В отечественных и зарубежных научных статьях нет четких рекомендаций по лечению пациентов со стриктурой пищевода, вызванной КПЛ. В настоящее время не определена универсальная методика лечения стриктуры, выбора медикаментозных препаратов и оптимальных схем лечения.
Цель исследования: осветить проблему клиники, диагностики и лечения редкой стриктуры пищевода, вызванной красным плоским лишаем.
Материалы и методы исследования
С 2011 по 2019 гг. в СПб ГБУЗ «Городская Мариинская больница», на базе кафедры общей хирургии с курсом эндоскопии ФГБОУ ВО «Санкт-Петербургский государственный педиатрический университет» Минздрава РФ находились на лечении 17 больных в возрасте от 50 до 72 лет со стриктурой пищевода, причиной которой явился КПЛ. Для статистической обработки полученных результатов применяли непараметрический метод – критерий согласия χ2, анализ проведен с использованием пакета статистических программ StatSoft STATISTICA 10.0.1011.0 Russian Portable для Windows 10 и Microsoft Exel 2017.
Наиболее часто заболеванию подвергались лица женского пола пожилого возрастного периода (классификация ВОЗ) – 84% (χ2=8,62, p<0,05), средний возраст был равен 61,7 ± 6,3 года. Все больные имели длительный анамнез заболевания, который составлял от 12 до 19 лет, в среднем 15,4±4,5 года, и находились под наблюдением дерматолога поликлиники по месту жительства. Следует отметить, что диагноз КПЛ 6 (35%) больным впервые был установлен оториноларингологом, а 11 (65%) – стоматологом. Слизистая оболочка полости рта была поражена в 76% случаев, что говорило об активной стадии течения заболевания (рис. 1).
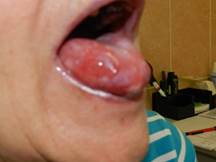
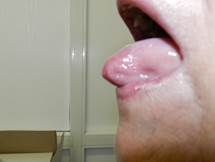
Рис. 1. Фотография больной со стриктурой пищевода на фоне КПЛ, имеющей поражение слизистой оболочки полости рта
У 3 (18%) больных имелась типичная форма поражения кожи, сопровождающаяся зудом. Наиболее характерной жалобой являлась дисфагия, которую испытывали 17 (100%) больных, степень ее выраженности варьировала от 1 до 3 баллов (шкала S. Bown, 1987 г.). Дисфагия носила постоянный характер и прогрессировала в течение длительного времени. Боль при глотании, преимущественно за счет эрозивно-язвенного поражения СОПР, также испытывали все больные, вошедшие в исследование; в свою очередь одинофагия отмечалась лишь у 5 (29%) больных. Двумя неспецифическими жалобами были регургитация и снижение массы тела, которые наблюдались у 3 (18%) и 4 (23%) больных соответственно с дисфагией 3 балла. Учитывая длительный анамнез заболевания, ранее подтвержденный диагноз – КПЛ, основными методами диагностики в нашем исследовании для верификации уровня, протяженности и степени выраженности стриктуры пищевода, исключения малигнизации являлись рентгеноскопия с методом двойного контрастирования, ЭГДС и морфологическое исследование.
Результаты исследования и их обсуждение
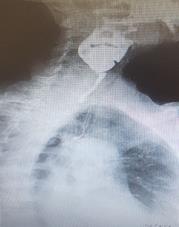
Методика рентгеноскопии пищевода с двойным контрастированием позволила установить, что стриктура достоверно образовывалась в проксимальном его отделе: у 10 (58%) больных стриктура локализовалась в шейном отделе (рис. 2а), а у 7 (42%) – в верхнем грудном. Средняя протяженность сужения составила 1,8±0,6 см.
Для детальной визуализации измененных участков и оценки слизистой оболочки пищевода, исключения патологии желудка и двенадцатиперстной кишки использовали ЭГДС с режимами ZOOM и NBI. Для 76% больных, имевших воспалительные изменения слизистой оболочки полости рта СОПР, были характерны поверхностные эрозии, изъязвления и псевдомембранозные налеты на стенке пищевода (рис. 2б), у 69% из них имелись множественные папулы на слизистой оболочке белесоватого цвета (рис. 2б). А 24% больных имели неизмененную слизистую оболочку стенки пищевода. Осмотр самой стриктуры производили с помощью гастроскопа Olympus GIF-XP160, который позволял визуализировать ее на всем протяжении, оценить стенку, исключить малигнизацию в стриктуре. При осмотре сужения стриктуры у всех 17 (100%) больных слизистая оболочка легко отслаивалась от пищевода, оставляя рыхлую, легко кровоточащую при контакте воспаленную поверхность. При проведении ЭГДС обязательным условием являлось выполнение биопсии из проксимального отдела пищевода. При наличии воспалительных изменений слизистой оболочки пищевода (76% больных) биопсию брали из данных участков, у 24% больных с неизмененной слизистой оболочкой взятие биоптатов производили из 7–10 участков на разной протяженности шейного и грудного отделов пищевода. Первичная биопсия позволяла диагностировать специфические для КПЛ признаки в 70% случаев, для патоморфологической картины которых были характерны: плоский эпителий, множественные лимфоцитарные инфильтраты и рассеянные апоптотические кератиноциты, тельца Сиватта (рис. 2в). Фотография гистологического среза представлена на рисунке 2в, на котором красной стрелкой указаны тельца Сиватта. 30% больным для верификации подтверждения диагноза требовалась повторная биопсия, которую производили через 10–14 дней после бужирования стриктуры.
 а
а 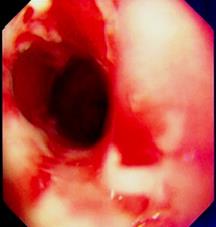 б
б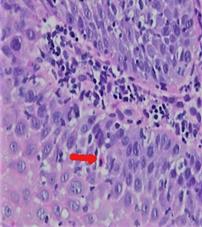 в
в
Рис. 2: а – рентгенограмма стриктуры пищевода при КПЛ; б – эндофото пищевода; в – фотография гистологического среза биоптата (окраска гематоксилином и эозином с увеличением х400)
Как основной метод лечения стриктуры пищевода использовали эндоскопическое бужирование, произведенное всем 17 (100%) больным. Количество сеансов было вариабельным – от 1 до 3. Для патогенетического системного воздействия на активность течения КПЛ использовали следующие медикаментозные препараты: преднизолон от 5 до 30 мг/сутки в зависимости от степени тяжести заболевания, азатиоприн 50 мг/сутки. Также применяли алюминийсодержащие антациды, действие которых связано с цитопротективным эффектом, заключающимся в их способности создавать защитную пленку на поверхности поврежденной слизистой оболочки пищевода, стимулировать синтез простагландинов, которые в свою очередь улучшают микроциркуляцию сосудистого русла и повышают регенераторную функцию слизистой оболочки.
Оценка эффективности и результатов лечения производилась на 14-й день после последнего сеанса дилатации, спустя 1 год и через 3 года. Через 2 недели у 17 (100%) больных дисфагия полностью регрессировала, восстановление просвета органа отмечалось и при рентгенологическом исследовании пищевода с водорастворимым контрастом. Отличительной особенностью заболевания являлось возникновение свежих эрозий и язв в пищеводе после бужирования в местах механической травматизации стенки за счет механического воздействия бужа на суженный участок органа даже у тех больных, которые при первичной ЭГДС не имели воспалительных изменений слизистой оболочки пищевода и поражения СОПР. Данное наблюдение схоже с симптомом Кёбнера, который отмечается при кожном проявлении заболевания. Данный факт может свидетельствовать, что бужирование вызывает обострение КПЛ. Спустя 1 год контрольный осмотр проведен 15 (88%) больным. Дискомфорт при приеме твердой пищи испытывали 11 (73%) пациентов, диаметр стриктуры пищевода был равен 0,9±0,1 см, показаний к бужированию у данной группы больных не выявлено. У 4 (27%) имелась клиника дисфагии 2–3 балла, сопровождающаяся одинофагией, диаметр стриктуры составлял 0,4±0,2 см, что говорило о рецидиве стриктуры. Данной группе была произведена повторная дилатация сужения и скорректирована дозировка медикаментозных препаратов. Рецидив стриктуры отмечался у категории больных, самостоятельно отказавшихся без указания врача от приема препаратов в разные сроки после выписки, что может свидетельствовать о тяжелом и сложно контролируемом течении болезни. Через 3 года результат лечения удалось оценить у 13 (76%) больных. Рецидив стриктуры, сопровождающийся клиникой дисфагии более 1 балла и потребовавший повторного бужирования, диагностирован у 5 (38%) больных.
Поражение пищевода КПЛ, осложняющееся образованием стриктуры, – крайне редкая патология, встречающаяся менее чем в 1% случаев от общего числа пациентов с КПЛ [12]. Основная роль в диагностике должна принадлежать тщательному сбору анамнеза заболевания пациента. Все больные имели длительный анамнез заболевания, в среднем 15,4±4,5 года, подтвержденный лабораторным и патоморфологическим методами диагностики. Сбор анамнеза важен для дифференциальной диагностики дисфагии, частота которой может достигать 30–40%. Образованию стриктур пищевода на фоне поражения органа КПЛ наиболее подвержены женщины пожилого возраста, стриктуры непротяженные и локализуются в проксимальном отделе пищевода [10]. Основной методикой лечения, направленной на обеспечение возможности адекватного энтерального питания за счет восстановления проходимости пищевода, является поэтапное эндоскопическое бужирование, которое сопровождается проведением специфической медикаментозной терапии в максимальных дозировках для данного вида нозологии, так как нами показано, что механическая травматизация стриктуры бужом вызывает обострение КПЛ, о чем свидетельствует положительный симптом Кёбнера. Частота и кратность сеансов дилатации зависят от ответа на проводимое комбинированное лечение [8]. В литературе имеются данные, что частота спонтанных ремиссий КПЛ слизистой оболочки полости рта колеблется от 2,8% до 6,5%, данных о частоте спонтанных ремиссий при поражении пищевода в литературе не содержится. Всем больным после восстановления проходимости пищевода для достижения ремиссии необходима длительная поддерживающая терапия, так как отмена кортикостероидов влечет за собой рецидив заболевания у 88–94% пациентов в срок от 3 до 9 месяцев [13]. Franco D.L. et al. сообщают, что большинство больных с лишайной стриктурой пищевода принимали глюкокортикостероиды, которые могут вызывать кандидозный эзофагит [10]. Данный факт требует внимательного прицельного эндоскопического осмотра стенки органа, так как эндоскопическая картина очень схожа и характерные изменения слизистой оболочки для КПЛ могут быть ошибочно трактованы как кандидозное поражение. Мы наблюдали рецидив стриктуры у 27% и 38 % наших больных спустя 1 и 3 года после лечения, все они отказались от приема лекарственных препаратов. Зарубежные коллеги упоминают о том, что при неэффективности дилатации пищевода, стойких стриктурах в редких случаях пациент может быть подвержен хирургическому лечению [8] либо эндоскопическому стентированию пищевода [13].
Заключение
Лечение стриктуры пищевода, вызванной поражением органа КПЛ, должно включать в себя поэтапное бужирование стриктуры и медикаментозную терапию, которая назначается в максимальных дозировках в период проведения сеансов дилатации и обострения, а в дальнейшем дозировка препаратов постепенно снижается и остается в минимальной поддерживающей дозе в течение длительного времени.
Библиографическая ссылка
Лучинина Д.В., Оглоблин А.Л., Королёв М.П., Федотов Л.Е. КРАСНЫЙ ПЛОСКИЙ ЛИШАЙ КАК ОДНА ИЗ ПРИЧИН ОБРАЗОВАНИЯСТРИКТУРЫ ПИЩЕВОДА – КЛИНИКА, ДИАГНОСТИКА И ПОДХОДЫ К ЛЕЧЕНИЮ В МНОГОПРОФИЛЬНОМ СТАЦИОНАРЕ // Современные проблемы науки и образования. 2020. № 4. ;URL: https://science-education.ru/ru/article/view?id=30049 (дата обращения: 13.02.2026).
DOI: https://doi.org/10.17513/spno.30049



