Гипогликемия и гипергликемия часто встречаются у новорожденных детей с различной массой тела во время реабилитации, но диагностика и предотвращение таких состояний не всегда происходят вовремя [1-3]. У новорожденных, нуждающихся в интенсивной терапии, нарушен контроль уровня глюкозы и наблюдаются значительные колебания уровня глюкозы в крови, их развивающийся мозг более восприимчив к этим метаболическим нарушениям [4]. Гипогликемия связана с плохим исходом развития нервной системы, а гипергликемия связана с повышенной смертностью и заболеваемостью у недоношенных детей [5-7]. Нарушения углеводного обмена связаны с плохими клиническими исходами, но данные и клинически значимые пороги гипогликемии и гипергликемии в различных источниках противоречивы, так же как и методы диагностики [8]. Определение уровня глюкозы в плазме представляет собой золотой стандарт для диагностики метаболических нарушений, однако этот метод позволяет получать только точечные значения и не позволяет в режиме реального времени контролировать уровень гликемии и ее тенденций. Это может объяснить различные нормогликемии по литературным данным в популяции новорожденных и недостаток правильных диагнозов [9; 10]. В частности, нет единого мнения об определении «значимой гипогликемии» (значения глюкозы в крови, требующей медицинского лечения), а также о пороге концентрации глюкозы и времени, необходимого для причинения неврологического повреждения [11; 12]. Непрерывный мониторинг глюкозы (CGM) может быть использован для изучения гомеостаза глюкозы в неонатальном периоде, и некоторые исследования показали, что его использование безопасно и надежно [13; 14]. Кроме того, продемонстрировано, что CGM может обнаруживать значительно большее количество эпизодов гипо/гипергликемии по сравнению с прерывистым измерением уровня глюкозы в крови. Большой группой ученых было проведено перспективное исследование доношенных и поздних недоношенных детей, подверженных риску неонатальной гипогликемии, которым был установлен непрерывный мониторинг уровня гликемии в течение первых 48 часов жизни. Это исследование показало, что, несмотря на регулярное тестирование глюкозы и клиническую цель поддерживать глюкозу >2,6 ммоль /л, многие дети подвергались длительным периодам, когда уровень глюкозы в сенсоре был <2,6 ммоль/л. Среди детей с диагностированной гипогликемией (<2,6 ммоль/л) 25% проводили по меньшей мере 5 часов с глюкозой <2,6 ммоль/л, и почти четверть детей, которые, как считалось, имели нормальные уровни гликемии, имели клинически эпизоды бессимптомной гипогликемии, которые выявляются с помощью непрерывного мониторинга гликемии [15]. Пациентов перенесших неонатальную гипогликемию, повторно подвергли исследованию через 2 года, гипогликемии выявлено не было. Было проанализировано, что новорожденные активных форм кислорода. Нейровизуализирующие исследования у новорожденных с неонатальной гипогликемией показывают диффузные повреждения коры головного мозга и подкоркового белого вещества, преимущественно в теменной и затылочных долях, но не существует порогового уровня глюкозы и длительности гипогликемии, которые вызывают неврологические нарушения. Пороговый уровень гликемии будет изменяться в зависимости от массы тела и гестационного возраста, особенностью является то, что тяжелые эпизоды гипогликемии происходят без сопутствующих клинических симптомов. Таким образом, систематическое исследование глюкозы в крови дает возможности контроля неотложных состояний, но не дает данных о времени возникновения гипогликемии и времени начала снижения показателя для оперативных действий, направленных на лечение и предупреждение экстремально низких показателей глюкозы [16]. Системы непрерывного мониторинга уровня гликемии разработаны для пациентов с сахарным диабетом, но в настоящее время адаптированы и могут применяться в неонатальной службе, тем самым обеспечивают тщательный контроль глюкозы в режиме реального времени, прогнозирование экстренных состояний и уменьшение количества забора крови у недоношенных новорожденных.
Цель исследования: оценить возможности использования системы непрерывного мониторинга гликемии у недоношенных новорождённых для прогнозирования и контроля жизненно угрожающих состояний.
Материалы и методы исследования
Для достижения цели и решения поставленных задач были изучены истории болезни пациентов отделения патологии новорожденных ОГАУЗ «Областной перинатальный центр им. И.Д. Евтушенко» г. Томск.
Клинический пример
Пациентка В., родилась на 36,1 недели в 13:00. Выставлен диагноз: задержка внутриутробного развития 1 степени по гипотрофическому типу. Низкая масса тела. Угроза по гипогликемии, внутриутробная инфекция. Беременность в первой половине протекала без особенностей, вторая половина: флегмонозный аппендицит (аппендэктомия), антибиотикотерапия. Течение родов: беременность 36,1 недели, преждевременные оперативные роды в головном предлежании плода, дистресс плода, задержка развития плода 1 степени с гемодинамическими нарушениями 1 степени, однократное тугое обвитие пуповины вокруг туловища и ножек плода, обвитие по типу портупеи, гестационная артериальная гипертензия, анемия легкой степени тяжести, бессимптомная бактериурия (лечение), большое кесарево сечение в нижнем маточном сегменте поперечным разрезом. Антропометрические данные при рождении: масса при рождении – 2,23 кг, рост - 48 см, окружность головы - 32 см, окружность груди – 29 см. В отделении новорожденных были сделаны стандартные назначения, а также контроль гликемии с помощью глюкометра. В 13:10 состояние пациентки ухудшилось: появились признаки дыхательной недостаточности, при контроле уровень гликемии 2,5 ммоль/л, ребенок накормлен по физиологическим потребностям, контроль через 1 час - уровень глюкозы 3,1 ммоль/л. В 14:10 у ребенка появилась тахикардия до 168 в мин., одышка до 70, аускультативно дыхание в верхних отделах звучное, в нижних ослаблено, по шкале Сильвермана 3 балла, оценка по шкале Балларда - 30 баллов, недоношенность 36 недель, соответствует сроку гестации, оценка по шкале Фентона - недоношенность 36 недель, сроку гестации соответствует, низкая масса тела. Было принято решение о переводе ребенка в отделение реанимации и интенсивной терапии новорожденных. В установленное время при контроле гликемии - 2,2 ммоль/л. В отделении реанимации и интенсивной терапии начата респираторная поддержка и стартовая инфузионная терапия из расчёта физиологической потребности 60 мл/кг/сут., углеводы 4 мг/кг/мин., кальций 1,5 ммоль/кг/сут., энтеральное питание 10 мл (белки 6 г/сут., жиры 4,8 г/сут., углеводы 6,1 г/сут.), каждые 3 часа, раз в сутки. При контрольном измерении глюкоза - 1,6 ммоль/л, экстренная коррекция гипогликемии: болюс 10% глюкозы 2 мл/кг. Контроль гликемии через 30 минут – 3,9 ммоль/л. Для определения дальнейшей тактики ведения пациента был приглашен детский эндокринолог. После осмотра и оценки тяжести состояния здоровья новорожденного, для тщательного контроля гликемии и прогнозирования тяжелых гипогликемий и уменьшения количества заборов крови, пациентке установлен сенсор непрерывного мониторинга гликемии Guardian Real-Time в верхней трети бедра. Система осуществляет 24-часовой мониторинг уровня глюкозы в интерстициальной жидкости в реальном времени, проводит измерение глюкозы 288 раз в сутки. Постоянное отображение информации на дисплее для контроля, информация обновляется каждые 5 минут, также был установлен звуковой сигнал при снижении уровня гликемии к 2,6 ммоль/л (нижняя граница нормы по стандарту) и 8,0 ммоль/л как верхнюю границу. В 20:00 на приборе непрерывного мониторинга уровень гликемии 2,3 ммоль/л (прозвучал звуковой сигнал), при контроле глюкометром глюкоза 1,9 ммоль/л, проведена коррекция болюсного введения 10% глюкозы 2 мл/кг. В питании увеличена дотация углеводов на 1 мг/кг/с, через 1 час глюкоза 4,5 ммоль/л. На вторые сутки после рождения отмечается тенденция к гипогликемии, питание усваивает хорошо, клинических симптомов снижения уровня глюкозы нет. По сигналу Guardian Real-Time гликемия в 06:00 2-х суток - 2,1 ммоль/л, (по глюкометру 1,8 ммоль/л) проведена коррекция болюс: 10% глюкоза - 4,5 мл. По результатам параклинических данных выявлены: респираторный алкалоз, гипокапния, анемии нет, гиперкальциемия, гиперкалиемия, метаболический статус в норме. УЗИ ОБП: признаки невыраженного отечного синдрома. Отмена респираторной поддержки. Энтеральное питание расширено на 30 мл/кг, дотация углеводами увеличена до 8,1 г/сут., инфузионная терапия: физиологическая потребность 120 мл (белки, жиры), дотация не проводится, весь объем с энтеральным питанием углеводы 5 мг/кг/мин., Са 0,5 ммоль/кг. После консультации невролога выставлен диагноз: транзиторная гипогликемия. Для исключения наследственных болезней обмена веществ рекомендовано дополнительное обследование: ТСХ - тандемная масс-спектрометрия, результат отрицательный. Осмотр эндокринолога от 26.12.19: транзиторный гипотиреоз. Транзиторная гипогликемия. Назначен контроль гликемии через каждые 5 часов. В 10:30 при неплановом контроле гликемия 2,3 ммоль/л, повторно введено 10% глюкозы 2 мл/кг, в динамике гликемия восстановлена 3,9 ммоль/л, при контроле через 1 час - 1,3 ммоль/л. Учитывая стойкую сохраняющуюся гипогликемию, проведена коррекция инфузионной терапии, дотация углеводов 6 мг/кг/мин. (глюкоза 10% + глюкоза 20%). Контроль в динамике через 2 часа 1,7 ммоль/л, повторно 2 мл/кг глюкозы, объем парентерального питания увеличен до 80 мл/кг, скорость 7 мл/час. На 2-е сутки ребенок переведен в отделение патологии новорожденных. При объективном осмотре отмечается снижение массы тела (-65 граммов), при разворачивании ребенка прослеживается легкий тремор рук и ног, реакция на осмотр спокойная, плач тихий, двигательная активность достаточная. По мониторингу уровень гликемии - 2,0 ммоль/л, проведена стандартная коррекция по массе тела, при повторном измерении достигнута нормогликемия, и ребенок переведен на вскармливание каждые 2 часа. При повторном контроле в режиме реального времени в течение 5 часов сохранялась нормогликемия, но при мониторинге в ночное время было значение 2,1 ммоль/л, проведена стандартная коррекция, кормление ребенка. Учитывая стойкую гипогликемию, в инфузионной терапии увеличена 10% глюкоза до 10 мг/кг/мин. В течение 9 часов сохраняется нормогликемия, также произведен забор стандартных анализов. В начале 3-х суток получены результаты анализов, по которым обнаружены – ретикулоцитоз, лейкоцитоз; общий анализ мочи - без патологии. По данным сенсора уровень гликемии повторно снизился до 2,3 ммоль/л, при этом контроль глюкозы глюкометром запланирован только через 2,5 часа. В экстренном порядке проведено увеличение дотации глюкозы 10 мг/кг/мин., со скоростью 13 мл/ч, и введен болюс 10% глюкозы 2 мл/кг. При измерении уровня глюкозы через 3 часа – гипогликемия 2,5 ммоль/л. Повторно проведена консультация детским эндокринологом, рекомендовано провести забор крови на определение кортизола, гормонов щитовидной железы. С учетом нестабильной гипогликемии и невозможности достичь длительного состояния эугликемии назначено введение Дексаметазона 6 мг 1 раз в сутки в течение 3 дней. Получены результаты анализов гормонов щитовидной железы (ТТГ 11,5 мкМЕ/мл, свТ4 17,5 пмоль/л, Т3 5,6 пмоль/л), выставлен диагноз: транзиторный гипотиреоз, назначено лечение: Эутирокс 6,25 мкг, утром за 20-30 минут до еды в течение 7-8 недель, затем повторный контроль показателей. В первые сутки после начала введения Дексаметазона уровень гликемии менее 2,6 ммоль/л зарегистрирован 3 раза, длительность эугликемического состояния достигала более 6 часов после стандартной болюсной коррекции. По истечении 3 дней введения гормональных препаратов по мониторингу уровня гликемии достигнута стойкая 24-часовая эугликемия. Непрерывный мониторинг уровня гликемии продолжался у пациентки в течение 7 дней до стойкого эугликемического состояния, затем был удален, но контроль гликемии сохранялся 1 раз в сутки. Повышенная концентрация углеводов в смесях для парентерального питания сохранялась в течение 10 дней после рождения, энтеральное питание в течение 16 дней, затем переведена на грудное вскармливание. Пациентка выписана из отделения патологии новорожденных через 21 день в удовлетворительном состоянии, вес 2525 граммов. После выписки пациентка в рекомендованные сроки наблюдалась в кабинет катамнеза ОГАУЗ «Областной перинатальный центр» г. Томска. Проведение НМТ предполагает возможность загрузить данные на персональный компьютер и отобразить их в виде гликемических кривых на координатной плоскости «время уровень глюкозы». Визуальная оценка этих кривых позволила оценить амплитуду колебаний уровня глюкозы у пациентки, а также скорость изменения гликемии во времени, выявить «случайные» и повторяющиеся явления (рис. 1).
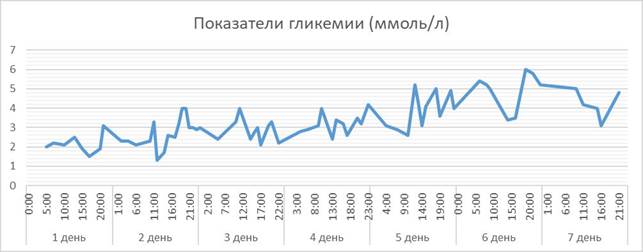
Рис. 1. Динамика гликемии в течение 7 дней
При обработке показаний уровня гликемии были получены сведения о том, что гипогликемия была зарегистрирована 32 раза и продолжалась 196 минут, средний уровень глюкозы – 4,7 ммоль/л. За время наблюдения глюкоза выше целевого значения наблюдалась в 3% случаев, в пределах целевого значения 63% и ниже целевого диапазон 34% за весь период наблюдения. Устройство непрерывного мониторинга гликемии позволило получить данные об уровне гликемии, которые позже были обработаны с помощью специализированного калькулятора вариабельности гликемии – EasyGV [17]. С помощью калькулятора EasyGV рассчитались индексы вариабельности гликемии, которые можно интерпретировать в качестве независимых параметров прогнозирования нарушения углеводного обмена: средний уровень гликемии (Mean), ммоль/л – отражает среднее значение гликемии в течение определенного промежутка времени; стандартное отклонение (SD), ммоль/л – показатель, отражающий колебания гликемии; индекс длительного повышения гликемии (CONGA), ммоль/л – показатель, анализирующий колебания внутрисуточной гликемии; индекс лабильности гликемии (LI), (ммоль/л)2 /час – предиктор гипогликемии, отражает изменения гликемии в течение времени; индекс риска гипогликемии (LBGI) – отражает степень развития риска возникновения гипогликемических явлений; индекс риска гипергликемии (HBGI) - отражает степень развития риска возникновения гипергликемических явлений (рис. 2).
|
Показатель |
Mean |
SD |
CONGA |
LI |
LBGI |
HBGI |
|
1-й день |
3,10 |
0,77 |
2,49 |
0,80 |
20,49 |
0 |
|
7-й день |
5,15 |
0,78 |
4,50 |
1,14 |
2,47 |
0,01 |
Рис. 2. Характеристика индексов вариабельности гликемии
При сравнении индексов вариабельности гликемии отмечено, что все показатели в седьмой день увеличились, что говорит о вариабельности гликемии с показателями глюкозы в пределах нормы. Риск развития гипогликемии значительно ниже в седьмой день, чем в первый.
Заключение
Непрерывный мониторинг уровня гликемии является безопасным и надежным для новорожденных с низкой массой тела, которые находятся на парентеральном и энтеральном питании. Сбор гликемических показателей позволил получить гликемические перцентили, которые могут быть полезны для адаптации потребления глюкозы у пациентов и определить границы. Расчет индексов вариабельности гликемии необходимо учитывать как предиктор достижения компенсации углеводного обмена и выявления рисков развития жизнеугрожающих состояний у новорожденных. Постановка сенсора непрерывного мониторинга гликемии помогает исключить дополнительные заборы крови для контроля гликемии, что очень важно для недоношенных новорожденных, и визуально проследить в графическом варианте контроль гликемии и прогнозировать изменения. Сигнальная система режима контроля в реальном времени оповещает медицинский персонал о снижении глюкозы к пороговым значениям, и тем самым дает возможность оперативного реагирования на экстренное состояние, от которого в дальнейшем зависит нервно-психическое развитие новорождённого.
Библиографическая ссылка
Самойлова Ю.Г., Сиволобова Т.В., Желев В.А., Филиппова Т.А., Петракович А.М. КЛИНИЧЕСКИЙ СЛУЧАЙ ДИАГНОСТИКИ НАРУШЕНИЯ УГЛЕВОДНОГО ОБМЕНА У НЕДОНОШЕННОГО НОВОРОЖДЕННОГО // Современные проблемы науки и образования. 2020. № 4. ;URL: https://science-education.ru/ru/article/view?id=29987 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.29987



