Одной из главных и ведущих причин заболеваемости и смертности во всех странах мира остаются острые нарушения мозгового кровообращения [1, 2]. Так, в России ежегодно регистрируется более 450 тыс. инсультных состояний. Практически треть случаев отмечается у лиц трудоспособной категории, из которых восстанавливается только каждый четвертый больной. Заболевание может возникнуть в любом возрасте, в том числе и в репродуктивном. Так, ишемические инсульты в молодом возрасте, до 40–55 лет, в развитых странах встречаются в 3,4–14% случаев всех ишемических инсультов [3]. Высокий уровень смертности или инвалидизации пациентов, перенесших острое нарушение мозгового кровообращения, делает проблему поиска новых лекарственных средств для терапии подобных пациентов актуальной.
Одна из перспективных групп для медикаментозного лечения пациентов, перенесших инсульт, включает в себя средства с глутaмaтергическим мехaнизмом действия, в частности модуляторы или aгонисты АМРА-рецепторов [4, 5].
Исследуемое лекарственное средство на основе производного 3,7-диазабицикло[3.3.1]нонана обеспечивает длительную активацию AMPA-рецепторов и дальнейшую выработку нейротрофических факторов [5, 6]. Предположительно возможно терапевтическое применение данного лекарственного средства для лечения нарушений когнитивной функции и реабилитации пациентов, перенесших острую продолжительную гипоксию головного мозга вследствие ишемии или других повреждений мозга, что требует более детального изучения фармакологических свойств исследуемого вещества [5].
Целью исследования являлись выявление и оценка потенциального токсического воздействия лекарственного средства на репродуктивные функции у крыс.
Материалы и методы исследования
Объектом исследования являлась фармацевтическая субстанция с химическим названием по международному классификатору IUPAC 6-[4метокси-3-(1Н-пиразол-1-илметил) бензил]-1,11диметил-3,6,9-триазатрицикло [7.3.1.1] тетрадекан-4,8,12-триона, которая была впервые синтезирована на базе химического факультета МГУ им. М.В. Ломоносова [7]. Структура и химическая формула представлены на рисунке.
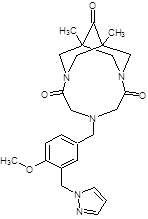
Производное 3,7-диазабицикло[3.3.1]нонана
В работе были использованы 435 половозрелых крыс (300 самок и 135 самцов линии Sprague Dawley (SD), масса тела 180–200 г) и их потомство – 787 крысенок. Изучение репродуктивной токсичности лекарственного средства проводилось в соответствии с руководством по доклиническим исследованиям под редакцией А.Н. Миронова [8].
Влияние лекарственного средства на репродуктивную функцию самок изучалось при пероральном введении крысам (180 самкам и 90 самцам). В исследованиях на самках лекарственное средство растворяли в ДМСО, затем в 2%-ном крахмальном геле, вводили перорально половозрелым виргинным самкам каждый день в течение 15 дней (3 эстральных цикла) до спаривания в двух дозах (2,5 мг/кг и 25 мг/кг)). В контрольной группе вместо лекарственного средства использовали ДМСО и 2%-ный крахмальный гель (плацебо). По завершении процесса введения лекарственного средства особей женского пола подсаживали к интактным самцам в соотношении 2:1 на 2 эстральных цикла (10 дней). Каждая группа животных состояла из 30 особей (10 самцов и 20 самок). Во время исследования оценивали поведение животных и общее физическое состояние. Самок взвешивали до начала исследования, по завершении применения лекарственного средства и перед эвтаназией на 20-й день беременности. Первый день беременности устанавливали путем анализа влагалищных мазков и по наличию в них сперматозоидов.
Изучалось состояние репродуктивных органов беременных особей — в яичниках оценивали количество желтых тел, в матке – мест имплантаций, мертвых и живых плодов, определяли краниокаудальный размер и массу плодов. Для установления целостной картины при помощи полученных данных определяли показатели характеристик пред- и постимплантационной гибели. Также был проведен анализ индекса фертильности (отношение числа беременных самок к числу подсаженных). Из каждой группы животных, получающих лекарственное средство, 50% беременных самок оставляли до родов и в течение одного месяца наблюдали за развитием потомства, при этом проводили оценку таких важных параметров, как поведение, динамика массы тела, общее физическое состояние и гибель крысят.
В исследованиях репродуктивной функции самцов (30 самцов и 60 самок) лекарственное средство вводили самцам крыс (группы по 10 животных) в двух пероральных дозах (2,5 мг/кг и 25 мг/кг) в течение 48 дней (период сперматогенеза). По завершении процесса введения лекарственного средства к самцам подсаживали интактных самок в соотношении 1:2 на 2 эстральных цикла (10 дней). После регистрации беременности самцов подвергали эвтаназии. На 20-й день беременности 50% самок из каждой группы подвергали эвтаназии с последующим вскрытием. Из каждой группы животных 50% беременных самок оставляли до родов и в течение 30 дней наблюдали за развитием потомства, оценивая и регистрируя поведение, динамику роста массы тела, общее физическое состояние и гибель крысят. Состояние репродуктивной функции самцов оценивали по результатам изучения репродуктивных органов самок, спаренных с получавшими лекарственное средство самцами, применяя те же показатели для оценки, что и при оценке репродуктивной функции самок, а также на основе гистологических и морфологических исследований семенников самцов, функционального состояния сперматозоидов и индекса сперматогенеза. Морфологическую оценку состояния сперматогенного эпителия проводили по индексу сперматогенеза (индекс сперматогенеза = ∑А/100, где А – число подсчитанных клеток в каждом канальце, 100 – число подсчитанных при микроскопии канальцев). Индекс сперматогенеза подсчитывали по системе, имеющей деление на 4 балла, регистрируя в канальце наличие сперматогоний, сперматоцитов первого и второго порядка, сперматид и сперматозоидов [9]. Для изучения функционального состояния сперматозоидов использовали метод введения окситоцина для получения эякулята [9].
Для исследования токсичности лекарственного средства в антенатальном периоде развития в эксперименте использованы 30 половозрелых виргинных самок, разделенных на 3 равные группы, и 15 половозрелых самцов. К самкам подсаживали самцов в соотношении 2:1. Изучаемое лекарственное средство вводили перорально беременным самкам крыс с 1-го по 19-й дни беременности, в двух дозах (2,5 мг/кг и 25 мг/кг), один раз в сутки.
Результаты оценивались после эвтаназии путем декапитации и вскрытия самок на 20-й день беременности. После проведения хирургического вмешательства (лапаротомии) извлекали матку с зародышами из плодовместилищ; проводили регистрацию и оценку количества желтых тел во время беременности в обоих яичниках, числа живых, мертвых плодов и резорбированных остатков, а также мест имплантации. Эмбрионы внимательно осматривали на наличие каких-либо внешних аномалий развития, вызванных тератогенными факторами; определяли толщину и массу плаценты; оценивали краниокаудальный размер и массу плодов; определяли общую эмбриональную смертность, являвшуюся следствием различных факторов, пред- и постимплантационную смертность. Также 50% плодов использовали для исследования на наличие внутренних аномалий развития по методу Вильсона. После регистрации плодов в жидкости Буэна в течение недели лезвием бритвы делали девять сагиттальных срезов, которые исследовали при стереомикроскопии на МБС-2 на наличие внутренних аномалий развития.
Для исследования токсического действия лекарственного средства в постнатальном периоде развития лекарственное средство вводили беременным самкам крыс (3 группы по 10 животных) с 6-го дня беременности и до родов (период органогенеза и фетогенеза). Вещество вводили per os в суточных дозах 2,5 мг/кг и 25 мг/кг. За 3–4 дня до родов беременных самок отделяли от самцов и рассаживали в отдельные клетки по одной в каждую.
Проводились оценка и регистрация эмоционального состояния и общего физического состояния самок крыс, продолжительности беременности и динамики состояния характеристики массы тела до родов и после. Осуществлялся анализ развития потомства крыс в течение первых 2 месяцев развития по ряду специфических и интегральных параметров, таких как общее количество крысят в помете, количество мертворожденных и живых плодов; гибель крысят. Регистрировали и оценивали массу крысят при рождении и на 4-е, 7-е; 14-е, 30-е, 45-е и 30-е сутки; измеряли краниокаудальный размер при рождении и на 4-е сутки. Также отмечали и оценивали сроки открытия глаз, появления шерстного покрова, отлипания ушной раковины от головы.
Изучались эмоциональная реакция, двигательная активность и способность к координации движений у всего потомства крысят. Влияние ЛС на скорость созревания сенсорно-двигательных рефлексов потомства оценивалось в тесте «Переворачивание на плоскости» на 8-й день и в тесте «Открытое поле» на 10-й, 15-й и 20-й дни после рождения. В тесте «Переворачивание на плоскости» крысят клали на спину на плоской поверхности и быстро отпускали. При этом определяли время возвращения в нормальное состояние. В тесте «Открытое поле» крысят помещали на 1 мин на площадку размерами 300 × 300 мм, на которой заранее были проведены линии ограничения, образующие 36 квадратов [8]. Проводили регистрацию основных сенсорно-двигательных рефлексов, таких как поднимание головы и передних лап, ползание (число посещенных клеток), опора на задние конечности (стойки), подъем всего тела, а на 20-й день изучали двигательную активность: число пересеченных квадратов, число умываний, встряхиваний и заглядываний в норки. Полученные данные были обработаны статистически (программой Statistica 8.0).
Результаты исследования и их обсуждение
При изучении репродуктивной функции самок были получены следующие результаты (табл. 1). Все самки в контрольной и опытных группах забеременели. Процент гибели эмбрионов на всех стадиях развития у самок, получавших лекарственное средство, не отличался от контрольных значений. Достоверных различий с контролем в массе и размерах плодов и плаценты также не выявлено. При макроскопическом и гистологическом исследовании яичников самок, получавших лекарственное средство в течение 15 дней до спаривания, никаких патологических изменений не выявлено. Яичники самок всех групп темно-красного цвета, с неровной поверхностью, плотные. В корковом веществе яичников исследуемых самок крыс видны фолликулы различной степени созревания и установлены их размеры. Фолликулярный эпителий не изменен, ядра светлые, четкие, мозговое вещество яичников полнокровное.
Таблица 1
Состояние репродуктивных органов беременных самок крыс, получавших ЛС в течение 15 дней перед спариванием
|
Контроль (n=10) |
ЛС |
|||||
|
Доза |
2,5 мг/кг (n=10) |
25 мг/кг (n=10) |
||||
|
Показатели |
M |
SD |
M |
SD |
M |
SD |
|
Число плодов |
6,5 |
1,25 |
6,9 |
1,30 |
7,0 |
1,40 |
|
Число резорбций |
0 |
– |
0 |
– |
0 |
– |
|
Предимплaнтaционная гибель, % |
4,17 |
– |
5,26 |
– |
5,12 |
– |
|
Постимплaнтационнaя гибель, % |
5,80 |
– |
4,17 |
– |
5,41 |
– |
|
Общая эмбриональнaя смертность, % |
9,72 |
– |
9,21 |
– |
10,26 |
– |
|
Масса плода, г |
2,36 |
0,20 |
2,45 |
0,12 |
2,38 |
0,09 |
|
Крaниокаудальный размер плода, см |
2,98 |
0,11 |
2,95 |
0,08 |
2,97 |
0,07 |
|
Масса плaценты, г |
0,49 |
0,03 |
0,49 |
0,02 |
0,48 |
0,02 |
|
Диаметр плaценты, см |
1,44 |
0,04 |
1,43 |
0,03 |
1,42 |
0,04 |
|
Индекс фертильности |
1 |
1 |
1 |
|||
* M – медиана, SD – стандартное отклонение
50% беременных крыс из каждой группы отделяли и оставляли до родов и в течение 30 дней наблюдали за развитием потомства: проводили регистрацию динамики массы, поведения, оценивали общее физическое состояние и гибель крысят. Продолжительность беременности у данных самок крыс находилась на уровне контрольной группы и соответствовала физиологической норме для этого вида животных. Во всех группах роды прошли нормально у всех беременных самок. Все 226 крысят родились жизнеспособными. Гибель крысят в первый месяц жизни не зафиксирована.
При изучении репродуктивной функции самцов, получавших перорально ЛС в течение 48 дней, установлено, что функциональное состояние сперматозоидов было одинаково у животных всех групп (табл. 2). Макроскопическое и гистологическое исследование семенников самцов не выявило никаких морфологических изменений под действием вещества. У всех животных семенники без изменений, овальной формы, бледно-серого цвета, имеют хорошо выраженное дольчатое строение; кровеносные сосуды умеренно выражены. В дольках извитые семенные канальца, полость которых выстлана слоем фолликулярных клеток, в петлях рядами залегают клетки сперматогенного эпителия, находящиеся на разных стадиях созревания. В соединительнотканных перегородках семенника около капилляров расположены скопления крупных многоугольных клеток (интерстициальных клеток), которые изобилуют липидными включениями. Кровеносные сосуды, находящиеся в прослойках рыхлой волокнистой неоформленной соединительной ткани, без патологии. Число сперматогоний в одном канальце и индекс сперматогенеза в контрольной и опытных группах не отличались (табл. 2).
Таблица 2
Влияние исследуемого ЛС в течение 48 дней на сперматогенез крыс
|
Контроль (n=10) |
ЛС |
|||||
|
Доза |
2,5 мг/кг (n=10) |
25 мг/кг (n=10) |
||||
|
Показатели |
M |
SD |
M |
SD |
M |
SD |
|
Функциональное состояние |
||||||
|
Среднее количество сперматозоидов, млн/мл |
176,3 |
44,5 |
180,3 |
51,6 |
182,7 |
46,8 |
|
% живых сперматозоидов |
82,3 |
– |
84,3 |
– |
83,6 |
– |
|
% патологических форм сперматозоидов |
3,2 |
– |
3,9 |
– |
3,5 |
– |
|
Подвижность сперматозоидов по 10-балльной шкале |
8,9 |
1,1 |
8,6 |
1,0 |
8,7 |
1,2 |
|
Морфологическое исследование |
||||||
|
Индекс сперматогенеза |
3,32 |
0,12 |
3,36 |
0,08 |
3,46 |
0,12 |
|
Число сперматогоний в одном канальце |
70,5 |
2,1 |
72,0 |
1,1 |
71,6 |
1,6 |
|
Относительное число канальцев |
0,4 |
0,1 |
0,3 |
0,1 |
0,4 |
0,2 |
* M – медиана, SD – стандартное отклонение
По завершении этапа введения лекарственного средства к самцам подсаживали интактных самок в соотношении 1:2 на 10 дней. Показатели состояния и характеристика репродуктивных органов беременных самок крыс, спаренных с самцами, получавшими лекарственное средство в течение 48 дней в дозах 2,5 и 25 мг/кг, не отличались от показателей самок, которые были спарены с интактными самцами (табл. 3). Это свидетельствует о том, что введение лекарственного средства не оказывает отрицательного воздействия на репродуктивную функцию самцов.
Таблица 3
Состояние репродуктивных органов беременных самок крыс, спаренных с самцами, которые получали исследуемое вещество в течение 48 дней перед спариванием
|
Контроль (n=10) |
Исследуемое лекарственное средство |
|||||
|
Доза |
2,5 мг/кг (n=10) |
25 мг/кг (n=10) |
||||
|
Показатели |
M |
SD |
M |
SD |
M |
SD |
|
Число плодов |
8,80 |
1,10 |
9,20 |
1,20 |
9,00 |
1,00 |
|
Число резорбций |
0 |
– |
0 |
– |
0 |
– |
|
Предимплaнтационная гибель, % |
6,38 |
– |
6,12 |
– |
5,26 |
– |
|
Постимплaнтационная гибель, % |
6,82 |
– |
4,35 |
– |
6,67 |
– |
|
Общая эмбрионaльная смертность, % |
12,77 |
– |
10,2 |
– |
11,58 |
– |
|
Мaсса плода, г |
2,48 |
0,03 |
2,45 |
0,05 |
2,44 |
0,04 |
|
Крaниокаудальный рaзмер плода, см |
3,05 |
0,05 |
3,03 |
0,06 |
3,02 |
0,02 |
|
Масса плaценты, г |
0,52 |
0,01 |
0,54 |
0,03 |
0,48 |
0,01 |
|
Диаметр плaценты, см |
1,46 |
0,03 |
1,45 |
0,04 |
1,42 |
0,03 |
|
Индекс фертильности |
1 |
– |
1 |
– |
1 |
– |
* M – медиана, SD – стандартное отклонение
Каждую группу беременных самок крыс делили в соответствии с соотношением 50:50. 50% беременных самок крыс из каждой группы оставляли для изучения постнатального развития потомства. Роды во всех группах протекали без особенностей и осложнений, ни один из 254 крысят не погиб. В течение одного месяца наблюдали за развитием потомства, проводили регистрацию динамики массы крысят, оценивали общее физическое состояние и поведение. Развитие крысят опытных групп проходило с той же скоростью, что и у контрольных животных.
Изучение характеристики потенциального эмбриотоксического действия лекарственного средства, регистрируемого в антенатальном периоде развития, показало, что при введении лекарственного средства в дозах 2,5 и 25 мг/кг с 1-го по 19-й день эмбриогенеза у самок крыс не отмечено признаков падежа и видимых нарушений беременности. При динамическом наблюдении за приростом массы тела у данных самок не регистрировали отклонений в динамике привеса по сравнению с контрольной группой животных. Доля эмбриональной гибели на всех стадиях развития у крыс, получавших лекарственное средство во всех дозах, не отличается от соответствующих значений у контрольной группы животных (табл. 4). Достоверных различий с контролем в массе и размерах плодов и плаценты также не обнаружено. При осмотре эмбрионов не было выявлено внешних уродств; результаты исследования девяти сагиттальных срезов свидетельствовали и об отсутствии внутренних аномалий развития организмов.
Таблица 4
Влияние ЛС на состояние репродуктивных органов при пероральном введении самкам в течение первых 19 дней беременности
|
Лекарственное средство |
Контроль (n=10) |
ЛС |
||||
|
Доза |
2,5 мг/кг (n=10) |
25 мг/кг (n=10) |
||||
|
Показатели |
M |
SD |
M |
SD |
M |
SD |
|
Число плодoв |
11,80 |
1,14 |
11,50 |
1,69 |
11,60 |
1,16 |
|
Число резoрбций |
0 |
– |
0 |
– |
0 |
– |
|
Предимплaнтационная гибель, % |
5,60 |
– |
5,73 |
– |
5,69 |
– |
|
Постимплaнтационная гибель, % |
8,47 |
– |
6,09 |
– |
5,17 |
– |
|
Общая эмбрионaльная смертность, % |
13,60 |
– |
11,48 |
– |
10,57 |
– |
|
Масса плoда, г |
2,46 |
0,02 |
2,45 |
0,04 |
2,44 |
0,04 |
|
Краниокаудальный размер плoда, см |
3,02 |
0,03 |
3,05 |
0,05 |
3,04 |
0,03 |
|
Масса плaценты, г |
0,52 |
0,01 |
0,53 |
0,02 |
0,52 |
0,03 |
|
Диаметр плaценты, см |
1,44 |
0,01 |
1,45 |
0,02 |
1,47 |
0,02 |
* M – медиана, SD – стандартное отклонение
Изучение потенциального эмбрио- и фетотоксического действия исследуемого ЛС, регистрируемого в постнатальном периоде развития, проводилось на потомстве самок крыс, которым вводили ЛС перорально с 6-го дня беременности и до родов (период органогенеза и фетогенеза) в суточных дозах 2,5 и 25 мг/кг. Во всех группах роды прошли нормально у всех беременных самок. Все 307 крысят родились жизнеспособными. Отсутствовала гибель крысят в первые два месяца жизни. Исходя из того что материнское молоко находилось в желудках крысят, введение исследуемой субстанции самкам крыс отрицательно не отразилось на сосательном рефлексе у крысят и лактации самок. Физическое развитие потомства крыс протекало без каких-либо отклонений от контрольной группы и нормы. Анализ и оценка характеристик проводились в регистрируемые сроки проявления специфических показателей развития, которые включают отлипание ушных раковин, появление первичного волосяного покрова. Открытие глаз у крысят опытных групп находилось в пределах контрольных значений и характерных для данного вида животных колебаний.
Скорость созревания сенсорно-двигательных рефлексов у крысят контрольной и опытной групп в период вскармливания изучалась в тесте «Переворачивание на плоскости» и в тесте «Открытое поле». В тесте «Переворачивание на плоскости» на момент проведения теста (8-й день) рефлекс был полностью сформирован во всех пометах всех групп: крысята возвращались на все 4 лапы за время не более 30 с. Среднее время возвращения в нормальное положение в пометах опытных групп не отличалось статистически значимым образом от значения, полученного в контрольной группе. Крысята всех пометов демонстрировали схожие способности к ползанию, стойкам и подниманию головы на 10-й и 15-й день развития. В возрасте 20 дней все крысята были способны к стойкам, активно перемещались по площадке, умывались и встряхивались (табл. 5). Отличий между животными различных групп не наблюдалось.
Таблица 5
Влияние вещества ЛС при многократном пероральном введении самкам в течение беременности на двигательную активность потомства на 10-й и 15-й день в эксперименте «Открытое поле»
|
Контроль (n=101) |
ЛС |
|||||
|
Доза |
2,5 мг/кг (n=102) |
25 мг/кг (n=104) |
||||
|
Показатели |
M |
SD |
M |
SD |
M |
SD |
|
10-й день |
||||||
|
Поднимание головы |
2,6 |
0,4 |
2,5 |
0,5 |
2,7 |
0,6 |
|
Клетки (ползание) |
3,4 |
0,2 |
3,3 |
0,3 |
3,5 |
0,3 |
|
Стойки |
0 |
– |
0 |
– |
0 |
– |
|
15-й день |
||||||
|
Поднимание головы |
4,5 |
0,5 |
4,1 |
0,4 |
4,2 |
0,4 |
|
Клетки (ползание) |
13,4 |
1,0 |
13,8 |
1,3 |
14,2 |
1,6 |
|
Стойки |
3,1 |
0,7 |
2,8 |
0,7 |
3,1 |
0,6 |
* M – медиана, SD – стандартное отклонение
Пероральное введение исследуемого лекарственного средства беременным самкам крыс с 6-го дня беременности и до родов не оказало значительного влияния на физическое развитие потомства, выработку сенсорно-двигательных рефлексов в период вскармливания и на двигательную активность и эмоциональные реакции после окончания вскармливания. Таким образом, исследуемое лекарственное средство не оказывало фето- и эмбриотоксического эффекта, регистрируемого в постнатальном периоде развития.
Заключение
Лекарственное средство на основе производного 3,7-диазабицикло[3.3.1]нонана (бициклононана) при многократном пероральном введении в дозах 2,5 мг/кг и 25 мг/кг не оказывает негативного действия на репродуктивную функцию самок и самцов крыс, что подтверждается исследованием репродуктивных органов беременных самок, гистологическим изучением яичников и семенников, показателями функционального состояния сперматозоидов, индексом сперматогенеза крыс опытных и контрольной групп, а также нормальным развитием потомства. Вещество не оказывает фето- и эмбриотоксического эффекта, регистрируемого при протекании антенатального и постнатального периода развития организма.
Результаты проведенных исследований на крысах показывают, что лекарственное средство при пероральном введении в дозах 2,5 мг/кг и 25 мг/кг не обладает репродуктивной токсичностью.
Библиографическая ссылка
Бркич Г.Э., Пятигорская Н.В., Недорубов А.А., Филиппова О.В., Зырянов О.А. ИССЛЕДОВАНИЕ РЕПРОДУКТИВНОЙ ТОКСИЧНОСТИ ЛЕКАРСТВЕННОГО СРЕДСТВА НА ОСНОВЕ ПРОИЗВОДНОГО 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНА // Современные проблемы науки и образования. 2020. № 3. ;URL: https://science-education.ru/ru/article/view?id=29791 (дата обращения: 15.01.2026).
DOI: https://doi.org/10.17513/spno.29791



