Существует значительное количество научных публикаций, посвященных влиянию симпатического и парасимпатического отделов вегетативной нервной системы на тонус и регуляцию артериального русла сердечно-сосудистой системы [1]. В то же время отмечается полное отсутствие публикаций, посвященных изменениям адренореактивности артерий при мышечной гиперемии на фоне адаптации организма к холоду. А между тем научное изучение механизмов данного феномена мышечной гиперемии имеет практическое значение и представляет фундаментальный научный интерес. Известно, что около 40% массы человеческого тела составляет мускулатура; вот почему основная часть кровоснабжения и энергозатраты приходятся на обеспечение функционирования поперечно-полосатой мускулатуры. В результате сосудистая система поперечно-полосатых мышц, в частности периферическое сопротивление сосудов, оказывает колоссальное влияние на механизмы регулирования работы сердечно-сосудистой системы, в том числе и на показатели артериального давления [2]. Под феноменом рабочей гиперемии мускулатуры понимают значительное увеличение в них кровотока в условиях совершения ими работы, когда происходит расширение просвета артериальных сосудов [2]. Однако основные механизмы данного явления изучены недостаточно, для их объяснения в публикациях были представлены самые различные точки зрения: повышение содержания углекислого газа, понижение парциального давления кислорода, повышение количества молочной кислоты в мышцах, совершающих работу, и так далее [3, 4]. Бесспорен тот факт, что каждый из этих регуляторных механизмов имеет определенное влияние на кровоток в мускулатуре, однако отсутствует [5–7] количественная оценка такого влияния при гиперемии мышц.
Как никогда актуальны исследования рабочей гиперемии мускулатуры в наше время, что связано с развитием у значительной части населения гиподинамии в связи с автоматизацией и компьютеризацией как на производстве [2], так и в гуманитарных профессиях. Досуг работающего населения также происходит без значительной физической активности в условиях доступности теле-, видео-, компьютерной аппаратуры. В научных работах по физиологии, терапии давно показана связь гиподинамии с нарушениями работы сердечно-сосудистой (в первую очередь) функциональной системы и других регуляторных механизмов. Например, в результате первых космических полетов выяснилось, что буквально нескольких дней гиподинамии достаточно для того, чтобы после приземления космонавт потерял способность самостоятельно передвигаться. Этого влияния гиподинамии стало возможно избежать только после введения в режим космонавтов обязательных ежедневных физических упражнений при полетах.
В Российской Федерации фиксируется [8] высокая смертность от сердечно-сосудистых заболеваний (ССЗ). В свою очередь артериальная гипертензия занимает первое место по смертности в ряду ССЗ в Российской Федерации по данным на начало текущего столетия [8, 9]. Так, 40% взрослого населения имеют показатели артериального давления выше 140/90 мм рт. ст. В Европе он составляет 30%; это, конечно, меньше, чем в России, но тем не менее достаточно высокий показатель. Нужно отметить, что главенствующим фактором увеличения уровня артериального давления при гипертонической болезни нужно считать так называемый [8–10] сосудистый фактор.
Как показывает анализ доступных научных публикаций, одной из новых и актуальных задач фундаментальной науки [1, 2, 8, 9], бесспорно, является исследование влияния рабочей гиперемии мускулатуры на показатели артериальной адренореактивности сосудов поперечно-полосатых мышц после адаптации к пониженным температурам. Вот почему было принято решение провести комплексное научное исследование, направленное на получение данных α1-адренореактивности в бассейне a. femoralis кролика в условиях гиперемии мускулатуры, достигнутой электромиостимуляцией при тридцатидневном периоде адаптации к пониженным температурам.
Материал и методы исследования. Всего в экспериментах участвовало 30 разделенных на две равновеликие группы особей (кроликов). При этом группа из 15 кроликов не подвергалась воздействию низких температур (контроль), у них проводилось определение реактивности артерий бассейна a. femoralis по 8 дозам норэпинефрина с помощью перфузионного насоса постоянной производительности без мышечного сокращения и на фоне мышечного сокращения, вызванного электростимулятором. Каждая доза норэпинефрина вводилась через 10 минут после прекращения реакции и восстановления тонуса артерий до исходного уровня по показаниям перфузионного давления. Так как последующие дозы норэпинефрина были всегда больше предыдущих, исключалось изменение реактивности рецепторов. После максимальной дозы через 10 минут вводилась минимальная доза норадреналина; если величина реакции была равна первоначальной, опыт продолжался, если нет – животное и данные не учитывались (таких кроликов было 6–8%, и у них отмечались небольшие заболевания).
Остальные особи (группа из 15 кроликов) подвергалась в течение 30 дней влиянию на протяжении 6 часов пониженной температуры окружающей среды в помещении (–10?С). Оставшееся время животные содержались при стандартной комнатной температуре. С завершением тридцатидневного холодового адаптационного процесса особи брали в острый опыт, который проводился по схеме (как в контрольной группе).
Наркотизация подопытных животных достигалась гексеналом (дозировка 30 мг/кг), с целью предотвращения коагуляции крови использовался гепарин (1000 единиц на 1 кг веса). Для опыта произведено выделение кожно-мышечного препарата задней конечности путем перевязки всех артерий, кроме a. femoralis, через которую насосом кровь подавалась в бассейн бедренной артерии, датчик давления подключался к выходу насоса. Сокращение артерий от норадреналина бассейна бедренной артерии вело к увеличению перфузионного давления. Так как насос качал постоянный объем крови, датчик регистрировал увеличение давления, по величине увеличения давления судили о функциональной активности адренорецепторов. Величина изменения уровня давления фиксировалась датчиком и через АЦП отправлялась для обработки и хранения на персональном компьютере. Мы совершали инъекции Norepinephrine компании «Sigma – Aldrich Corporation» (норадреналина) в arterial femoralis в восьми различных дозировках. Моделирование рабочей гиперемии мускулатуры осуществлялось с применением электромиостимуляции при частоте тока 5 Гц и электрическом напряжении 10 В импульсом прямоугольной формы длительностью 5 мс. Дозировки норадреналина при этом были идентичны таковым для группы без электромиостимуляции.
В результате мы получали значения сенситивности и числа активных в данный момент артериальных адренорецепторов благодаря применению графического метода оценки в двойных обратных координатах Лайнуивера–Берка [1, 15]. Далее производилась статистическая обработка по Стьюденту полученных данных.
Результаты исследования и их обсуждение. Инъекции норадреналина, как видно на графике (рис. 1), в условиях гиперемии мускулатуры на каждую из восьми дозировок приводили к менее интенсивному вазоконстрикторному эффекту артерий нижней конечности.
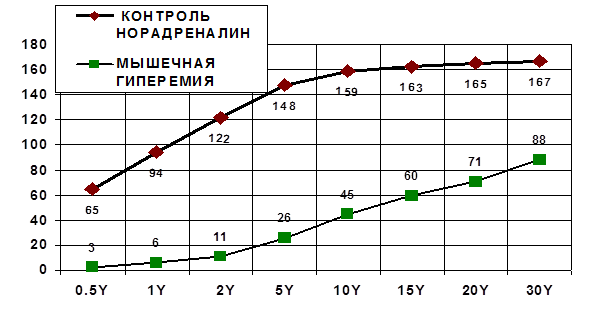
Рис. 1. Значения повышения в группе контроля давления перфузии arterial femoralis (ромбы, линия сверху) и по достижении гиперемии мускулатуры (квадраты, линия снизу). Ось абсцисс: дозировки норадреналина в мкг/кг (Y). На оси ординат отмечено увеличение величин давления перфузии (мм рт. ст.) в ответ на инъекции норадреналина в состоянии гиперемии мускулатуры (P<0,05)
Чтобы выявить возможный максимум эффекта сужения сосудов (Pm = 172 мм рт. ст.) при введении наибольшей из представленных дозировок норадреналина, была графически произведена экстраполяция построения обратного значения 1/Pm, что отслеживается по графику (рис. 2), с применением выражения в двойных обратных координатах зависимости в паре «доза – эффект» по методике Лайнуивера–Берка. Найденная величина достигается при вовлечении 100% всего пула α-1-адренорецепторов arterial femoralis. При этом, так как была отмечена идентичность данного значения в контроле и опыте по достижении гиперемии мускулатуры, правомерно утверждение об отсутствии разности в числе активных α-1-адренорецепторов как до, так и при наступлении состояния гиперемии мускулатуры.
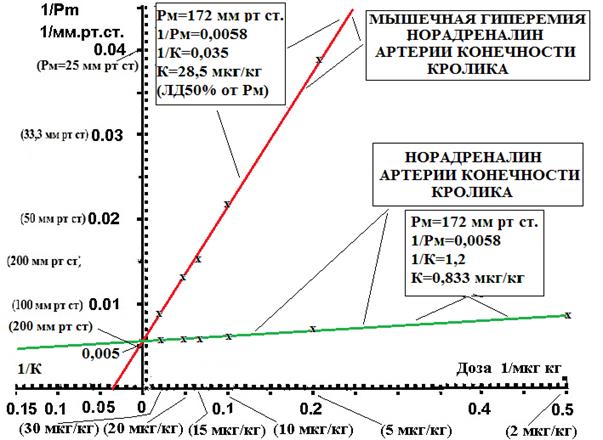
Рис. 2. Сосудистая реактивность α-1-адренорецепторов в ответ на инъекции повышающихся дозировок норадреналина в контроле и при мышечной гиперемии. Построение в двойных обратных координатах по методике Лайнуивера–Берка. Ось абсцисс: дозировки норадреналина в обратных значениях 1/Доза. Ось ординат: увеличение давления перфузии (обратные значения 1/Pm) в 1/мм рт. ст. в ответ на инъекции норадреналина
В таблице 1 представлены данные статистического анализа действия 8 доз норадреналина на тонус артерий задней конечности у 15 кроликов в контроле и во время работы мышц при их электростимуляции, что моделировало рабочую мышечную гиперемию.
Таблица 1
Данные статистического анализа 1

Примечание. М – среднее арифметическое, +-m ошибка средней арифметической, S –среднеквадратическое отклонение, tф – критерий Фишера, из него определяется вер.ош% различия контроля с опытом.
По диаграммам можно сделать заключение (рис. 1, 2), что одно лишь уменьшение сенситивности α-1-адренорецепторов (значения 1/К=1,2; в группе животных контроля, значения 1/К=0,035 в состоянии гиперемии мускулатуры) к норадреналину привело к снижению его влияния на периферические артериальные сосуды, что выразилось в общем понижении артериальной реактивности к медиатору в состоянии гиперемии мускулатуры. Снижение сенситивности адренорецепторов при достижении состояния гиперемии мускулатуры является одним из важнейших механизмов контроля артериального тонуса. По результатам опытов выявилась закономерность снижения вазоконстрикторного эффекта по достижении гиперемии мускулатуры, что ведет за собой понижение артериального давления. Мы своими исследованиями доказали, что для профилактики и лечения гипертонической болезни так важна умеренная физическая активность, которая уменьшает сократительное действие норэпинефрина на артерии работающих мышц.
Число активных рецепторов не изменилось по достижении рабочей мускульной гиперемии, но при этом отмечено значительное уменьшение их сенситивности.
На следующих графиках (рис. 3, 4) видны результаты опытов при тридцатидневной адаптации особей к пониженным температурам и изменение значений артериальной реактивности в ответ на инъекции норадреналина при наступлении гиперемии мускулатуры и вне таковой.
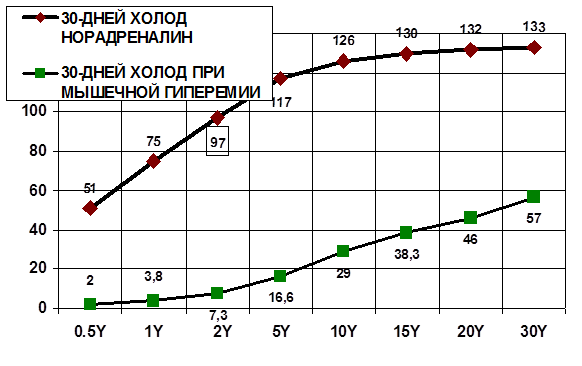
Рис. 3. Кролики после 30-дневного воздействия низких температур. Первая группа – без гиперемии мускулатуры (линия сверху с ромбами), вторая группа – опыты при достижении гиперемии мускулатуры (линия внизу с квадратами). Ось абсцисс: дозировки норадреналина в мкг/кг (Y). Ось ординат: увеличение показателя давления перфузии (мм рт. ст.) в ответ на инъекции норадреналина. Достоверность разницы значений (P<0,05) ответа на каждую из восьми дозировок норадреналина в условиях гиперемии мускулатуры и без нее
Инъекции норадреналина (рис. 3) перед забором крови насосом у кроликов в дискретных возрастающих дозировках после адаптации к пониженным температурам без электромиостимуляции и с электромиостимуляцией (смоделирована гиперемия мускулатуры) влекли за собой увеличение значений давления перфузии в результате возбуждения α-1-адренорецепторов с вазоконстрикторным эффектом (табл. 2, рис. 3).
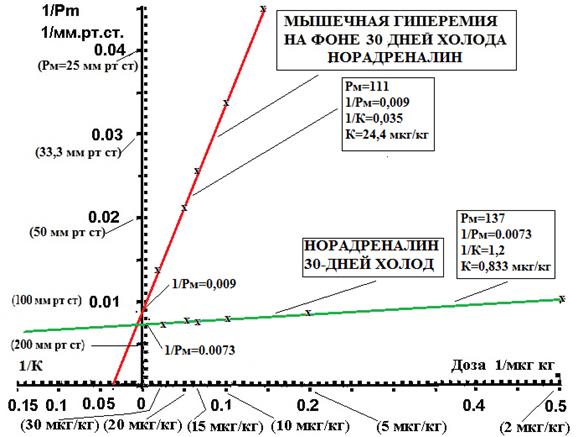
Рис. 4. Опытная группа кроликов при наступлении тридцатого дня холодового воздействия и контрольная группа без холода. Изучено изменение реактивности артериальных α-1-адренорецепторов в ответ на инъекции дискретных дозировок норадреналина по достижении состояния гиперемии мускулатуры и без такового с применением построения в двойных обратных координатах по методике Лайнуивера–Берка. Ось абсцисс: дозировка нейромедиатора (обратное значение 1/Доза в 1/(мкг/кг) для внутриартериальной инъекции. Ось ординат: увеличение давления перфузии (обратное значение 1/Pm, в 1/мм рт. ст.)
Таблица 2
Данные статистического анализа 2

Вместе с тем повышение дозировок норадреналина закономерно повышало вазоконстрикторную реакцию, что влекло за собой увеличение давления перфузии в регионе arterial femoralis. Таким образом, по результатам исследований можно сделать вывод о том, что без электромиостимуляции мускулатуры эффект в результате инъекций восьми дозировок норадреналина наблюдался каждый раз более интенсивно, чем при его введении по достижении состояния гиперемии мускулатуры (табл. 2, рис. 3).
При наступлении тридцатого дня холодового воздействия (рис. 1, 3) вазоконстрикторный эффект в результате инъекций норадреналина (при различных дозировках) артерий нижних конечностей снизился, если сравнивать с животными из группы, не подвергающейся холодовому воздействию. На рисунке 4 отмечены полученные данные в парах параметров «доза – эффект» с использованием методики построения в двойных обратных координатах по Лайнуиверу–Берку, что позволяет выявить физиологические контрольные механизмы вариаций реактивности артериальных адренорецепторов в условиях гиперемии мускулатуры вследствие адаптации к пониженным температурам.
Таким образом, проведенные эксперименты с уверенностью доказали (рис. 3, 4) значительное уменьшение вазоконстрикторного действия норадреналина на регион перфузии arterial femoralis во всех представленных дозировках после адаптации к пониженным температурам окружающей среды. При этом установлено, что расширение артерий в состоянии гиперемии мускулатуры после электромиостимуляции вызвано существенным снижением сенситивности (1/K) α-1-артериальных адренорецепторов (рис. 4) – в 34,3 раза. При этом состояние гиперемии мускулатуры приводит к снижению числа (Pm) артериальных α-1-адренорецепторов артерий со значения Рм=137 мм рт. ст. после адаптации к низким температурам до Рм=111 мм рт. ст. при гиперемии мускулатуры, то есть в 1,23 раза. На тридцатый день воздействия низких температур и наступления адаптации к ним отмечено существенное уменьшение вазоконстрикторного эффекта норадреналина в условиях гиперемии мускулатуры в результате снижения в 34,3 раза сенситивности (1/К) α-1-адренорецепторов к норадреналину, при этом, однако, число (Рм) α-1-адренорецепторов уменьшилось при гиперемии мускулатуры не так выраженно (в 1,23 раза)
В серии опытов по изучению артериальной реактивности в ответ на восемь повышающихся дозировок норадреналина у кроликов, подвергнутых воздействию пониженных температур в течение тридцати дней, впервые показано, что достоверно (при P<0,05) рабочая гиперемия мышц существенно снижает вазоконстрикторный эффект от инъекций норадреналина при всех дозировках. Отмечена интенсификация кровообращения в функционирующих мышцах по сравнению с мускулатурой в покое. С использованием методики Лайниувера–Берка для физиологического анализа данного явления с построением графиков в двойных обратных координатах по парам параметров «доза – эффект» было доказано понижение чувствительности α-1-адренорецепторов в 34,3 раза (1/K) по достижении состояния гиперемии мускулатуры в сравнении с опытами без таковой. При этом число Рм=111 мм рт. ст. активных в данный момент α-1-адренорецепторов уменьшилось в 1,23 раза при гиперемии мускулатуры в сравнении с числом Рм=137 мм рт. ст., зафиксированным без гиперемии мускулатуры. Так, при каждой из исследованных дозировок норадреналина кровообращение усилено при гиперемии мускулатуры, что было вызвано снижением именно числа α-1-адренорецепторов при достижении состояния гиперемии мускулатуры. Адаптационно-эволюционный смысл данного явления заключается в том, что после тридцати дней адаптации к пониженным температурам окружающей среды теплопродукция возрастает настолько, что имеется возможность увеличить интенсивность периферического кровообращения, что усиливает прогревание периферических тканей и увеличивает эффективность работы мускулатуры.
Выводы
Таким образом, можно с уверенностью утверждать, что после тридцатидневной адаптации к низким температурам имеется возможность более эффективно совершать интенсивную мышечную работу в условиях холода, даже при высокой концентрации норадреналина в крови. Наши исследования позволяют сделать заключение о том, что уже на тридцатый день холодовой адаптации функциональная активность α-1-адренорецепторов претерпевает значительные модификации в функционирующих мышцах, при этом меняются как число активных адренорецепторов, так и их чувствительность.
Библиографическая ссылка
Ананьев В.Н., Ананьева О.В., Ананьев Г.В. ФИЗИОЛОГИЧЕСКИЕ АДРЕНЕРГИЧЕСКИЕ МЕХАНИЗМЫ МЫШЕЧНОЙ ГИПЕРЕМИИ ПРИ 30-ДНЕВНОЙ АДАПТАЦИИ К ХОЛОДУ // Современные проблемы науки и образования. 2019. № 5. ;URL: https://science-education.ru/ru/article/view?id=29143 (дата обращения: 11.01.2026).



