Эндопротезирование коленного сустава на данный момент – один из самых востребованных и высокоэффективных методов лечения многих заболеваний и последствий травматических деформаций коленного сустава, в частности остеоартроза и исходов остеоартрита. В Российской Федерации частота повреждения коленного сустава составляет до 2 млн случаев в год. По данным Американского исследовательского центра травматологии и внутреннего остеосинтеза, до 60% всех травм нижних конечностей приходится на травматические повреждения коленного сустава – как костного, так и связочного аппарата [1, 2]. В Российской Федерации заболеваемость остеоартрозом составляет в среднем 18 человек на 10 000 населения [3, 4]. Наибольшая потребность в эндопротезировании коленного сустава в последние годы возникает у пациентов моложе 65 лет, притом что в 2005 г. возрастной ценз находился в пределах от 65 до 74 лет [5]. В Новосибирском НИИТО им. Я.Л. Цивьяна за 2012–2017 гг. выполнено 11 425 операций первичного тотального эндопротезирования коленных суставов.
С увеличением числа оперативных вмешательств по поводу эндопротезирования коленного сустава растет и количество ревизионных операций, связанных не только с инфекцией области хирургического вмешательства, но и нередко с асептической нестабильностью компонентов эндопротеза, в том числе в результате полученной травмы области эндопротеза. Как правило, в таких ситуациях требуется ревизионное оперативное вмешательство в условиях дефицита костной массы опорных поверхностей – проксимального отдела большеберцовой и дистального отдела бедренной костей. Ревизионное эндопротезирование коленного сустава, являясь более сложным оперативным вмешательством, ставит перед хирургом ряд задач – как по общему ведению пациента, так и в плане технических особенностей хода оперативного вмешательства. По данным зарубежных авторов, у 74% пациентов, а по данным РНИИТО им. Р.Р. Вредена – у 94% больных [3–5] в ходе ревизионного эндопротезирования коленного сустава зачастую формируется дефект костной ткани, требующий компенсации и являющийся сложнейшей проблемой ревизионной артропластики коленного сустава на современном этапе.
Ежегодно растет число пациентов с обширными дефектами большеберцовой кости, у которых достижение стабильности эндопротеза является трудной или даже невозможной задачей. В таких случаях возникают показания к применению аддитивных технологий с изготовлением индивидуального 3D имплантата [6–8]. По данным регистра эндопротезирования РНИИТО им. Р.Р. Вредена, доля ревизионных вмешательств в общей структуре операций эндопротезирования коленного сустава в последние годы колеблется от 12 до 16% [8]. В 18% случаев после удаления компонентов эндопротеза встает вопрос о замещении дефектов дистального отдела бедренной кости и проксимального отдела большеберцовой кости с целью восстановления их опороспособности для последующего реэндопротезирования [9].
В представленной статье описан клинический случай ревизионного эндопротезирования коленного сустава с использованием индивидуального 3D имплантата, замещающего дефект проксимального отдела большеберцовой кости. Имплантат напечатан на 3D принтере по SLS технологии из порошка титана марки LPW-TI64-GD23-TYPE5 по ASTM F136.
Материалы и методы исследования. В предоперационном периоде пациенту выполнялась МСКТ (мультисрезовая компьютерная томография), по результатам которой создавалась 3D модель коленного сустава и проводилось предоперационное планирование: верифицировалась истинная геометрия дефекта, определялись границы опороспособной костной ткани.
В работе использовалось специализированное программное обеспечение: для получения 3D моделей применялись конвертер файлов DICOM формата, DICOM Viever; 3D/CAD проектировщики для обработки и коррекции объемных моделей; специальное программное обеспечение InVesalius 3.0, позволяющее оценить плотность костной ткани по шкале Хаунсфилда; K-Pacs программа для просмотра материалов, полученных в результате МСКТ и рентгенографии.
Применялась ЭВМ со следующими параметрами: intel Core i7-3470 3,2 GHz. ОЗУ 4,0 ГБ, видеокарта: AMD Rodeon R9-390X [10, 11].
Для определения истинной геометрии области дефекта проксимального отдела большеберцовой кости с наличием тибиального компонента эндопротеза использовался метод послойной объемной визуализации, который позволяет визуализировать область дефекта костной ткани при наличии металлоконструкции. Применение данного метода дает возможность более корректного моделирования индивидуального имплантата с установкой его в наиболее плотную костную ткань [12, 13]. Реализация метода осуществляется в несколько этапов, он используется как при первичном, так и при ревизионном эндопротезировании коленного сустава.
В результате отбора был выбран один пациент: мужчина А. 57 лет, с посттравматическим дефектом проксимального отдела большеберцовой кости, первичное эндопротезирование коленного сустава в 2009 г. по поводу правостороннего посттравматического гонартроза 3-й стадии. Из анамнеза: 27.11.2017 падение на улице, в результате которого ощутил резкую боль в области правого коленного сустава, отмечает неопорность правой нижней конечности, хруст и резкую боль при минимальных движениях в коленном суставе. Проведено рентгенологическое исследование пораженного коленного сустава справа 28.11.2017 (рис. 1). Диагноз при поступлении в клинику эндопротезирования ФГБУ Новосибирского НИИТО им Я.Л. Цивьяна: Тотально замещенный правый коленный сустав эндопротезом Zimmer (2009 г., Новосибирский НИИТО). Парапротезный перелом медиального мыщелка правой большеберцовой кости. Латеральная связочная нестабильность правого коленного сустава. Варусная деформация правой нижней конечности. НФС 2–3-й ст. Выраженный синдром правосторонней гоналгии.
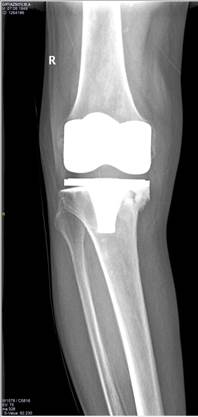
Рис. 1. Рентгенограмма правого коленного сустава в прямой проекции. Нестабильность тибиального компонента эндопротеза.
Варусная деформация коленного сустава
Посредством метода послойной объемной визуализации виртуально были удалены артефакты и металлические компоненты эндопротеза коленного сустава, определена истинная геометрия дефекта проксимального отдела большеберцовой кости (рис. 2).


Рис. 2. Виртуальная модель проксимального отдела большеберцовой кости после обработки по методу послойной объемной визуализации. Верификация истинного дефекта костной ткани проксимального отдела большеберцовой кости
(слева – вид сверху, справа – вид спереди)
При помощи стандартных функций программы 3D/CAD произвели моделирование индивидуального имплантата проксимального отдела большеберцовой кости. При этом учитывали, что имплантация будет производиться после первичной обработки области дефекта двумя полусферическими фрезами размером 44 мм и 36 мм в диаметре. В индивидуальном имплантате предусмотрены технологическое отверстие и ряд характерных полостей, соответствующих установке ревизионного большеберцового компонента эндопротеза коленного сустава (рис. 3).
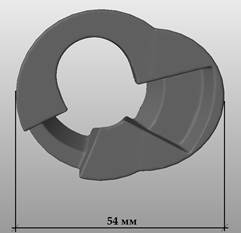
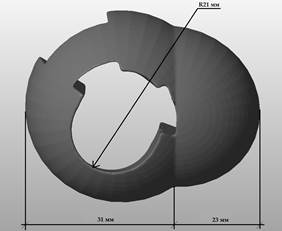
Рис. 3. Моделирование индивидуального имплантата проксимального отдела большеберцовой кости с учетом планируемой интраоперационной обработки области дефекта костной ткани (слева – вид сверху, справа – вид снизу)
После завершения компьютерного моделирования индивидуального 3D имплантата он сохраняется в формате stl. в виде отдельного файла. Непосредственно производство индивидуального имплантата осуществляется на 3D принтере методом селективного лазерного спекания (SLS-печати) из порошка титана марки LPW-TI64-GD23-TYPE5 по ASTM F136 [14, 15]. Затем индивидуальный имплантат стерилизуется с использованием сухожарового шкафа при температуре 180°С в течение 60 минут.
Оперативное вмешательство длительностью 1 ч 45 мин производилось с использованием ревизионного инструментария Zimmer LCCK, прошло без технических сложностей и интраоперационных осложнений (рис. 4), кровопотеря 230 мл. В раннем постоперационном периоде пациент А. в сознании был переведен в отделение реанимации и интенсивной терапии. В течение последующих суток пациент переведен в палату стационара, на вторые сутки активизирован, обучен ходьбе с костылями.
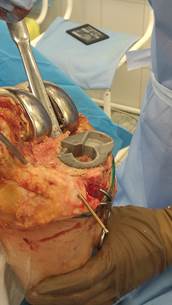
Рис. 4. Фотоснимки установки имплантат на операционном столе. Индивидуальный имплантат полностью закрывает дефект костной ткани проксимального отдела большеберцовой кости, при этом максимально конгруэнтен поверхности дефекта
Результаты исследования и обсуждение. В клинике эндопротезирования Новосибирского НИИТО им Я.Л. Цивьяна в декабре 2017 г. впервые проведено ревизионное эндопротезирование коленного сустава с использованием индивидуального имплантата, напечатанного на 3D принтере. При контрольной рентгенографии определено: положение компонентов правильное, признаков нестабильности тибиального компонента нет, деформация оси нижней конечности исправлена (рис. 5). Пациент на вторые сутки после оперативного лечения вертикализирован, обучен ходьбе при помощи костылей. Общая продолжительность лечения составила 12 суток, моделирование и производство индивидуального имплантата заняли 7 суток. В удовлетворительном состоянии на тринадцатые сутки пациент выписан под наблюдение травматолога по месту жительства, передвигается самостоятельно при помощи костылей, отмечает резко положительную динамику относительно болевого синдрома.
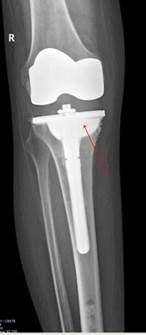
Рис. 5. Рентгенограмма правого коленного сустава в прямой и боковой проекциях после оперативного лечения: положение компонентов правильное, варусная деформация нижней конечности исправлена, отмечается полное заполнение дефекта проксимального отдела большеберцовой кости индивидуальным аугментом
Использование индивидуальных имплантатов в эндопротезировании коленного сустава применяется сравнительно недавно, говорить о каких-либо положительных или отрицательных результатах рано. Однако в ходе нашего опыта мы отметили ряд преимуществ и недостатков, которыми характеризуется использование индивидуальных имплантатов в эндопротезировании коленного сустава. Индивидуальный имплантат при правильном предоперационном планировании является оптимальным с точки зрения сохранения собственной костной ткани – не требует дополнительной резекции, в отличие от применения стандартных аугментов. Сокращаются время оперативного вмешательства и количество используемого ревизионного инструментария, но при этом, если данный имплантат по каким-либо причинам не получится установить, другому пациенту его имплантировать не удастся.
Заключение. В Новосибирском НИИТО им. Я.Л. Цивьяна эндопротезирование коленного сустава с использованием индивидуальных имплантатов было проведено впервые в 2017 г. В период с 2017 по 2018 гг. подобных оперативных вмешательств было проведено 8, во всех клинических случаях были получены хорошие и удовлетворительные результаты. Несмотря на сравнительно небольшой период наблюдения данной категории пациентов, полученный опыт применения индивидуальных имплантатов в эндопротезировании коленного сустава показал ряд преимуществ перед использованием стандартных аугментов. Сократилось время оперативного вмешательства, нет необходимости в специализированном ревизионном инструментарии, в подборе и приобретении стандартных аугментов, снизилась стоимость оперативного лечения. Несмотря на все плюсы, технология производства индивидуальных имплантатов на данный момент доступна лишь в условиях специализированного травматологического отделения при наличии соответствующего программного обеспечения и 3D принтера, печатающего по SLS-технологии из порошка титана TI64-GD23-TYPE5 по ASTM F136.
Библиографическая ссылка
Базлов В.А., Гуражев М.Б., Мамуладзе Т.З., Панченко А.А., Пронских А.А., Соловьев В.Ю., Баитов В.С. ИСПОЛЬЗОВАНИЕ ИНДИВИДУАЛЬНЫХ ИМПЛАНТАТОВ В РЕВИЗИОННОМ ЭНДОПРОТЕЗИРОВАНИИ КОЛЕННОГО СУСТАВА // Современные проблемы науки и образования. 2019. № 4. ;URL: https://science-education.ru/ru/article/view?id=29130 (дата обращения: 12.01.2026).
DOI: https://doi.org/10.17513/spno.29130



