Рак молочной железы (РМЖ) в структуре онкологической заболеваемости женщин занимает 1-е место. Заболеваемость РМЖ с каждым годом неуклонно растет на 1–2%, ежегодно в мире регистрируют более 1 млн новых случаев [1]. В настоящее время установлено, что РМЖ является гетерогенным заболеванием, поэтому успехи лечения и прогноза РМЖ напрямую зависят от правильной и своевременной морфологической, иммуногистохимической, молекулярно-генетической диагностики данного заболевания. В то время как таргетные методы лечения доступны для пациентов с РМЖ, у которых опухоли экспрессируют эстрогеновые и прогестероновые рецепторы или имеется гиперэкспрессия онкобелка HER-2/neu, для тройного негативного (ТН) РМЖ такого лечения не существует. ТН РМЖ составляет от 10 до 20% всех опухолей молочной железы, эти раки традиционно связывают с более плохим прогнозом течения заболевания, однако некоторые больные показывают повышенный риск смерти в течение первых 5 лет, а другие выживают в течение более 10 лет после постановки диагноза. Поиск предикторных факторов и мишеней для терапии этого подтипа РМЖ остается актуальным.
Биомаркеры клеточного цикла, в частности Циклины, ассоциированные с ними циклин-зависимые киназы и циклин-зависимые ингибиторы киназ играют важнейшую роль в развитии клеточного цикла. При опухолях различного генеза установлено, что повышенная продукция Циклина D1 способствует инициации клеточного деления, коррелирует с большей частотой метастазирования опухолей и худшей выживаемостью больных [2, 3].
Данные об уровне экспрессии Циклина D1 и его прогностическом значении в лечении РМЖ остаются противоречивыми. Часть исследований показали, что избыточная экспрессия Циклина D1 является хорошим прогностическим фактором, особенно для эстроген-позитивных пациентов, в некоторых условиях Циклин D1 может вызывать остановку роста вместо прогрессирования клеточного цикла [4, 5]. Однако другие авторы сообщают, что избыточная экспрессия Циклина D1 является предиктором плохого прогноза, Циклин D1 способствует фосфорилированию белка ретинобластомы и других субстратов путем связывания с циклин-зависимой киназой 4/6 (CDK4/6), что способствует быстрому размножению клеток [6, 7].
Цель исследования: Оценить связь уровня экспрессии Циклина D1 в ТН РМЖ с бессобытийной выживаемостью больных c учетом подтипа опухоли – c наличием признаков базального эпителия или их отсутствием.
Материалы и методы исследования. В исследование включены 60 пациенток с подтвержденным ТН РМЖ в клинической стадии 2А (T2N0M0/T1N1M0), находившихся на лечении в ФГБУ «Ростовский научно-исследовательский онкологический институт» МЗ РФ с 2012 по 2015 гг. Во всех случаях операция являлась первым этапом лечения, затем пациентки получали лучевую терапию и химиотерапию по схеме FAC и AC. Возраст пациенток колебался от 29 лет до 71 года, средний возраст составил 51,3±3,5 года, возраст большинства женщин (66,7%) приходился на промежуток от 41 до 60 лет.
Иммуногистохимическое (ИГХ) исследование проводили на парафиновых срезах операционного материала. Для выделения группы базальноподобных (БП) раков использовали ИГХ маркеры к цитокератинам 5/6 (CK5/6) и эпидермальному фактору роста 1-го типа (EGFR). БП ТН РМЖ считали раки, в клетках которых наблюдалась экспрессия СК5/6 (более 10% клеток) и/или EGFR (любое окрашивание), остальные отнесли к неклассифицированным (НК) ТН РМЖ. Чувствительность данного метода определения базальноподобных характеристик составляет 80% и 100% специфичности для базально-подобного подтипа [8]. Для характеристики экспрессии Циклина D1 вычисляли долю клеток с окрашенными ядрами в процентах от общего количества опухолевых клеток. Подсчет проводили полуколичественным методом не менее чем в 10 случайных полях зрения при увеличении х200. ИГХ-окрашивание проводили в иммуногистостейнере BenchMark ULTRA Ventana с антителами к Циклин D1 (клон EP12) Dako, 1:200; CK 5/6 (клон D5/6BH) Dako, 1:200; EGFR (клон E30) Dako, 1:50. Для статистического анализа результатов исследования использовали компьютерную программу STATISTICA 12.0 (StatSoft, США).
Результаты исследования и их обсуждение. На сегодняшний день многочисленные попытки выделения подтипов среди тройных негативных раков молочной железы привели к устойчивому выделению лишь его базальноподобного подтипа, поэтому в нашем исследовании мы ограничились выделением именно этого подтипа. На основании результатов ИГХ-исследования с антителами к СК5/6 и EGFR все ТН РМЖ распределились следующим образом: базальные характеристики были выявлены в 37 (61,7%) опухолях (БП ТН РМЖ) и отсутствовали в 23 (38,3%), последние мы отнесли к неклассифицированным (НК) ТН РМЖ (табл. 1).
Таблица 1
Распределение ТН РМЖ в зависимости от подтипа и уровня экспрессии Циклина D1
|
Подтип ТН РМЖ абс. (%) |
Уровень Циклина D1 |
абс. (%) |
|
|
Всего: 60 (100) |
Базальноподобный 37 (61,7) |
высокий |
12 (32,4) |
|
низкий |
25 (67,6) |
||
|
Всего: 37 (100) |
|||
|
Неклассифицированный 23 (38,3) |
высокий |
10 (43,5) |
|
|
низкий |
13 (56,5) |
||
|
Всего: 23 (100) |
|||
Известно, что ТН РМЖ, как правило, характеризуются высоким уровнем маркера пролиферации Ki-67. Ранее мы установили, что в исследованных опухолях при общем высоком уровне и относительной однородности показателей Ki-67 (76,4±2,2%) экспрессия другого маркера клеточного цикла – Циклина D1 – сильно варьировала (от 1 до 100% популяции опухолевых клеток). Среднее значение этого показателя в БП ТН РМЖ было достоверно выше по сравнению с НК ТН РМЖ (89,9±4,7% и 66,5±6,6% соответственно, р≤0,05) [9]. За пороговое значение Циклина D1 мы приняли 30%, поскольку в исследованных опухолях доля окрашенных клеток находилась либо в интервале от 1 до 30%, либо от 50 до 100%, также подобную градацию встречали у других исследователей [10].
Высокий уровень Циклина D1 (>30% клеток) в обоих подтипах встречался реже, чем низкий: в БП ТН РМЖ – в 32,4% наблюдений, в НК ТН РМЖ – в 43,5% (табл. 1).
У больных с НК ТН РМЖ экспрессия Циклина D1 в опухолевой ткани не сказывалась на бессобытийной выживаемости (рис. 1). По Log-Rank тесту различие между кривыми Каплана-Мейера было недостоверным (р=0,32). У больных с НК ТН РМЖ и высокой экспрессией Циклина D1 выживаемость снижалась со 100% до 60%, а у пациенток с НК ТН РМЖ и низкой экспрессией Циклина D1 в опухолевой ткани – со 100 до 71,4% (табл. 2).
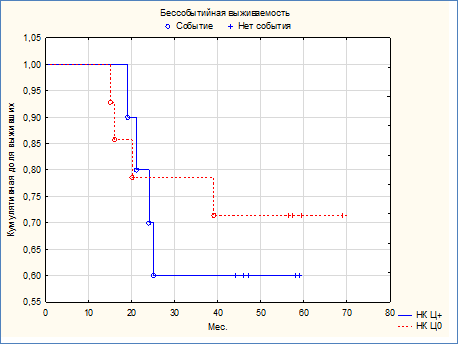
Рис. 1. Кривые Каплана-Мейера бессобытийной выживаемости больных с НК ТН РМЖ и учетом экспрессии Циклина D1. НК Ц+ – экспрессия Циклина D1 высокая, Ц0 – экспрессия Циклина D1 низкая, р=0,32
Экспрессия Циклина D1 БП ТН РМЖ в опухолевой ткани, напротив, статистически значимо (р=0,018) отразилась на бессобытийной выживаемости больных (рис. 2). По Log-Rank тесту различие между кривыми Каплана-Мейера было достоверным (р=0,018). У больных с БП ТН РМЖ и высокой экспрессией Циклина D1 выживаемость снижалась со 100% до 42,9%, в то время как у пациенток с БП ТН РМЖ с низкой экспрессией Циклина D1 в опухолевой ткани – со 100% до 93,75% (табл. 3).
Таблица 2
Динамика кумулятивной доли бессобытийной выживаемости больных с НК ТН РМЖ с учетом экспрессии Циклина D1 в опухолевой ткани
|
Период после операции, месяцев |
Уровень экспрессии Циклина D1 в НК ТН РМЖ |
|
|
высокий |
низкий |
|
|
15,0 |
100,0 |
100 |
|
21,1 |
80,0 |
78,6 |
|
27,2 |
60,0 |
78,6 |
|
33,3 |
60,0 |
78,6 |
|
39,4 |
60,0 |
71,4 |
|
45,6 |
60,0 |
71,4 |
|
51,7 |
60,0 |
71,4 |
|
57,8 |
60,0 |
71,4 |
|
63,9 |
60,0 |
71,4 |
|
70,0 |
60,0 |
71,4 |
Таким образом, в нашем исследовании удалось установить, что в группе больных с ТН РМЖ, имевших базальноподобные характеристики (СК5/6+ и/или EGFR+), наличие высокого уровня экспрессии Циклина D1 (>30%) статистически достоверно сказывалось на выживаемости больных, она была наименьшей. В небазальноподобных раках уровень экспрессии Циклина D1 достоверно не влиял на показатели бессобытийной выживаемости больных.
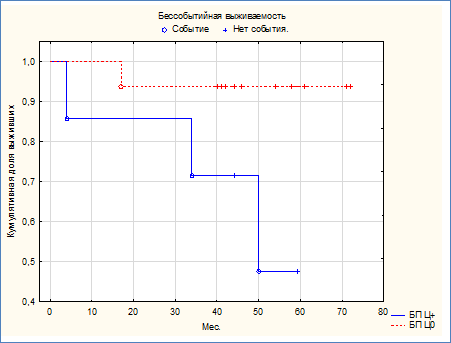
Рис. 2. Кривые Каплана-Мейера бессобытийной выживаемости больных с БП ТН РМЖ и учетом экспрессии Циклина D1. Ц+ – экспрессия Циклина D1 высокая, Ц0 – экспрессия Циклина D1 низкая, р=0,018
Таблица 3
Динамика кумулятивной доли бессобытийной выживаемости больных с БП ТН РМЖ с учетом экспрессии Циклина D1 в опухолевой ткани
|
Период после операции, месяцев |
Уровень экспрессии Циклина D1 в БП ТН РМЖ |
|
|
высокий |
низкий |
|
|
4,0 |
100,0 |
100,0 |
|
11,6 |
85,7 |
100,0 |
|
19,1 |
85,7 |
93,8 |
|
26,7 |
85,7 |
93,8 |
|
34,2 |
71,4 |
93,8 |
|
41,8 |
71,4 |
93,8 |
|
49,3 |
71,4 |
93,8 |
|
56,9 |
42,9 |
93,8 |
|
64,4 |
42,9 |
93,8 |
|
72,0 |
42,9 |
93,8 |
Для оценки влияния количественных параметров экспрессии Циклина D1 на бессобытийную выживаемость был предпринят регрессионный анализ методом пропорциональных интенсивностей Кокса. В результате было установлено, что от количественного показателя, отражающего выраженность экспрессии Циклина D1 в опухолевой ткани, статистически значимо (р=0,008) зависят временные параметры бессобытийной выживаемости. Стандартизированный коэффициент регрессии β составил 1,143±0,008, что свидетельствовало о выраженной силе взаимосвязи между изучаемыми параметрами. Статистика Вальда имела высокое значение 3,72 и с достаточной вероятностью (р=0,008) позволяла отвергнуть нулевую гипотезу о равенстве стандартизированного коэффициента нулю, что позволяло считать полученную информацию о влиянии фактора адекватной.
Гиперэкспрессия Циклина D1 приводит к дисрегуляции активности циклинзависимых киназ, быстрому росту клеток в условиях ограниченной митогенной передачи сигналов, обходу ключевых клеточных контрольных точек и в итоге к опухолевому росту. Недавно выявлена роль Циклина D1 в индукции клеточной миграции и инвазии, усилении ангиогенеза [11].
В эксперименте показано, что ингибирование циклин-зависимых киназ приводит к блокированию клеточного цикла. Определены субстанции, ингибирующие Циклин-зависимые киназы, и в настоящее время некоторые из них проходят клинические испытания [12].
Таким образом, определение уровня экспрессии Циклина D1 в ТН РМЖ является перспективным для использования его в качестве прогностического маркера, а также потенциальной мишени для таргетной терапии.
Выводы
1. Наличие гиперэкспрессии Циклина D1 (>30%) в БП ТН РМЖ является фактором плохого прогноза в отношении бессобытийной выживаемости больных (по Log-Rank тесту различие между кривыми Каплана-Мейера было достоверным: р=0,018).
2. Временные параметры бессобытийной выживаемости статистически значимо (р=0,008) зависят от количественного показателя, отражающего выраженность экспрессии Циклина D1 в опухолевой ткани.
3. В ТН РМЖ без признаков базального эпителия экспрессия Циклина D1 в опухолевой ткани не сказывалась на бессобытийной выживаемости больных (по Log-Rank тесту различие между кривыми Каплана-Мейера было недостоверным: р=0,32).
Библиографическая ссылка
Ващенко Л.Н., Кварчия М.В., Карнаухов Н.С., Гудцкова Т.Н. ЦИКЛИН D1 КАК ПРЕДИКТОР И ПОТЕНЦИАЛЬНАЯ МИШЕНЬ ДЛЯ ТЕРАПИИ ТРОЙНОГО НЕГАТИВНОГО РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ // Современные проблемы науки и образования. 2019. № 3. ;URL: https://science-education.ru/ru/article/view?id=28960 (дата обращения: 02.07.2025).



