Побочное действие лекарственных средств (ПДЛС) продолжает оставаться актуальнейшей проблемой клинической медицины. По данным ВОЗ (2015), ПДЛС занимает 5-е место в мире после сердечно-сосудистых, онкологических, легочных заболеваний и травм [1]. ПДЛС считается реакцией организма, обусловленной приемом лекарственного препарата (ЛП) в дозировке, указанной в инструкции по применению для лечения и профилактики болезней [2].
Под лекарственной токсидермией (ЛТ) принято понимать острое воспаление кожных покровов и слизистых оболочек, развивающееся вследствие действия ЛП, попавшего внутрь организма через дыхательную систему, желудочно-кишечный тракт, при инфузионном введении [3]. ЛТ составляет 25% среди побочных реакций при использовании ЛП, являясь огромной проблемой для системы здравоохранения и фармацевтического производства [4].
С повышением количества лекарственных средств (ЛС), применяемых в лечебной практике, увеличивается риск развития ЛТ. По данным ФГБУ «ГНЦ Институт иммунологии» (2013), у 5–14% госпитализированных пациентов ЛТ возникает после приема антибиотиков, у 3–4% – после нестероидных противовоспалительных средств (НПВС), у 2–3% – после анестетиков, у 1–2% – после сульфаниламидов [1, 2].
Практически все лекарственные средства (ЛС), попадающие в организм человека, могут вызывать ЛТ. ЛС, представляющие высокомолекулярные соединения белковой природы, являются полноценными антигенами. Некоторые низкомолекулярные ЛП, такие как карбоксиметилцеллюлоза и четвертичные аммонийные соединения – нейромышечные релаксанты, также способны активизировать иммунокомпетентные клетки как полноценные антигены [5]. К неполноценным аллергенам (гаптенам) относятся ЛС с низкой молекулярной массой (менее 1 кДа). Данные препараты запускают иммунный ответ только при присоединении к белкам, липидам, полисахаридам и другим макромолекулам-носителям [6].
Огромной проблемой являются перекрестные реакции на ЛС. У многих ЛП имеются общие детерминанты, что делает их близкими по антигенным свойствам, например пенициллин и цефалоспорины [4].
В настоящее время в зависимости от механизма активации иммунной системы выделяют ЛТ как проявление неаллергических гиперчувствительных реакций (псевдоаллергии) и аллергических реакций гиперчувствительности [3]. По классификации Gell и Coombs (1968 г.) аллергические реакции гиперчувствительности подразделяются на четыре типа: реакция гиперчувствительности немедленного типа (I тип), комплементоопосредованная цитотоксичность (II тип), иммунные комплексы (тип III), реакция гиперчувствительности замедленного типа (IV тип) [4, 7].
Псевдоаллергические реакции выявляются у 60% пациентов, аллергические реакции немедленного типа (I тип) – у 12% пациентов, иммунокомплексные реакции (III тип) – у 3% пациентов, реакция гиперчувствительности замедленного типа – у 25% пациентов, цитотоксический тип реакции (II тип) встречается редко [6, 7].
В зависимости от времени манифестации аллергические реакции на ЛС принято делить на два типа: на аллергические реакции немедленного и замедленного типов [1]. Реакции немедленного типа развиваются в течение первого часа после приема ЛС, клиническими проявлениями являются крапивница, отек Квинке и анафилактический шок [8]. Реакции замедленного типа развиваются через 24–48 часов после приема лекарственного препарата, клинически широко вариабельны: от локализованных форм (лекарственная сыпь, фиксированная токсидермия (фиксированная сульфаниламидная эритема), красный плоский лишай) до обширных поражений кожи и слизистых оболочек с вовлечением в патологический процесс других жизненно важных органов и систем (синдром Стивенса–Джонсона и синдром Лайелла) [7].
Клиническая картина ЛТ выделяется своим многообразием и полиморфизмом (истинным и ложным). В то же время она является неспецифичной, разные ЛП могут вызывать одинаковые клинические проявления у различных людей, тогда как один и тот же препарат может способствовать развитию различных проявлений у одного и того же человека [4].
Самой частой формой ЛТ (в 75% случаях) является лекарственно-индуцированная макуло-папулезная сыпь, напоминающая коревую сыпь (рис. 1) [9]. На коже наблюдаются высыпания, которые представлены пятнами или папулами ярко-красной окраски, размером от нескольких миллиметров до 1 см в диаметре, расположенных симметрично, склонных к слиянию и инфильтрации. Наиболее часто областями поражения являются кожа туловища и конечностей. Могут иметь место повышение температуры и сильный зуд. Разрешаются высыпания спустя несколько дней после окончания приема ЛП [2].
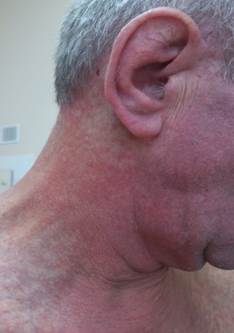
Рис. 1. Пятнисто-папулезные высыпания на прием НПВС
При фиксированной эритеме наблюдается появление отечного пятна круглой или овальной формы, имеющего четкие границы, ярко-красного цвета, со временем становящегося темно-красным с фиолетовым оттенком, размером от нескольких миллиметров до 10–20 см в диаметре (рис. 2). Пятно возникает спустя несколько часов после приема препарата и сохраняется в течение приема ЛС. Регресс патологического процесса наступает через несколько дней или недель после отмены приема ЛП [10].
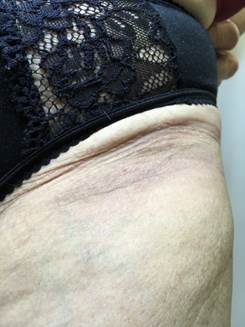
Рис. 2. Фиксированная эритема на прием витаминов группы В
Крапивница проявляется в виде уртикарий разного размера, единичных или множественных, разного размера, различной локализации, впоследствии бесследно исчезающих. Иногда могут сопровождаться ангиоотеком. Наиболее часто вызваны приемом НПВС, антибактериальных препаратов, рентгенконтрастных веществ, витаминов группы В [10].
При отеке Квинке у пациентов возникает отек кожи, подкожной клетчатки, часто и слизистых оболочек. Патологический процесс может сопровождаться чувством жжения в области ладоней и подошв, болезненностью в области отека, сильным зудом, давящей болью за грудиной, слабостью [11].
В случае острой узловатой эритемы наблюдается формирование узлов в области передненаружной поверхности голеней. Узлы ярко-красного цвета, размером от 1 до 6 см, с перифокальным отеком, сопровождаются выраженной болезненностью. Эритема над ними вначале синюшного цвета, со временем меняется на желтовато-зеленую [12]. Пациенты могут предъявлять жалобы на недомогание, лихорадку, артралгию, миалгию. Через 3–6 недели узлы разрешаются бесследно [11].
Токсический эпидермальный некролиз (синдром Лайелла) является тяжелейшей формой ЛТ (рис. 3). Заболевание начинается внезапно, через несколько часов после приема ЛС. На коже возникают эритематозные или уртикарные высыпания с последующим формированием на них пузырей. При надавливании на них их площадь увеличивается до 15 см в диаметре. Синдром Лайелла напоминает синдром Стивенса–Джонсона вследствие образования пузырей на слизистых оболочках ротовой полости, носа, конъюнктиве. Сопровождается слабостью, артралгией, повышением температуры до 39°С. Впоследствии пациенты находятся почти в коматозном состоянии. Основной симптом – массивное отслоение эпидермиса. Симптом Никольского положительный. В случае усиления степени тяжести патологического процесса летальный исход наступает в течение 3–5 дней после начала заболевания [8].
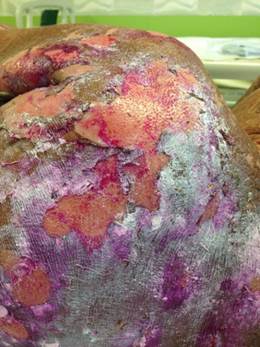
Рис. 3. Синдром Лайелла на прием пенициллина
Целью настоящего исследования являлось выявление лекарственных препаратов, способствующих развитию лекарственной токсидермии, и определение клинических проявлений лекарственной токсидермии.
Материалы и методы исследования
Проведен ретроспективный анализ 100 историй болезней пациентов с ЛТ, находившихся на лечении в клинике кожных и венерических болезней им. В.А. Рахманова за последние пять лет (2012–2016 гг.).
Статистический анализ полученных результатов проводился при помощи пакета программ EXCEL 2010 и STATISTICA 7.0 с использованием критериев Фишера и Манна–Уитни.
Результаты исследования и их обсуждение. В результате ретроспективного анализа 100 историй болезней установлено, что среди пациентов с ЛТ преобладали женщины – 75 человек по отношению к мужчинам – 25 человек, соотношение 3:1.
Пациенты находились в возрасте от 18 до 75 лет, медиана – 53. Полученные данные соответствуют данным, представленным в литературе [2, 9].
Пациентам с ЛТ диагноз «Токсидермия» был выставлен в 69 случаях (69%) , в том числе «Буллезная форма токсидермии» в 1 случае (1%), «Острая крапивница» – в 12 случаях (12%), «Многоформная экссудативная эритема» – в 8 (8%), «Красный плоский лишай медикаментозного генеза» – в 6 (6%), «Фиксированная эритема» – в 4 (4%), «Синдром Стивенса–Джонсона» – в 1 (1%).
Выявлено, что наиболее часто случаи ЛТ развивались при приеме ЛП группы НПВС – 39% и антибиотиков – 22% (р<0,01) (рис. 4).
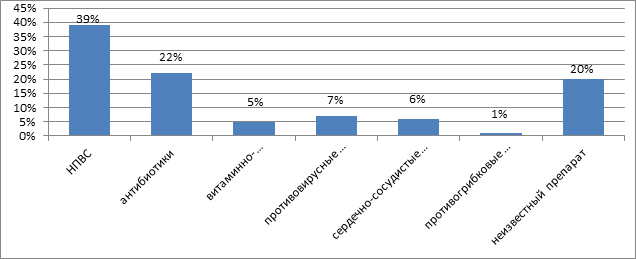
Рис. 4. Группы лекарственных препаратов, вызывающих лекарственную токсидермию
Среди ЛП группы НПВС развитие заболевания достоверно в наибольшей степени было вызвано приемом нурофена – 23,9%, найза – 23,9% и парацетамола – 23,9% (p≤0,003), а среди ЛП группы антибиотиков – приемом амоксициллина – 22,7% и цефтриаксона – 22,7% (р<0,01) (табл. 1).
Таблица 1
Лекарственные препараты, вызывающие лекарственную токсидермию
|
Лекарственный препарат |
Количество наблюдений |
|
НПВС |
39 |
|
Нурофен |
9 |
|
Найз |
9 |
|
Парацетамол |
9 |
|
Диклофенак |
5 |
|
Анальгин |
3 |
|
Аспирин |
2 |
|
Спазган |
2 |
|
Антибиотики |
22 |
|
Амоксициллин |
5 |
|
Цефтриаксон |
5 |
|
Амоксиклав |
3 |
|
Цифран |
3 |
|
Аугментин |
2 |
|
Азитромицин |
2 |
|
Ципрофлоксацин |
1 |
|
Сумамед |
1 |
|
Противовирусные средства |
7 |
|
Тамифлю |
3 |
|
Арбидол |
2 |
|
Амиксин |
2 |
|
Сердечно-сосудистые препараты |
6 |
|
Эналаприл |
3 |
|
Конкор |
2 |
|
Варфарин |
1 |
|
Витаминно-минеральный комплекс |
5 |
|
Мильгамма |
3 |
|
Витаминный комплекс «Алфавит» |
2 |
|
Противогрибковые средства |
1 |
|
Экзифин |
1 |
В процессе анализа историй болезни было выяснено, что достоверно среди кожных проявлений ЛТ преобладали пятнистые элементы – 72 пациента (72%) и папулезные элементы – 68 пациентов (68%) (p<0,05). У 15 пациентов (15%) наблюдались уртикарные элементы, у 10 (10%) – везикулезные элементы, у одного – буллезные элементы (табл. 2).
Таблица 2
Первичные морфологические элементы, наблюдавшиеся у больных при приеме лекарственных препаратов
|
Первичные морфологические элементы сыпи |
||||||||||||||
|
НПВС |
||||||||||||||
|
Название действующего вещества (ЛП) |
Пятно |
Папула |
Везикула |
Пузырь |
волдырь |
|||||||||
|
Кол-во больных |
% |
% |
% |
% |
% |
|||||||||
|
Ибупрофен |
6 |
66,7 |
5 |
55,6 |
– |
– |
– |
– |
3 |
33,3 |
||||
|
Нимесулид |
4 |
44,4 |
6 |
66,7 |
3 |
33,3 |
1 |
11,1 |
1 |
11,1 |
||||
|
Парацетамол |
3 |
33,3 |
4 |
44,4 |
– |
– |
– |
– |
4 |
44,4 |
||||
|
Диклофенак натрия |
4 |
80 |
2 |
40 |
1 |
20 |
– |
– |
– |
– |
||||
|
Метамизол натрия |
4 |
80 |
3 |
60 |
– |
– |
– |
– |
1 |
20 |
||||
|
Ацетилсалициловая кислота |
1 |
50 |
2 |
100 |
– |
– |
– |
– |
– |
– |
||||
|
Антибиотики |
||||||||||||||
|
Амоксициллин |
6 |
85,7 |
5 |
71,4 |
– |
– |
– |
– |
– |
– |
||||
|
Цефтриаксон |
3 |
60 |
2 |
40 |
1 |
20 |
– |
– |
2 |
40 |
||||
|
Амоксициллин + клавулоновая кислота |
2 |
66,7 |
1 |
33,3 |
1 |
33,3 |
– |
– |
1 |
33,3 |
||||
|
Ципрофлоксацин |
4 |
100 |
4 |
100 |
– |
– |
– |
– |
– |
– |
||||
|
Азитромицина дигидрат |
– |
– |
3 |
100 |
2 |
66,7 |
– |
– |
– |
– |
||||
|
Противовирусные средства |
||||||||||||||
|
Осельтамивир |
2 |
66,7 |
3 |
100 |
– |
– |
– |
– |
– |
– |
||||
|
Умифеновир |
2 |
100 |
1 |
50 |
– |
– |
– |
– |
– |
– |
||||
|
Тиролон |
2 |
100 |
1 |
50 |
– |
– |
– |
– |
– |
– |
||||
|
Сердечно-сосудистые препараты |
||||||||||||||
|
Эналаприла малеат |
3 |
100 |
2 |
66,7 |
1 |
33,3 |
– |
– |
– |
– |
||||
|
Бисопролол |
2 |
100 |
1 |
50 |
1 |
50 |
– |
– |
– |
– |
||||
|
Варфарин |
1 |
100 |
– |
– |
– |
– |
– |
– |
– |
– |
||||
|
Витаминно-минеральные комплексы |
||||||||||||||
|
Пиридоксин, тиамин, лидокаин, цианокобаламин (мильгамма) |
2 |
66,7 |
3 |
100 |
– |
– |
– |
– |
– |
– |
||||
|
Токоферол, цианокобаламин, тиамин, йод (витаминный комплекс «Алфавит» т.д.) |
1 |
50 |
2 |
100 |
– |
– |
– |
– |
– |
– |
||||
|
Противогрибковые средства |
||||||||||||||
|
Тербинафин |
1 |
100 |
– |
– |
– |
– |
– |
– |
– |
– |
||||
У 62 пациентов (62%) с ЛТ отмечался полиморфизм высыпаний (табл. 3).
Таблица 3
Сочетание различных высыпаний при различных лекарственных препаратах
|
Действующее вещество (ЛП) |
Первичные морфологические элементы сыпи |
|||||||||||||
|
Пятнисто- папулезные |
Пятнисто-везикулезные |
Папуло-везикулезные |
Пятнисто-папуло-везикулезные |
|||||||||||
|
Кол-во больных |
% |
Кол-во больных |
% |
Кол-во больных |
% |
Кол-во больных |
% |
|||||||
|
НПВС |
||||||||||||||
|
Ибупрофен |
5 |
55,6 |
– |
– |
– |
– |
– |
– |
||||||
|
Нимесулид |
2 |
22,2 |
– |
– |
2 |
22,2 |
1 |
11,1 |
||||||
|
Парацетамол |
2 |
22,2 |
– |
– |
– |
– |
– |
– |
||||||
|
Диклофенак натрия |
2 |
40 |
1 |
20 |
– |
– |
– |
– |
||||||
|
Метамизол натрия |
2 |
40 |
– |
– |
1 |
– |
– |
|||||||
|
Ацетилсалициловая кислота |
1 |
50 |
– |
– |
– |
– |
– |
– |
||||||
|
Антибиотики |
||||||||||||||
|
Амоксицил-лин |
4 |
80 |
– |
– |
– |
– |
– |
– |
||||||
|
Цефтриаксон |
1 |
20 |
1 |
20 |
– |
– |
– |
– |
||||||
|
Амоксициллин + клавулоновая кислота |
– |
– |
– |
– |
– |
– |
1 |
33,3 |
||||||
|
Ципрофлоксацин |
4 |
100 |
– |
– |
– |
– |
– |
– |
||||||
|
Азитроми-цина дигидрат |
– |
– |
2 |
66,7 |
– |
– |
– |
– |
||||||
|
Противовирусные средства |
||||||||||||||
|
Осельтами-вир |
2 |
66,7 |
– |
– |
– |
– |
– |
– |
||||||
|
Умифеновир |
1 |
50 |
– |
– |
– |
– |
– |
– |
||||||
|
Тиролон |
1 |
50 |
– |
– |
– |
– |
– |
– |
||||||
|
Эналаприла малеат |
2 |
66,7 |
1 |
33,3 |
– |
– |
– |
– |
||||||
|
Бисопролол |
1 |
50 |
– |
– |
– |
– |
– |
– |
||||||
|
Пиридоксин, тиамин, лидокаин, цианокобала-мин (мильгамма) |
2 |
66,7 |
– |
– |
– |
– |
– |
– |
||||||
|
Токоферол, цианокобаламин, тиамин, йод и т.д. (витаминный комплекс «Алфавит») |
1 |
50 |
– |
– |
– |
– |
– |
– |
||||||
Важно отметить, что статистически значимой связи между клинической картиной ЛТ и ЛП, индуцировавшим развитие заболевания, выявлено не было (p>0,05) . Один и тот же ЛП мог вызвать различные проявления у пациентов, и в то же время разные ЛП могли приводить к развитию одинаковых проявлений, что доказывает неспецифичность симптоматики ЛТ.
Изолированное поражение кожи было выявлено у 93 больных (93%), слизисто-кожный синдром – у 7 больных (7%), высыпания только на слизистой оболочке не были выявлены ни у одного пациента. Высыпания у пациентов с ЛТ чаще всего локализовались на коже верхних конечностей – 66 случаев (66%) и туловища – 61 случай (61 %), реже – на коже волосистой части головы – 3 случая из 100 (рис. 5).
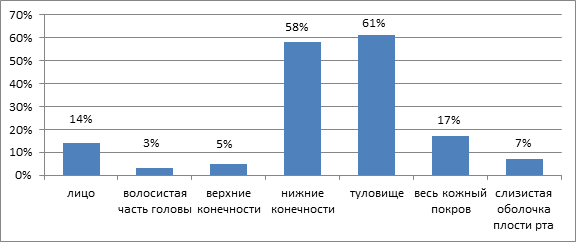
Рис. 5. Локализация сыпи у пациентов с ЛТ
Была определена достоверная связь между приемом ЛП группы НПВС и локализацией сыпи на коже верхних конечностей – 81,6% (р<0,001).
Выводы
1. Прием НПВС и антибиотиков достоверно чаще способствует развитию ЛТ (р<0,01).
2. Пятнисто-папулезные элементы являются наиболее распространенными кожными проявлениями ЛТ (p<0,05).
3. Клинические проявления отличаются полиморфизмом.
4. Клиническая картина ЛТ неспецифична: один и тот же ЛП может вызывать различные клинические проявления, а разные ЛП могут вызывать одинаковые клинические проявления.
Библиографическая ссылка
Теплюк Н.П., Кадырова З.С. РАЗНООБРАЗИЕ КЛИНИЧЕСКИХ ПРОЯВЛЕНИЙ ЛЕКАРСТВЕННОЙ ТОКСИДЕРМИИ У БОЛЬНЫХ, НАХОДИВШИХСЯ НА ЛЕЧЕНИИ В КЛИНИКЕ КОЖНЫХ И ВЕНЕРИЧЕСКИХ БОЛЕЗНЕЙ ИМ. В.А. РАХМАНОВА ФГАОУ ВО ПЕРВЫЙ МГМУ ИМ. И.М. СЕЧЕНОВА МИНЗДРАВА РОССИИ // Современные проблемы науки и образования. 2019. № 3. ;URL: https://science-education.ru/ru/article/view?id=28900 (дата обращения: 03.10.2025).
DOI: https://doi.org/10.17513/spno.28900



