Актуальность. Несмотря на все современные достижения хирургии, антибактериальной терапии и превентивной медицины, послеоперационные стерномедиастинальные инфекции по-прежнему оказывают существенное влияние на заболеваемость и смертность, длительность госпитализации и величину затрат на лечение кардиохирургических пациентов.
Проблема послеоперационных осложнений в кардиохирургии вообще, и инфекционных осложнений стернотомных ран в частности, особенно актуальна в настоящее время на фоне увеличения числа гериатрических пациентов, а также пациентов с сахарным диабетом [1; 2].
Несмотря на длительную историю применения срединной стернотомии, данный доступ имеет ряд недостатков, основным из которых является развитие инфекционных осложнений в области хирургического вмешательства. Они протекают с формированием поверхностной или глубокой раневой инфекции, диастазов и фрагментации грудины, дестабилизации костного каркаса грудной клетки [3; 4].
Частота медиастинитов после кардиохирургических операций, даже при адаптации по отношению к современным методам лечения и профилактики, варьирует от 1.1% до 19% [5; 6]. Несостоятельность швов и инфекция стернотомной раны – грозное осложнение, имеющее высокие цифры летальности, которая составляет в группе риска от 14% до 75% [7]. Развитие ПСМ ассоциируется со значительным снижением долговременной выживаемости [8; 9]. Risnes с коллегами показали, что пациенты, перенесшие передний стерномедиастенит (ПСМ), имеют на 59% больший риск смерти в течение 10-летнего периода после операции в сравнении с пациентами, не переносившими данное осложнение [10; 11]. Это объясняется тем, что хронический воспалительный процесс, связанный с медиастинитом, может отрицательно влиять на тромбогенность и проходимость шунтов и тем самым вести к снижению долговременной выживаемости [12].
ПСМ – одно из самых дорогостоящих осложнений. Стоимость лечения пациентов с ПСМ в среднем в 2-3 раза выше, чем лечение аналогичных пациентов без данного осложнения [13; 14].
Цель исследования - улучшение результатов лечения кардиохирургических пациентов и оценка эффективности VAC-терапии.
В связи с этим решалась задача оценки клинико-морфологических показателей и индукции регенераторных процессов в постоперационной ране у кардиохирургических пациентов при применении открытого метода лечения, воздействия переменного и постоянного вакуума.
Материал и методы исследования. Обследование и лечение пациентов проведено на базе 4 центров, оказывающих кардиохирургическую помощь населению РФ:
1. Центр кардиохирургии и сосудистой хирургии МЦ ДВФУ г. Владивосток.
2. Отделение кардиохирургии ПККБ № 1 г. Владивосток.
3. Федеральный центр сердечно-сосудистой хирургии МЗРФ г. Хабаровск.
4. НЦССХ им. Бакулева МЗРФ.
Группой 1 являлись пациенты с применением переменного вакуумного дренирования, группой 2 – с применением постоянного вакуумного дренирования, группой 3 – с применением метода открытого ведения. Специалистам, привлеченным для анализа и интерпретации гистологического компонента исследования, не предоставлялась никакая информация о принадлежности пациентов к отдельным исследуемым группам с целью снижения вероятности систематических статистических ошибок в исследовании и максимальной объективизации в интерпретации гистологических данных.
Исследование проведено в соответствии с требованиями Минздравмедпрома РФ от 29.04.94 № 82 и согласно номенклатуре клинических лабораторных исследований МЗ РФ (Приказ № 64 от 21.02.2000 г.) с учетом положений Хельсинкской декларации (2000). На основе проспективных, контролируемых сравнительных исследований проведен мониторинг морфологических изменений в условиях регенерации инфицированной стернотомной раны в соответствии с принципами доказательной медицины. Использованы клинические и классические морфологические методы исследования в мониторинге репаративных процессов у пациентов с послеоперационными стерномедиастинитами с последующим статистическим анализом полученных данных. В нашем исследовании мы опирались на рекомендации Вишневского А.А., Рудакова С.С. и Миланова Н.О. с соавторами (2005), полагающими, что термин «послеоперационный стерномедиастинит» является собирательным, с учётом известных классификаций медиастенитов Иванова А.Я. (1959), а также «Классификации острого медиастинита» М.М. Абакумова (2010), так как инфицирование грудины практически почти всегда сопровождается поражением не только подкожной жировой клетчатки, но с вовлечением ребер, хрящей, мышц грудной стенки, ключиц, переднего средостения. В нашем исследовании мы использовали уровень отрицательного давления (ОД) -50 мм рт. ст. (min) и -125 мм рт. ст. (max), поскольку применение ОД в нижнем и среднем терапевтическом диапазоне является наиболее эффективным. Для переменной вакуум-терапии использовался аспиратор “Suprasorb CNP P1”. При VAC-терапии в режиме постоянного разряжения давление устанавливалось на уровне 120-170 мм рт. ст. Для создания постоянного вакуумного разряжения нами использовался аппарат “Medela Vario-18 ac/dc”.
При открытом способе ведения перевязки совершались от 2 до 5 раз в сутки. Частота перевязок определялась скоростью экссудации раны. Повязки пропитывались комбинированным антимикробным препаратом для местного применения (Хлорамфеникол + Метилурацил). Вне зависимости от метода лечения санация раны при перевязках производилась с применением растворов хлоргексидина и бетадин-йода. Исследование проведено с разрешения Этического комитета ФГБОУ ВО «ТГМУ» и ФГАОУ ВО «ДВФУ». Данные о распределении пациентов по группам представлены в таблице.
Распределение пациентов по методам послеоперационного лечения
|
№ группы |
Методы послеоперационного лечения |
Количество пациентов |
|
1 |
Переменного вакуумного разряжения |
13 |
|
2 |
Постоянного вакуумного разряжения |
14 |
|
3 |
Метод открытого ведения |
30 |
|
Итого: |
57 |
|
Для решения вопросов о возможных механизмах репаративной регенерации в условиях открытого метода лечения с применением постоянного и переменного вакуума с помощью морфологических методов исследования нами была получена объективная оценка регенерации в поврежденных тканях. Для сравнительной оценки забор тканей для исследований производился в день выявления ПСМ и через каждые 4 дня после выявления и начала лечения ПСМ, во время проведения хирургических санаций постстернотомных ран по показаниям, в объеме тканей не более 1 мм3.
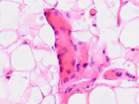
Результаты исследования и их обсуждение. Из биоптатов, взятых во время хирургических манипуляций, в дальнейшем были изготовлены срезы для исследования исходной ткани классическими морфологическими методами с дальнейшим окрашиванием гематоксилином и эозином. Препараты характеризовались высоким содержанием жировой ткани и кровеносных сосудов с прослойками рыхлой волокнистой соединительной ткани (рис. 1).
 а
а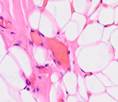 б
б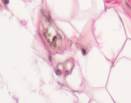 в
в
 г
г  д
д
Рис. 1. Биоптаты тканей послеоперационной раны, полученные в момент проведения хирургической манипуляции (пациент с нормальной массой тела и без сахарного диабета) (а-д). Окраска гематоксилином и эозином. Микрофото. Увеличение х200
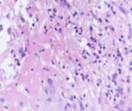
Биоптаты с зоны раневой поверхности, взятые у пациентов с сахарным диабетом 2 типа, после проведения лечения: открытым методом ведения раны (рис. 2, 3).
 а
а 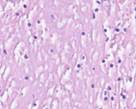 б
б 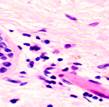 в
в 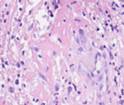 г
г
Рис. 2. Поверхностный лейкоцитарно-некротический слой; лейкоцитарная инфильтрация в ране на препарате из биоптата зоны раневой поверхности пациентов с сахарным диабетом 2 типа, после лечения: а) методом открытого ведения; б) с применением переменного вакуумного дренирования; в, г) с применением постоянного вакуумного дренирования. Окраска гематоксилином и эозином. Микрофото.
Увеличение: а, б, г) х200; в) х400
 а
а 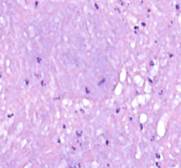 б
б
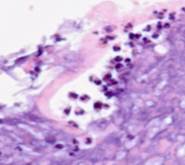
Рис. 3. Сосудистый слой грануляций. Лейкоцитарная инфильтрация за пределы сосуда в ране на препарате из биоптата зоны раневой поверхности пациента, страдающего сахарным диабетом 2 типа, после лечения с применением переменного вакуумного дренирования. Окраска гематоксилином и эозином. Микрофото. Увеличение х200. Идентифицируются гиперемированные сосуды (а), инфильтрация ткани (б)
Отличительной особенностью этой стадии раневого процесса является соединение краев раны грануляциями, а не рубцом. Сменяющая отёк воспалительная реакция расплавляет мертвые ткани и очищает рану, а по мере ее завершения начинают развиваться грануляции, постепенно заполняющие возникший дефект.
Анализ микропрепаратов показал, что наименьшая гиперемия и отёк во всех группах пациентов при различной патологии на I этапе заживления наблюдается при лечении методом переменной VAC-терапии (рис. 4).
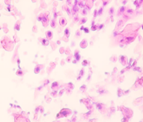 а
а 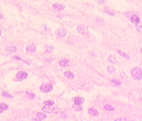 б
б 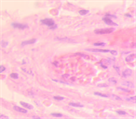 в
в
Рис. 4. Кровеносные сосуды на препарате из биоптата зоны раневой поверхности пациента без избыточной массы тела и сахарного диабета на 4-е сутки после диагностики ПСМ и хирургической санации постстернотомной раны после лечения: а) методом открытого типа; б) методом переменного вакуумного дренирования; в) методом постоянного вакуумного дренирования. Окраска гематоксилином и эозином. Микрофото. Увеличение х200
Грануляции имеют различный вид в зависимости от стадии развития. Нормальные грануляции изначально имеют вид нежнозернистой ткани, покрытой мутноватым, серо-зеленоватым налетом, сочной, богатой тонкостенными сосудами, из-за чего легко кровоточат. В более поздних периодах они становятся бледнее, плотнее, зернистость исчезает, превращаясь в беловатый плотный рубец.
Грануляции состоят из шести постепенно переходящих друг в друга слоев: поверхностный лейкоцитарно-некротический слой; поверхностный слой сосудистых петель; слой вертикальных сосудов; созревающий слой; слой горизонтально расположенных фибробластов; фиброзный слой.
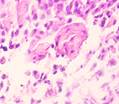
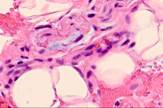
В наблюдениях за пациентами с открытым методом лечения было установлено, что на границах между краями раны на 4-е сутки появляются грануляции. Они состоят из множества гранул, которые тесно прижаты друг к другу. В их состав входят: амфорные вещества, петлевидные сосудистые капилляры, гистиоциты, фибробласты, полибласты, лимфоциты, многоядерные блуждающие клетки, коллагеновые и эластические волокна и сегментоядерные лейкоциты. В группе пациентов с применением переменного вакуумного дренирования выявлено более раннее появление грануляций: через двое суток на свободных от кровяных сгустков и некротизированной ткани участках можно заметить розово-красные узелки - величиной с просяное зерно гранулы. На третий день количество гранул значительно возрастает, и уже на 4-5-е сутки поверхность раны покрывают молодые грануляции. Здоровые крепкие грануляции розовато-красного цвета не кровоточат, имеют равномерный зернистый вид, очень плотную консистенцию, выделяют небольшое количество гнойного мутного экссудата. В нем содержится большое количество погибших клеточных элементов местной ткани, гнойные тельца, примеси эритроцитов, сегментоядерные лейкоциты, та или иная микрофлора с продуктами собственной жизнедеятельности. В данный экссудат происходит эмиграция клеток ретикулоэндотелиальной системы, белых кровяных телец, сюда же врастают сосудистые капилляры и фибробласты. На препаратах идентифицируются грануляции, представленные большим количеством мелких полнокровных кровеносных сосудов (капилляров, артериол), между которыми располагаются многочисленные пролиферирующие клеточные элементы, представленные гистиоцитами, лимфоцитами, плазматическими клетками, эпителиоидными клетками и фибробластами. Во всех случаях отмечается более активный ангиогенез при применении переменного вакуумного дренирования (рис. 5).
 а
а 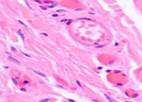 б
б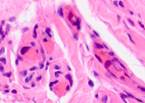 в
в 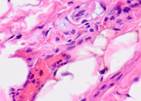 г
г
 д
д 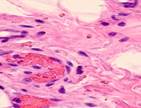 е
е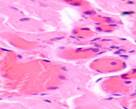 ж
ж
Рис. 5. Кровеносные сосуды на препарате из биоптата зоны раневой поверхности пациента с ХОБЛ, после лечения: а) методом открытого ведения; б-е) с применением переменного вакуумного дренирования; ж) с применением постоянного вакуумного дренирования. Окраска гематоксилином и эозином. Микрофото. Увеличение х200
При воздействии на раневую поверхность переменного вакуумного дренирования отмечается более раннее созревание грануляций, уменьшение количества кровеносных сосудов, заполнение раневой поверхности созревающей соединительной тканью и более ранняя эпителизация раневой поверхности (рис. 5 б-е).
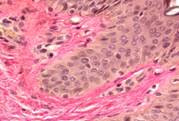
В ходе второго периода репарации молодые грануляции, расположенные между краями раны, быстро созревают, сопровождаясь активным образованием коллагена. Это ведет к уменьшению количества сосудов и клеточных элементов, с одной стороны, и увеличением числа коллагеновых и эластических волокон, с другой (рис. 6).
 а
а 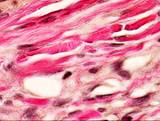 б
б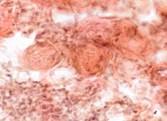 в
в
Рис. 6. Кровеносные сосуды на препарате из биоптата зоны раневой поверхности пациента с хронической почечной недостаточностью, после лечения: а) методом открытого ведения; б) с применением переменного вакуумного дренирования; в) с применением постоянного вакуумного дренирования. Окраска по Ван Гизону. Микрофото. Увеличение х200
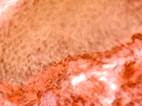
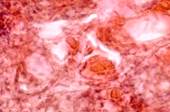
Третья стадия репарации характеризуется активным ростом соединительной ткани с образованием прочного рубца. В ходе этого периода количество волокнистых структур в рубце значительно увеличивается, а их пучки приобретают определенную ориентацию в соответствии с доминирующим направлением нагрузки. Соответственно, количество клеточных элементов и сосудов существенно уменьшается (рис. 7).
 а
а 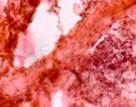 б
б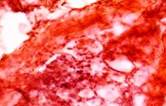 в
в
 г
г 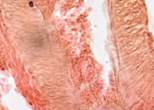 д
д 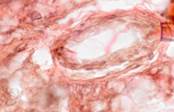 е
е
Рис. 7. Препарат из биоптата зоны раневой поверхности пациентов с хронической почечной недостаточностью, через 25 дней после диагностики ПСМ из группы: а) открытого метода ведения; б-г) переменного вакуумного дренирования; д, е) постоянного вакуумного дренирования. Окраска по Ван Гизону. Микрофото. Увеличение х200
Перестройка рубцовой ткани с усилением продольной ориентации волокон сопровождается уменьшением числа клеточных элементов и сохранением единичных мелких сосудов. Наибольшее количество волокон с правильной ориентацией в рубцовой ткани обнаруживалось в группах с применением вакуумного дренирования (рис. 8).
 а
а 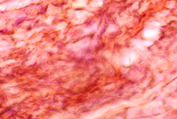 б
б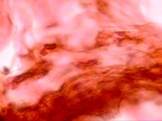 в
в
Рис. 8. Формирование соединительнотканного рубца у пациентов с ожирением на 45-е сутки лечения с применением: а) переменного вакуумного дренирования; б, в) постоянного вакуумного дренирования. Окраска по Ван Гизону. Микрофото. Увеличение х200
Гистологические методы исследования позволили установить, что вакуумное дренирование улучшает течение раневого процесса путем:
1) уменьшения локального отека;
2) усиления местной тканевой перфузии;
3) снижения уровня микробной загрязнённости раны;
4) целенаправленной деформации раневого ложа и уменьшения объема раневой полости;
5) снижения степени раневой экссудации;
6) поддержания оптимальной влажности раневой среды, необходимой для нормального заживления раны.
Анализ результатов клинических и морфологических наблюдений показал, что в группах пациентов с сахарным диабетом 2 типа при открытом методе ведения и при применении постоянного вакуумного дренирования (в сравнении с применением переменного вакуумного дренирования): отёк и инфильтрация окружающей рану ткани протекают более длительно; созревание грануляций, сопровождающееся ростом капилляров и артериол в грануляциях, идёт значительно медленнее, как и дальнейшее запустевание сосудов с уменьшением числа клеточных элементов соединительной ткани и мигрантов из кровяного русла.
Заключение. Применение вакуумного дренирования в переменном режиме индуцировало регенераторные процессы в зоне раневой поверхности в большей степени, в сравнении с группами постоянного вакуумного дренирования и открытого метода ведения, и позволило достигнуть увеличения количества волокон в рубцовой ткани и их правильной ориентации в соответствии с доминирующим направлением нагрузки в более ранние сроки. Преимуществом влияния вакуумного дренирования на раневой процесс, в сравнении с открытым методом ведения, является более выраженная стимуляция роста и улучшение качества грануляций. Вследствие того что вакуумная повязка, путем направленной деформации тканей, сокращает объем раневой поверхности, размеров раны, дополнительная мобилизация местных тканей перед вторичным закрытием раны может не понадобиться. Наложение вакуумного дренирования на рану позволяет удалять избыточный раневой экссудат, стимулирует ангиогенез.
Работа выполнена при поддержке Научного фонда ДВФУ, в рамках государственного задания 17.5740/2017/6.7.
Библиографическая ссылка
Фургал А.А., Рева И.В., Рева Г.В., Сорокин В.А., Гармаш Р.А., Гармаш А.И., Купатадзе Д.Д., Одинцова И.А., Верин В.К. ВАКУУМНОЕ ДРЕНИРОВАНИЕ ПРИ ЛЕЧЕНИИ ПОСЛЕОПЕРАЦИОННЫХ СТЕРНОМЕДИАСТИНИТОВ В КАРДИОХИРУРГИИ // Современные проблемы науки и образования. 2018. № 6. ;URL: https://science-education.ru/ru/article/view?id=28381 (дата обращения: 14.01.2026).
DOI: https://doi.org/10.17513/spno.28381



