Лечение пациентов со статическими деформациями стопы, в частности с поперечным плоскостопием, осложненным hallux valgus и деформациями II–IV (малых) пальцев стопы, имеет многовековую историю, о чем свидетельствуют труды Галена и Гиппократа. В настоящее время данное страдание является причиной каждого третьего обращения к специалисту, занимающемуся патологией стопы и голеностопного сустава [1]. При этом деформации малых пальцев встречаются у 28–32% пациентов, а частота хирургических вмешательств на малых пальцах достигает от 28 до 48% от всех операций на переднем отделе стопы [2].
При подготовке данного обзора авторы преследовали следующую цель: провести анализ данных мировой литературы по применению метода проксимального межфалангового артродеза в различных модификациях с учетом зафиксированных осложнений и оценить необходимость дальнейшего совершенствования данного метода лечения.
По данным литературы исследователи и практикующие врачи при хирургическом лечении фиксированной молоткообразной деформации II–IV пальцев отдают предпочтение хирургическим вмешательствам на проксимальном межфаланговом суставе. История внедрения в практику этих хирургических методов началась более 200 лет тому назад, когда Post предложил резецировать головку проксимальной фаланги пораженного пальца [3]. В начале XX века этот метод оперативного лечения был научно обоснован и получил широкое распространение благодаря работам немецкого хирурга Hohmann. До настоящего времени операция Hohmann остается востребованной среди практикующих ортопедов. Однако артропластическая резекция и формирование фиброзного анкилоза проксимального межфалангового сустава влекут за собой нарушение функции корригированного пальца стопы, являются причиной недопустимо высокого количества остаточных деформаций и низкой удовлетворенности пациентов [4]. Исходя из этого для лечения пациентов с фиксированной молоткообразной деформацией малых пальцев все большее число ортопедов отдают предпочтение операции артродеза проксимального межфалангового сустава в физиологически правильном положении, а формирование костного блока исключает риск вторичного смещения и снижает количество рецидивов деформации [5, 6]. Артродез проксимального межфалангового сустава впервые предложил Soule в 1882 году [3]. В последующем было описано множество модификаций этого хирургического метода. Однако основное различие этих модификаций заключается в выборе способа фиксации костных фрагментов [3, 6, 7]. В результате в настоящее время существует огромное количество фиксаторов и методов фиксации фаланг пальцев (в том числе трансартикулярная фиксация спицей Киршнера, фиксация проволочным швом, канюлированным винтом, биодеградируемым пином, скобами из нержавеющей стали или из металла с памятью формы и т.д.). В последнее десятилетие все большую популярность завоевывают имплантаты для интрамедуллярного остеосинтеза [7–10]. Каждый из этих методов фиксации имеет свои преимущества и недостатки, потенциальные риски и осложнения, но «золотой стандарт» в хирургическом лечении фиксированной молоткообразной деформации малых пальцев так и не установлен.
Наиболее распространенным способом фиксации при артродезе проксимального межфалангового сустава стопы является чрескожная трансартикулярная фиксация спицей Киршнера, которую впервые описал в 1940 году Taylor [11]. Этот метод стал очень популярным из-за доступности, простоты применения и минимальной затратности [8, 12, 13]. На фоне своих преимуществ этот метод обладает существенными недостатками, такими как миграция и/или переломы металлоконструкции, высокая частота несращений зоны артродеза и инфекционные осложнения в области проминирования спицы (выхода спицы на кожу), что может приводить к рецидиву деформации и необходимости повторных оперативных вмешательств [13, 14]. По данным ряда авторов, несращения скрепляемых фаланг после операции Taylor могут встречаться более чем у 20% пациентов [15]. Большое количество псевдоартрозов, вероятно, обусловлено отсутствием ротационной стабильности и подвижностью костных фрагментов в зоне артродеза, что и нарушает процессы консолидации [16]. Стоит подчеркнуть, что до сих пор четко не определены продолжительность фиксации и сроки удаления спицы, большинство авторов рекомендуют ее удаление в сроки от 3 до 6 недель после операции. Так, Klammer и соавторы утверждали, что 6 недель фиксации не приводят к увеличению частоты инфекции, но улучшают стабильность и снижают риски смещений и рецидивов деформаций [14]. При этом Reece и соавторы отмечают, что при сроке фиксации больше 6 недель частота инфекционных осложнений ровна 18%, что является недопустимо высоким [17, 18]. Также необходимо отметить интраоперационные проблемы, связанные с проведением спицы, такие как нарушение кровоснабжения пальцев в результате натяжения сосудисто-нервного пучка и повреждение хряща смежных интактных суставов [19, 20]. Кроме того, выступающая на кончике корригированного пальца спица нуждается в защите повязкой и постоянном уходе в послеоперационном периоде, а ее удаление вызывает беспокойство и боль у пациентов [14].
Чтобы избежать описанных недостатков традиционного метода, Creighton и соавторы [21] в 1995 году предложили использовать погружную фиксацию спицей Киршнера для проксимального межфалангового артродеза малых пальцев стопы (рис. 1 А), а Camasta и Cass в 2008 году описали оригинальную методику использования спицы Киршнера как интрамедуллярного фиксатора [22]. Авторы отметили снижение количества осложнений. При анализе 50 первых операций ни одного случая несостоятельности металлоконструкций (миграции или инфекции) авторы не встретили. Однако согласно Scholl (2013) хорошие результаты коррекции были достигнуто только у 24 (85,7%) пациентов согласно его сообщению о результатах проксимального межфалангового артродеза у 28 пациентов с фиксацией погружной спицей Киршнера. По его же данным, костный блок в зоне артродеза был достигнут у 22 (82,1%). Несостоятельность металлоконструкций в виде перелома спиц зафиксирована у 2 (7,1%) пациентов, а ревизионных вмешательств потребовали 3 (10,7%). Однако автор отмечает преимущества данного метода над использованием интрамедуллярного имплантата с памятью формы [23].
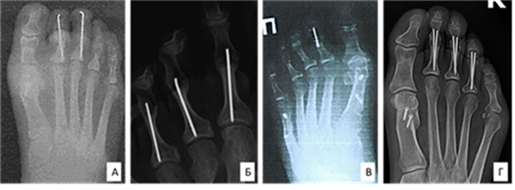
Рис. 1. Способы межфалангового артродеза малых пальцев стопы методом погружной фиксации: метод Creighton R.E. спицей Киршнера (А) [21]; метод Canales M.B. фиксации спицей с резьбой (Б) [24]; метод Тертышника С.С. с использованием шурупа 1,5 мм с резьбой (В); метод Hood C. R. фиксацией двумя расходящимися спицами Киршнера (Г) [25]
Canales и соавторы в 2014 году, указывая на недостатки метода Camasta и Cass, в частности на недостаточную стабильность скрепляемых фрагментов, предлагают свою модификацию с использованием спицы с резьбой (рис. 1 Б). При этом они сообщают о хороших результатах коррекции 217 пальцев, но описывают 6 случаев осложнений, в том числе 1 случай ранней нестабильности и глубокой инфекции [24]. Схожий метод был предложен группой отечественных авторов (рис. 1 В) и защищен патентом № RU 2 487 683 C1 (2013). В качестве погружного имплантата авторы используют шуруп с мелкой фрагментарной резьбой диаметром 1,5 мм. При установке шурупа скусывают его шляпку, осуществляют последующее «навинчивание» проксимальной и средней фаланги с плотным прижатием торцевых поверхностей, за счет чего создают компрессионные усилия. Однако авторы не приводят данные результатов использования метода в клинической практике. В 2016 году Hood для артродеза проксимального межфалангового сустава предлагает метод фиксации двумя расходящимися интрамедуллярными спицами Киршнера при лечении молоткообразной деформации пальцев стопы (рис. 1 Г). Стоит отметить, что авторы описанных методов в своих работах делают акцент на хирургическую технику и не приводят данные анализа удовлетворенности пациентов, не указывают количество сформированных костных межфаланговых анкилозов, также отсутствуют группы сравнения. При этом все подчеркивают необходимость дальнейших исследований [25].
В ряде источников авторы при артродезировании проксимального межфалангового сустава малых пальцев стопы описывают метод фиксации фаланг малых пальцев петлей из нержавеющей стальной проволоки (рис. 2) [26, 27]. К сожалению, приведенные источники страдают низким уровнем достоверности исследования – в этих исследованиях нет данных о количестве пациентов, получавших лечение с использованием этой техники, не указана частота осложнений и отсутствует группа сравнения. В некоторых случаях для достижения стабильной фиксации авторы использовали временную чреcкожную установку спицы Киршнера.
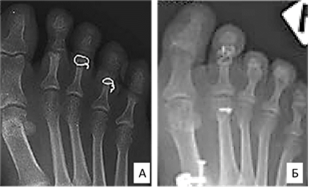
Рис. 2. Способы межфалангового артродеза малых пальцев стопы с внутрикостной фиксацией проволокой: метод Harris W. V. фиксация петлей (А) [26]; метод Gutteck N. S. фиксация восьмиобразной петлей (Б) [27]
Артродез проксимального межфалангового сустава с фиксацией интрамедуллярным канюлированным винтом впервые был описан Caterini и соавторами в 2004 году [28]. В своей статье авторы отмечают высокую частоту (до 94%) формирования костных блоков в зоне артродеза и ни одного случая рецидива деформации. При этом в 13% случаев конструкция была удалена в результате ее несостоятельности, инфекции или боли, вызванной конфликтом в области головки винта на «подушечке» пальца (рис. 3 А).
В современной специализированной литературе, к сожалению, немного источников, где авторы отмечают, что артродез проксимального межфалангового сустава с использованием канюлированного винта является простым, надежным и эффективным способом [29, 30]. При этом преимуществом данного метода является низкая частота несращений и рецидивов деформаций, что, по мнению авторов, обусловлено стабильной компримирующей фиксацией, возможностью ранней активизации пациента, а также легкостью удаления конструкций. Недостатками этой методики являются: повреждение дистального межфалангового сустава из-за трансартикулярного введения винта (рис. 3 Б) и необходимость повторной операции для удаления металлоконструкции. Авторы этих статей в выводах подчеркивают необходимость последующих исследований с оценкой долгосрочных результатов лечения [28, 29].
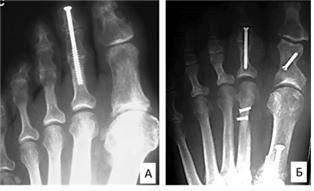
Рис. 3. Способы межфалангового артродеза малых пальцев стопы канюлированным интрамедуллярным винтом: метод Caterini R. введение винта с кончика пальца (А) [28]; метод Lane G.D. введение винта через головку средней фаланги (Б) [29]
В последние годы ортопеды в лечении данной группы больных все большее предпочтение отдают интрамедуллярным конструкциям. На мировом рынке медицинских изделий представлено около 68 разнообразных имплантатов, созданных для проксимального межфалангового артродеза малых пальцев стопы [30, 31].
Все интрамедуллярные имплантаты принято разделять на четыре категории в соответствии с техническими характеристиками и составом материалов согласно предложению Guelfi [32].
1. Биоактивные имплантаты, изготовленные из аллокости: поскольку эти устройства являются трансплантатами. Они обладают остеоиндуктивными и остеокондуктивными свойствами, что значительно улучшает их интеграцию. К этой группе также можно отнести биодеградируемые конструкции.
2. Формообразующие устройства из металла с памятью формы (Memometal, NiTinol), которые активируются температурой тела, изменяя свою форму после имплантации, и обеспечивают стабильность фиксации.
3. Двухкомпонентные имплантаты: после установки компонентов (одного в проксимальную фалангу, а другого – в среднюю) они скрепляются вместе.
4. Однокомпонентные имплантаты. При использовании этих имплантатов проксимальная часть ввинчивается в основную фалангу, а средняя фаланга насаживается на дистальную часть. Канюлированный тип также позволяет использовать спицу в качестве направителя. Они могут изготавливаться из стали, титана или полимеров.
В 2011 году Konkel и соавторы для артродеза проксимальных межфаланговых суставов малых пальцев стопы использовали биодеградируемые пины у 33 больных (47 пальцев стопы) и сообщили о хороших результатах в 28 (87%) случаях [33]. В 2017 году Wendelstein описывает результаты проксимального межфалангового артродеза у 34 пациентов с использованием биодеградируемого винта TRIM-IT 2,7 мм (рис. 4 А, Б). Преимущество биодеградируемого винта над пином – это возможность сжатия фрагментов в зоне артродеза. Теоретически это создает условия для лучшей репарации костной ткани. Однако при использовании винта TRIM-IT согласно результатам этого исследования костное сращение в зоне артродеза было достигнуто только в 28 (84,6%) случаях, а у двух (7,7%) пациентов имел место рецидив деформации. При этом один (3,8%) пациент потребовал повторного вмешательства для коррекции остаточных деформаций [34]. Авторы обеих статей отметили, что использование интрамедуллярных рассасывающихся конструкций позволило добиться лучших результатов с минимальным количеством осложнений и высокой удовлетворенностью пациентов. Другие исследователи полагают, что биодеградируемые имплантаты могут быть хорошей альтернативой металлоконструкциям у пациентов с аллергией на металл. Однако биодеградируемые конструкции широко не применяются в связи с рядом недостатков, таких как местное токсическое действие деградируемого полимера, низкие прочностные характеристики имплантатов. Основной же проблемой, не позволяющей широко использовать эти материалы, является их высокая стоимость [34–36].
В 2002 году Miller опубликовал результаты исследования, которое показало, что для проксимального межфалангового артродеза малых пальцев стопы можно использовать пин, изготовленный из лиофилизированной кортикальной аллокости (bone allograft pin) (рис. 4 В). При анализе результатов лечения у 26 пациентов автор отмечает несостоятельность фиксатора у двух (7,7%) пациентов, при этом один из них потребовал ревизионного хирургического вмешательства. У всех остальных пациентов был сформирован костный блок в зоне артродеза, при этом полная резорбция трансплантата произошла к 5–6-му месяцу с момента операции [37]. В отличие от металлических имплантатов и других рассасывающихся конструкций, фиксаторы, изготовленные из аллокости, обладают остеокондуктивными свойствами и замещаются костной тканью после резорбции [38]. Имплантаты из кортикальной кости обладают низкой биотканевой активностью и достаточной прочностью, но обеспечивают минимальное сжатие скрепляемых фрагментов. Стоит отметить, что по данным некоторых авторов костные аллотрасплантаты несут риск передачи инфекционных заболеваний [39]. В 2013 году Kominsky и соавторы опубликовали результаты лечения 63 пациентов с использованием интрамедуллярного имплантата TENFUSE Allograft (рис. 4 Г, Д). При этом авторы утверждают, что имплантат из аллокости, помимо надежной фиксации, обладает остеоиндуктивными и остеокондуктивными свойствами, что улучшает процесс сращения в зоне артродеза, и сообщают о 97% костных анкилозов за четырехмесячный период наблюдений [40]. Однако металлические изделия по-прежнему остаются более популярными для фиксации из-за их высокой прочности, универсальности, легкости имплантации и инертности к окружающим тканям. Тем не менее металлические имплантаты значительно более жесткие, чем кость, что может вызвать региональную остеопению вследствие перераспределения нагрузки, а для их удаления требуется повторная операция [39].
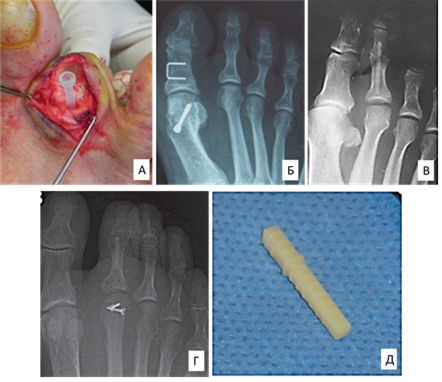
Рис. 4. Способы межфалангового артродеза малых пальцев стопы биоактивными имплантатами, изготовленными из аллокости или из биодеградируемых материалов: способ фиксации биодеградируемым винтом TRIM-IT 2,7 мм (внешний вид имплантата в ране (А) и контрольная рентгенограмма через 34 месяца после операции (Б)) [34]; метод Miller S.J. с фиксацией пином, изготовленным из лиофилизированной кортикальной аллокости (В) [37]; использование имплантата TENFUSE Allograft (послеоперационный рентгенконтроль (Г) и внешний вид имплантата (Д)) [40]
Согласно литературным данным из металлических имплантатов наиболее хорошо описаны устройства второй группы, в частности имплантат Smart Toe (рис. 5 А) [23, 41-43]. Он изготовлен из нитинола – металла с памятью формы. Данное устройство хранится при температуре 0°C и после имплантации при нагревании до температуры тела увеличивается в ширине (≤3 мм) и укорачивается в длину (≤2 мм). Такое изменение имплантата на месте установки и конструктивные особенности, по мнению авторов, создают компрессию скрепляемых костных поверхностей и обеспечивают трехплоскостную стабильность. Тем не менее Catena в своем исследовании использовал это устройство в сочетании со спицей Киршнера, чтобы увеличить надежность фиксации скрепляемых фаланг пальца. Спица удалялась через 3–4 недели после оперативного вмешательства [42]. В своем исследовании Khan при сравнении результатов лечения пациентов с молоткообразной деформацией малых пальцев с использованием имплантата Smart Toe и традиционного метода фиксацией спицей Киршнера пришел к выводу, что статистически значимых различий при использовании данных методов нет [43]. Однако рентгенографические признаки сформированного артифициального костного блока в зоне артродеза установлены только у 68,8% пациентов, что значительно ниже по сравнению с предыдущими исследованиями этого имплантата [41, 42, 44]. Частота несостоятельности металлоконструкций в группе исследования была впечатляющей и составила 20,7%, что в 3 раза превышает данный показатель в группе сравнения. Такие результаты авторы связывают с ограниченным выбором хирургом подходящего имплантата по длине и ширине и трудностями в технике его установки, которые учтены при создании второго поколения данного устройства и требуют дальнейших исследований [43]. Однако такие данные в доступной литературе не встречены.
В 2010 году Ellingt опубликовал анализ рентгенограмм результатов хирургического лечения 28 пациентов с молоткообразной деформацией малых пальцев стопы с использованием двухкомпонентного устройства StayFuse (рис. 5 Б). Коррекция деформации сохранялась у 23 (82%) пациентов, но только у 17 (61%) автор отмечает формирование костного блока в зоне артродеза, а 3 (8%) пациентам было проведено ревизионное хирургическое лечение. Во всех случаях это было связано с несостоятельностью металлоконструкции: у одного пациента произошел перелом имплантата, а у двух других – его разъединение, что является недостатком данной группы устройств [45]. Схожие результаты получили Jay и соавторы в 2016 году, проведя рандомизированное исследование использования двухкомпонентного имплантата Nextra в сравнении с чрескожной фиксацией спицей Киршнера (рис. 5 В). Авторы отмечают положительное влияние внутренней фиксации на комфортность послеоперационного периода лечения, скорость реабилитации, удовлетворенность пациентов результатами хирургического лечения. При этом авторы не отмечают ни одного осложнения, связанного с несостоятельностью металлоконструкций или инфекцией, однако число фиброзных анкилозов составило 42%, что является недопустимо высоким [46]. Таким образом, установка проксимальной и дистальной частей имплантата данной группы сопряжена с тонким балансом создания плотного соприкосновения сочленяющихся поверхностей и надежной фиксации пазов фиксатора, что иногда является трудной задачей и чревато формированием фиброзного блока в зоне артродеза или несостоятельностью конструкции.
Наименее изученной группой имплантатов для коррекции молоткообразной деформация являются интрамедуллярные конструкции четвертой группы. При этом авторы единичных исследований отмечают хорошие результаты коррекции деформации, значительное уменьшение боли и сохранение функции оперированного пальца с низкой частотой осложнений. Так, в 2014 году Coillard опубликовал исследования с оценкой результатов лечения 117 пациентов (156 корригированных малых пальцев стопы), которым был выполнен проксимальный межфаланговый артродез с использованием канюлированного однокомпонентного имплантата Ipp-On [47]. Авторы отмечают два интраоперационных осложнения в виде перелома проксимальной фаланги малого пальца при установке конструкции, три случая миграции имплантата и один случай его несостоятельности (перелом фиксатора), что потребовало ревизионных вмешательств. Костный блок зоны артродеза был сформирован в 98 (83,8%) случаях через год с момента операции, рецидив деформации отмечен у 3 (3,1%) пациентов. При этом автор отмечает высокую удовлетворенность пациентов результатами хирургического лечения (98% случаев), также отмечает значительное улучшение функциональных результатов и снижение болевого синдрома через 1 год после операции. Схожие результаты в 2016 году были получены отечественным травматологом А.М. Приваловым при использовании имплантата Ipp-On в лечении 13 пациентов (рис. 5 Г, Д), при этом авторы также отмечают высокую эффективность использования интрамедуллярной конструкции при хирургическом лечении тяжелой степени молоткообразной деформации пальцев стопы даже при ревизионных вмешательствах [48].
В 2012 году Witt и Hyer сообщили о серии оперативного лечения фиксированной молоткообразной деформации семи пальцев у 3 пациентов с использованием монолитного интрамедуллярного имплантата из нержавеющей стали (PRO-TOE) (рис. 5 Е, Ж). Авторы отмечают отсутствие интраоперационных или послеоперационных осложнений за однолетний период наблюдения. При этом они сообщили, что данный имплантат является альтернативой трансартикулярной фиксации спицей Киршнера, и отметили ряд технических преимуществ данного имплантата, включая уплощенную «елочкообразную» форму дистальной его части, что улучшает стабильность скрепляемых фрагментов в зоне артродеза. Также авторы предположили, что имплантат из одного компонента является более надежной конструкцией, чем двухкомпонентный [49]. Схожие данные получил в 2015 году Basil при анализе результатов лечения 23 пациентов (54 пальца), при этом автор отмечает формирование костного блока проксимального межфалангового сустава в 20 (85%) случаях, высокую удовлетворенность пациентов, снижение болевого синдрома и улучшение функциональных показателей согласно шкале AOFAS [50].
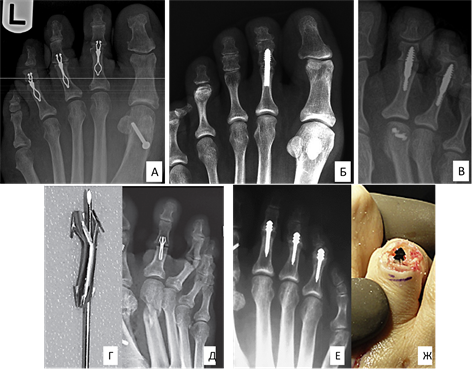
Рис. 5. Способы межфалангового артродеза малых пальцев стопы с использованием погружных имплантатов: имплантата Smart Toe, изготовленного из металла с памятью
формы (А) [23]; двухкомпонентных имплантатов StayFuse (Б) [45] и Nextra (В) [46]; интрамедуллярного имплантата Ipp-On (внешний вид имплантата (Г) и контрольная рентгенограмма после операции (Д)) [47]; монолитного однокомпонентного имплантата PRO-TOE (послеоперационный рентгенконтроль (Е) и внешний вид имплантата в ране (Ж)) [49]
Заключение
Таким образом, актуальность проблем лечения пациентов с молоткообразной деформацией малых пальцев стопы не утратила своего значения, а детальное изучение патогенеза данного страдания в последние 10–15 лет дало новый импульс к совершенствованию подходов хирургического лечения. В настоящее время большинство исследователей и практикующих травматологов-ортопедов сообщают о высокой эффективности выполнения артродеза проксимального межфалангового сустава в лечении пациентов с фиксированной молоткообразной деформацией, при этом результаты во многом зависят от надежности фиксации скрепляемых фрагментов. Традиционным методом фиксации считается чрескожная трансартикулярная фиксация спицей Киршнера, однако этот метод на фоне своих достоинств обладает рядом серьезных недостатков. Таким образом, задачей современной ортопедии является разработка метода, исключающего эти недостатки. Для решения этой задачи в настоящее время предложены десятки методов интрамедуллярной фиксации погружными фиксаторами. При этом первичный анализ результатов использования погружной фиксации спицами, канюлированных винтов, биодеградируемых имплантатов, фиксаторов, изготовленных из металла с памятью формы, двухкомпонентных имплантатов показал их недостатки. Наиболее эффективными фиксаторами являются однокомпонентные монолитные интрамедуллярные металлические имплантаты.
Библиографическая ссылка
Гуди С.М., Епишин В.В., Пахомов И.А., Корочкин С.Б., Кузнецов В.В. ПРОКСИМАЛЬНЫЙ МЕЖФАЛАНГОВЫЙ АРТРОДЕЗ В КОМПЛЕКСЕ ЛЕЧЕНИЯ ПАЦИЕНТОВ С МОЛОТКООБРАЗНОЙ ДЕФОРМАЦИЕЙ МАЛЫХ ПАЛЬЦЕВ СТОПЫ // Современные проблемы науки и образования. 2018. № 6. ;URL: https://science-education.ru/ru/article/view?id=28341 (дата обращения: 15.02.2026).



