Создание биодеградируемых материалов и конструкций для нужд пациентов ортопедии и травматологии является ветвью глобальной проблемы современной цивилизации – проблемы переработки «твердых бытовых отходов». При этом новизна биодеградируемых конструкций (БК) является надуманной – врачи используют БК с незапамятных времен – первое упоминание о биодеградируемом шовном материале встречается в трудах Галена в 175 году до Рождества Христова [1]. Количество биодеградируемых веществ и производимых из них погружных конструкций велико. Основными веществами для производства биодеградируемых конструкций являются керамикоподобные вещества, полимеры, комбинированные полимеры. Среди веществ, подобных керамике, заслуживает упоминания, прежде всего, фосфат кальция за счет своего сродства к неорганической части человеческой кости, и в том числе к патологическим обызвествленным тканям человека. Бета-трикальций фосфат (â- TCP) и гидроксиапатит обладают способностью к стимуляции образования новой кости. К сожалению, перечисленные материалы имеют недостаточную прочность и не могут использоваться как конструкции, самостоятельно несущие нагрузку весом тела [1].
Среди полимеров наиболее полезные свойства для травматологии и ортопедии продемонстрировали полигликолид (PGA), полилактид (PLA), смесь полигликолида с полилактидом в различных пропорциях, полидиоксанон (PDS), пропилен (PP), полисульфон (PS), и поликарбонат (PC). Среди всех предпочтительными являются полигликолид (PGA), полилактид (PLA) и их смеси в связи с полезным свойством – увеличивать прочность конструкции при набухании в тканях. Комбинированные полимеры представлены в основном смесью PLA и PGA в различных соотношениях в зависимости от предпочтений производителя: изменяя соотношение ингредиентов можно манипулировать как прочностью имплантов, так и длительностью их деградации [2; 3]. Впервые исследование свойств биодеградируемых конструкций для целей травматологии и ортопедии проведено Kulkarni et al. (1966) [4]. Ими была дана оценка биосовместимости поли-L-молочной кислоты (PLLA) с тканями лабораторных животных. Оценка веществу была дана положительная, с точки зрения низкой токсичности и способности используемого вещества постепенно деградировать в тканях. Это послужило основанием к использованию биодеградируемых конструкций в клинической, а точнее – в ветеринарной практике: Kulkarni et al. с успехом использовали винты для остеосинтеза переломов челюстей у собак, что вскоре было подтверждено другими исследователями [5]. Безусловно, прогресс в дизайне и производстве БК привел к повышению их безопасности и функциональной пригодности для лечения различных заболеваний и повреждений опорно-двигательного аппарата. При этом важной задачей для фундаментальной и прикладной науки в наше время является снижение стоимости как конструкций, так и лечения в целом [3]. Достижению этой цели может способствовать создание синтетических БК для травматологии и ортопедии, что повлечет изменения в тактике лечения за счет отсутствия необходимости во второй операции – удалении металлоконструкций [2]. Не менее важными преимуществами БК (по сравнению с металлическими) являются: невозможность их миграции, рентген-негативность [1]. Биодеградация импланта позволяет постепенный перенос нагрузки на срастающуюся кость, таким образом обеспечивая более физиологичные процессы ремодeлирования кости после повреждения и остеосинтеза. Эти теоретические выкладки вдохновили ученых, и первое исследование, описывающее применение БК в клинике, было представлено в 1966 году Kulkarni R.K. и др. [6]. Исследуя биосовместимость полимера молочной кислоты (PPLA) на животных, они показали нетоксичность материала, его деградацию без тяжелых воспалительных реакций со стороны окружающих тканей. Так началась эра БК-материалов в травматологии и ортопедии. Большинство клинических исследований описывали использование полимера гликолевой кислоты (PGA) и полимера молочной кислоты (PLA), о чем публиковалось в начале 90-х [5] годов ХХ века. В наше время множество компаний участвуют в производстве биодеградируемых конструкций; на рынке медицинских изделий предложены различные конструкции и импланты. Пины, шурупы из PGA и PLA, множество других изделий – мембраны, артроскопическая продукция - также доступны для использования. Уникальные механические свойства биодеградируемых материалов обеспечили использование в травматологии и ортопедии – PGA и PLA популярны среди хирургов ортопедов-травматологов. В наше время появились новые, более современные полиортоэстеры – poly[pdioxanone] (PDS), poly[e-caprolactone] (PCL), poly[b-hydroxybutyrate] (PHB) и poly[PHB hydroxyvalericacid] [6]. При этом большинство представленных на рынке биодеградируемых конструкций производятся из полимеров PGA и PLA. Вместе с тем прошло недостаточно времени с момента начала использования биодеградируемых конструкций в клинической практике для того, чтобы объективно судить об их возможных достоинствах и недостатках, прежде всего в практике отечественной травматологии и ортопедии. В связи с этим особое значение приобретают исследования, посвященные характеристике подобного рода имплантов, включая экономическую целесообразность их применения, что и определило цель нашего исследования.
Материалы и методы исследования. Проведено ретроспективное исследование результатов лечения 56 пациентов с разнообразной патологией стоп. Пациенты были разделены на контрольную и основную группы в зависимости от применяемых для лечения конструкций. В контрольную группу вошли 28 пациентов – 12 (42,9%) мужчин, 16 женщин (57,1%); средний возраст составил 44±6,5 лет. Основная группа была сформирована также из 28 пациентов, в ней насчитывалось 16 (57,1%) мужчин и 13 (42,9%) женщин. Средний возраст пациентов основной группы составил 45±5 лет. Всем пациентам проводились клиническое, рентгенологическое исследования, по показаниям проводились УЗИ, МРТ, МСКТ стоп при поступлении и в динамике. Для проведения клинико-экономического анализа определен средний койко-день, количество операций на одного пациента, средняя длительность операции, время, проведенное в реанимационном отделении. Всем пациентам производились реконструктивно-пластические операции на стопах. В контрольной группе пациентам для фиксации фрагментов костей применяли биостойкие металлоконструкции. В основной группе при проведении аналогичных хирургических вмешательств использованы БК. У всех пациентов после проведения лечения выполняли исследование функциональной активности поврежденного отдела стопы и голеностопного сустава для определения восстановления функции, опороспособности и выраженности болевого синдрома с использованием визуальной аналоговой шкалы выраженности болевого синдрома VAS по Wewers M.E. и Lowe N.K. (1990) и адаптированной анкеты американского общества подиатров AOFAS по Kitaoka H.B. et al. (1994). С учетом вышесказанного нами были сформированы совокупные критерии оценки исходного состояния и результатов лечения пациентов, включающие в себя данные всех методов обследования, на основе которых выделяли три вида клинических исходов (табл. 1). Оценку последних, наряду с характеристикой исходного состояния пациента до лечения, проводили в отдаленном периоде наблюдений после хирургического лечения (12 месяцев). Теоретическую и методологическую основу экономических расчетов составили положения и концепции, представленные в классических и современных работах по исследуемой проблематике. Были использованы такие общенаучные методы исследования, как логический, ситуационный, структурный и сравнительный анализ, контент-анализ; метод статистических группировок и экспертные оценки.
Информационную базу работы составили законодательные и нормативные акты Российской Федерации, постановления Правительства РФ, отчетные материалы, инструкции и статистические данные отделения эндопротезирования и эндоскопической хирургии суставов ФГБУ «ННИИТО им. Я.Л. Цивьяна» Минздрава России.
Расчет экономической эффективности выполнен на основе информационных данных за период с января 2010 года по ноябрь 2013 года контрольной и группы исследования. Полученные результаты статистически обработаны.
Полученные результаты. Все 56 пациентов были осмотрены, и результаты их лечения были оценены через 1 год после операции. Достоверной разницы в результатах лечения при сравнении в обеих группах не получено (табл. 1). В обеих группах были достигнуты все цели, поставленные во время предоперационного планирования. Тип использованных конструкций не влиял на сроки консолидации костей, которая наступила в планируемые сроки в обеих группах больных в зависимости от нозологической формы.
Оценка степени выраженности болевого синдрома по шкале VAS у пациентов обеих групп показала его трехкратное уменьшение относительно исходных величин, но достоверной разницы в результатах не отмечено, то есть результаты по VAS были приблизительно одинаковыми в обеих группах и свидетельствовали об эффективном купировании болевого синдрома у пациентов обеих групп (табл. 2).
Индекс по шкале AOFAS у пациентов в обеих группах спустя 12 месяцев после оперативного лечения более чем в два раза превышал исходную величину, составив 80,2±5,5 балла (p<0,01), что не отличалось достоверно от средней величины, полученной в группе сравнения после проведенного лечения (77,7±6,4 балла; p<0,01) (табл. 1). Таким образом, в итоге можно сделать вывод, что результаты использования биодеградируемых конструкций с клинической и функциональной точки зрения не имеют недостатков и не приводят к ухудшению результатов лечения пациентов.
Таблица 1
Клинические и функциональные результаты лечения пациентов в группах исследования
|
Группа пациентов |
Сроки наблюдения |
Оценка по шкале AOFAS, баллы |
Оценка по шкале VAS, баллы |
Результаты хирургического лечения пациентов с патологией стопы |
||
|
Основная группа (n=28) |
До операции |
34,0±5,2 |
78,5±7,1 |
хороший |
удовлетв. |
неудовлетв. |
|
Спустя 12 месяцев после операции |
80,2±5,5 * |
29,3±5,8 */** |
21(75%) |
5(17,9%) */** |
2(7,1%) |
|
|
Группа сравнения (n=28) |
До операции |
43,7±2,6 |
76,7±6,9 |
20(71,4%) |
5(17,9%) |
3(10,7%) |
|
Спустя 12 месяцев после операции |
77,7±6,4 * |
27,3±4,5 * |
||||
Примечание:* - p<0,01 по сравнению с величинами до хирургического лечения; ** - p<0,01 по сравнению с величинами, полученными в группе сравнения.
Однако если результаты клинической и функциональной оценки хирургического лечения были удовлетворительными в обеих группах, то отмечены выраженные различия в клинико-экономической оценке лечебного процесса. В группе сравнения количество операций и анестезий превышало таковое на 100% в основной группе. Также в группе сравнения время, проведенное пациентами в анестезиолого-реанимационном отделении, превышало на 44% таковое в основной группе.
Аналогично вышесказанному показатели среднего койко-дня и средних сроков реабилитации в группе сравнения были выше таковых в основной группе на 64% и 25% соответственно (табл. 2).
При этом по итоговым расчетам затратность применения биостойких конструкций, определенная на основе представленных данных в 1,35 выше по сравнению с хирургическим вмешательством, когда применялись биодеградируемые конструкции, исходя из представленных данных.
Таблица 2
Показатели лечебного процесса в группах сравнения
|
Группа пациентов |
Количество операций |
Количество анестезий |
Среднее время в АРО |
Средний койко-день |
Средние сроки реабилитации |
|
Основная группа (n=29) |
28* |
28 |
58±16 мин |
5,7±1 */** |
84±12 |
|
Группа сравнения (n=29) |
56 * |
56* |
84±15 мин |
9,4±1,8 |
105±16 |
|
Δ (осн./контр.) |
28 (100%) |
28 (100%) |
26±15 мин (44%) |
3,7±0,9 (64%) |
21±15 (25%) |
Примечание:* - p<0,01 по сравнению с величинами до хирургического лечения; ** - p<0,01 по сравнению с величинами, полученными в группе сравнения.
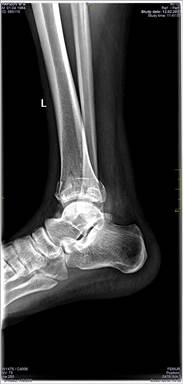
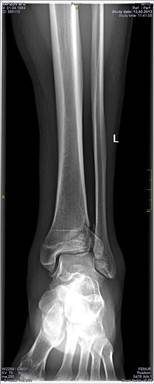
В качестве примера приводится клиническое наблюдение в виде исходных и контрольных (через год) рентгенограмм пациента А. (рис. 1-2).
 А
А
 Б
Б
Рис. 1. Рентгенограмма правого голеностопного сустава пациента А., 25 лет, И\б 702.13. в боковой проекции (А.), в прямой проекции (Б.): перелом пилона большеберцовой кости с выраженным смещением фрагментов в день получения повреждения
 А
А
 Б
Б
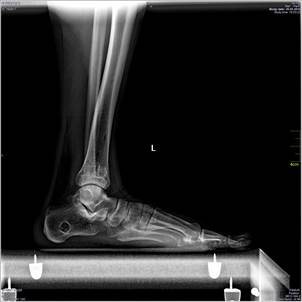
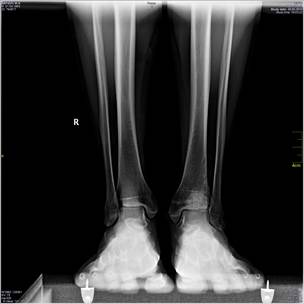
Рис. 2. Рентгенограмма правого голеностопного сустава пациента А., 25 лет, И\б 702.13., в боковой проекции (А), в прямой проекции (Б): консолидированный в удовлетворительном положении перелом пилона большеберцовой кости в условиях фиксации биодеградируемыми пинами через 1 год после повреждения и операции открытой репозиции, внутренней фиксации фрагментов пилона большеберцовой кости, костной аутопластики. Хороший результат лечения
Обсуждение. Необходимость точной репозиции фрагментов костей и стабильной их внутренней фиксации является непреложным законом травматологии и ортопедии. Двадцатый век вызвал к жизни бесчисленное количество металлоконструкций для скрепления костей с целью остеосинтеза и создания условий для их сращения в правильном положении. Цель – стабильная фиксация – была достигнута, но постепенно стали звучать голоса специалистов и ученых, что не все абсолютно благополучно с металлоконструкциями для остеосинтеза [5]. Теперь ясно, что металлоконструкции необходимо удалять, так как они вызывают остеопению, металлоз в результате коррозии металла, проминирование и раздражение окружающих тканей. Металлоконструкции не пропускают рентгеновские лучи, что создает сложности для оценки консолидации, положения фрагментов при контроле правильности остеосинтеза [4]. Казалось бы, проблема должна была разрешиться с появлением биодеградируемых конструкций для остеосинтеза в середине XX века. Однако они также оказались несвободными от серьезных недостатков, а именно – в первую очередь: высокая стоимость, низкая прочность, тканевые реакции, включая остеолиз вокруг импланта и формирование свищей. Есть данные о развитии синовита при интраартикулярной имплантации, правда, это является противоречивой информацией [5; 6]. Бостманом описан периимплантационный остеолиз, развивающийся у половины пациентов и начинающийся через 3 месяца после операции, правда, сам Бостман отмечал, что остеолиз не вызывал у пациентов проблем [1]. Конечно, по мере совершенствования производства биодеградируемых имплантов перечисленные недостатки исправлялись и все больше травматологов-ортопедов склонялись к их использованию. По мере улучшения материалов и техники появились и другие показания к применению этих имплантов в ортопедии и травматологии: для стимулирования остеогенеза при восстановлении дефектов костей, создания депо антибиотиков и факторов роста, формирования антиадгезивных мембран в хирургии сухожилий – сгибателей кисти, а также как матрица для тканевого инжиниринга хрящевой, костной, соединительной тканей [2; 4; 6]. Таким образом, к нашему времени ни у кого нет сомнения в полезности данного научно-практического направления, а данное исследование приводит к выводу, что, действительно, высокая стоимость конструкций нивелируется отказом от второй операции и связанных с ней расходов, потерь и риска для пациента.
Заключение. Таким образом, анализ результатов лечения 56 пациентов показал, что, несмотря на равноценность результатов оперативного лечения, проведенного всем пациентам, хирургические вмешательства с применением биодеградируемых конструкций сопровождались значительно меньшей травматичностью и существенным экономическим эффектом (более эффективная работа койки за счет отказа от повторной операции по удалению металлоконструкции и, соответственно, отсутствие затрат по пребыванию пациента в стационаре и отделении анестезиологии-реаниматологии).
Библиографическая ссылка
Пахомов И.А., Кузнецов В.В., Гуди С.М. ПРИМЕНЕНИЕ БИОДЕГРАДИРУЕМЫХ КОНСТРУКЦИЙ В ХИРУРГИЧЕСКОЙ ПОДИАТРИЧЕСКОЙ КЛИНИКЕ С ТОЧКИ ЗРЕНИЯ КЛИНИКО-ЭКОНОМИЧЕСКОГО АНАЛИЗА // Современные проблемы науки и образования. 2018. № 6. ;URL: https://science-education.ru/ru/article/view?id=28316 (дата обращения: 24.01.2026).



