Стресс-реакция – важнейший универсальный защитно-приспособительный комплекс биохимических и физиологических процессов, направленный на мобилизацию сил организма [1]. Известно, что при острой иммобилизации во внутренних органах нарушается микроциркуляция и возникает ишемия [2; 3]. Гипоксия почечной паренхимы является ведущим механизмом ее повреждения и одним из самых сложно корректируемых звеньев патологических процессов [3; 4]. В ответ на активацию свободнорадикальных процессов и изменение соотношения компонентов прооксидантно-антиоксидантной системы развивается оксидантный стресс [3-5]. Последний способствует активации нитрозергической системы и гиперпродукции монооксида азота [2; 6]. Именно интенсификация перекисного окисления липидов, цитотоксические и проапоптические эффекты монооксида азота являются главными факторами, повреждающими структуры нефрона при стрессовом воздействии, что может привести к развитию нефропатий [4-7]. Ввиду того что почки являются важнейшими компонентами системы адаптации к действиям различных факторов, целесообразным является изучение состояния различных функциональных систем почечной ткани при острой иммобилизации для оценки адаптивных возможностей организма. На современном этапе развития медицинской науки клеточная терапия рассматривается как альтернативный метод лечения различных патологических состояний [8; 9]. При этом наиболее перспективными считаются костномозговые мезенхимальные стволовые клетки (МСК) [10]. Однако биохимические механизмы подавления мезенхимальными стволовыми клетками оксислительного стресса за счет изменения активности компонентов антиоксидантной защиты при экстремальном воздействии физических факторов до конца не выяснены.
Цель исследования: изучить влияние аллогенных мезенхимальных стволовых клеток (МСК) на динамику содержания малонового диальдегида (МДА), как маркера перекисного окисления липидов, компонентов антиоксидантной системы (супероксиддисмутазы, каталазы и восстановленного глутатиона) на фоне 24-часового острого иммобилизационного стресса.
Материал и методы исследования. Эксперимент выполнен с использованием 208 самцов беспородных белых крыс массой 225 ± 25 граммов. Костномозговые мезенхимальные стволовые клетки извлекали из полостей бедренных и большеберцовых костей половозрелых лабораторных крыс путем промывания их питательной средой «ИГЛА МЕМ» («Биолот», Россия). Полученные клетки культивировали 14 суток в питательной среде «ИГЛА-МЕМ» («Биолот», Россия), обогащенной L-глютамином, с добавлением 10% жидкой эмбриональной телячьей сыворотки и двух антибиотиков при 37 °С в условиях СО2-инкубатора HF15UV (Heal Force, Китай) со сменой среды каждые 5 дней. Жизнеспособность клеток оценивали тестом с трипановым синим. Клеточную культуру фенотипировали непрямым иммунофлюоресцентным методом с помощью специфических маркеров к МСК: моноклональные антитела к СД 73, СД 105, СД 44, СД 90 и СД 54. В качестве модели острого стресса применяли однократную иммобилизацию животных в течение 24 часов в индивидуальных фиксирующих камерах, исключающих возможность каких-либо активных движений. Животные были разделены на группы: № 1 – интактные крысы; № 2 – крысы, подвергнувшиеся действию острого иммобилизационного стресса (контроль), № 3 – крысы, получавшие МСК после иммобилизации (экспериментальная группа). Через 1 час после действия стрессора животным группы № 2 внутривенно вводили по 1 мл физиологического раствора, группы № 3 – по 5 • 106 МСК. Животных выводили из эксперимента на 1, 3, 7, 14, 21 и 30-е сутки наблюдения путем цервикальной дислокации спинного мозга в шейном отделе под легким эфирным наркозом. Производили забор крови для получения сыворотки. Выделяли почки, гомогенизировали их в сахарозной среде выделения. Активность перекисного окисления липидов в сыворотке крови и в гомогенатах почечной ткани оценивали по уровню малонового диальдегида, который определяли спектрофотометрически с помощью спектрофотометра СФ-46 (длина волны 532 нм) после реакции с 2-тиобарбитуровой кислотой в кислой среде. Состояние неферментного звена антиоксидантной системы оценивали по содержанию восстановленного глутатиона в сыворотке крови и в почечной ткани, уровни которого определяли реакцией Эллмана с последующей спектрофотометрией при длине волны 400 нм. О состоянии ферментативного звена антиоксидантной защиты судили по изменению активности каталазы и супероксиддисмутазы (СОД), которые определяли спектрофотометрически (λ=410 нм и λ=347 нм) с помощью реакции с солями молибдена и реакции аутоокисления адреналина. Статистическую обработку данных проводили пакетом программ Statistica 10.0. Для сравнения результатов между исследуемыми группами использовали критерий Манна-Уитни. Результаты расценивались как достоверные при р<0,05. Данные представлялись в виде медианы и интерквартильного размаха.
Результаты исследования и их обсуждение. Опытным путем доказано, что показатели сыворотки крови и почечной ткани, характеризующие степень окислительного стресса, зависят от срока наблюдения в послестрессовом периоде и значительно изменяются под действием мезенхимальных стволовых клеток.
При анализе показателей малонового диальдегида было установлено его резкое повышение как в сыворотке крови, так и в почечной ткани животных, подвергнувшихся иммобилизационному стрессу (таблица).
Содержание малонового диальдегида в сыворотке крови и в почечной ткани после 24-часового иммобилизационного стресса и введения МСК
|
Группа животных |
Срок наблюдения |
МДА в сыворотке крови (мкмоль/л) |
МДА в почечной ткани (нмоль/г ткани) |
|
Интактная (n=28) |
- |
2,45 (1,96; 2,71) |
14,85 (13,86; 15,55) |
|
Контрольная (n=90) |
1-е сутки |
6,79 ** (6,41; 7,06) |
33,578 ** (32,622; 34,631) |
|
3-и сутки |
7,42 ** (6,85; 7,83) |
46,95 ** (45,73; 48,11) |
|
|
7-е сутки |
6,12 ** (5,72; 6,41) |
37,51 ** (35,58; 38,88) |
|
|
14-е сутки |
4,19 ** (3,67; 4,56) |
26,319 ** (25,154; 27,215) |
|
|
21-е сутки |
2,91 * (2,54; 3,15) |
17,284 ** (15,476; 18,572) |
|
|
30-е сутки |
2,45 (2,19; 2,64) |
15,66 (14,05; 16,81) |
|
|
Экспериментальная (n=90) |
1-е сутки |
6,85 ** (6,52; 7,11) |
32,831 ** (30,823; 33,919) |
|
3-и сутки |
7,24 ** (6,84; 7,59) |
46,067 ** (44,462; 47,152) |
|
|
7-е сутки |
4,81 **, ## (4,61; 4,96) |
31,085 **, ## (29,282; 32,441) |
|
|
14-е сутки |
2,91 *, ## (2,53; 3,18) |
19,19 **, ## (18,19; 19,92) |
|
|
21-е сутки |
2,5 # (2,2; 2,71) |
15,664 # (14,237; 16,681) |
|
|
30-е сутки |
2,39 (2,22; 2,51) |
14,69 # (13,68; 15,41) |
Примечание: n – количество наблюдений в группе;
* - p<0,05; ** - p<0,001 – относительно интактных значений;
# - p<0,05; ## - p<0,001 – относительно контрольных значений.
Так, уровень малонового диальдегида в сыворотке крови в 1-е и 3-и сутки постиммобилизационного периода возрос в контрольной группе на 177,14% и 202,8% соответственно (р<0,001), в экспериментальной группе – на 179,6% и 195,5% соответственно (р<0,001) по сравнению с интактными значениями. В группе № 2 на 7-е сутки показатели МДА достоверно превышали интактные цифры на 149,8% (р<0,001), на 14-е – на 71,02% (р<0,001), на 21-е – на 18,7% (р<0,001). У крыс, получавших в качестве терапии МСК, концентрация малонового диальдегида в сыворотке крови на 7, 14, 21 и 30-е сутки наблюдения была ниже контрольных показателей соответственно на 21,4% (р<0,001), 30,5% (р<0,001), 14,09% (р<0,001) и 2,45% (р<0,05).
В гомогенатах почечной ткани также отмечалось достоверное повышение уровня МДА относительно начальных значений на 1-е и 3-и сутки наблюдения в контрольной группе на 126,1% (р<0,001) и 216,16% соответственно (р<0,001), в экспериментальной группе – на 121,08% (р<0,001) и 210,2% (р<0,001) соответственно. В последующие сутки наблюдения у крыс группы контроля наблюдалось постепенное снижение цифр исследуемого показателя, однако на 7-е сутки они были достоверно выше интактных значений на 152,6% (р<0,001), на 14-е – на 77,23% (р<0,001), на 21-е – на 16,4% (р<0,001). К концу периода наблюдения содержание малонового диальдегида статистически не отличалось от показателей интактных животных. У крыс, получавших клеточную терапию, концентрация МДА на 7, 14, 21 и 30-е сутки достоверно снизилась по сравнению с показателями группы контроля на 17,13% (р<0,001), 27,08% (р<0,001), 9,4% и 6,2% (р<0,05) соответственно. Полученные результаты могут быть обусловлены активизацией свободнорадикальных процессов в ответ на гипоксию при иммобилизационном стрессе [2; 3; 5].
При изучении динамики восстановленного глутатиона в сыворотке крови крыс были получены следующие результаты: на 1-е и 3-и сутки наблюдения его значения снизились относительно интактных цифр как в контрольной (на 29,3% и 54,5%, р<0,001), так и в опытной (на 30,4% и 46,7%, р<0,001) группах. В группе № 2 данный показатель был достоверно меньше интактных значений на 7-е сутки на 43,4%, на 14-е сутки – на 26,1%, на 21-е сутки – на 11,9% (р<0,001). В группе № 3 отмечалось статистически значимое повышение уровня восстановленного глутатиона относительно контроля, однако его значения были достоверно ниже интактных цифр (р<0,001).
Что касается показателей восстановленного глутатиона в почечной ткани, то на 1-е и 3-и сутки исследования его уровень значительно снизился относительно интактных значений как во второй (на 35% и 53% соответственно, р<0,001), так и в третьей (на 35% и 51,3% соответственно, р<0,001) группах. В контрольной группе цифры восстановленного глутатиона были ниже интактных значений на 7, 14, 21 и 30-е сутки наблюдения соответственно на 46,4% (р<0,001), 37,6% (р<0,001), 20% (р<0,001) и 9,38% (р<0,05). У крыс, леченных МСК, отмечалось статистически значимое повышение уровня восстановленного глутатиона относительно контроля, однако его значения были достоверно ниже интактных цифр. Так, на 7-е сутки наблюдения исследуемый показатель у экспериментальных животных был достоверно ниже интактных значений на 35% (р<0,001), но был выше цифр группы контроля на 19,3% (р<0,05). На 14-е и 21-е сутки наблюдения его уровень у крыс опытной группы снизился на 22% (р<0,001) и 8,14% (р<0,05) соответственно по сравнению с показателями интактной группы, но превышал контрольные значения на 24,9% (р<0,01) и 15,2% (р<0,01). К концу исследования не было статистической разницы между показателями восстановленного глутатиона в почечной ткани крыс всех исследуемых групп. Полученные результаты могут указывать на интенсивное расходование данного вещества в реакциях конъюгации с продуктами свободнорадикальных процессов, резко активизирующихся при стрессе. Динамика уровня восстановленного глутатиона в сыворотке крови и в почечной ткани после 24-часовой иммобилизации и введения МСК показана на рисунке 1.
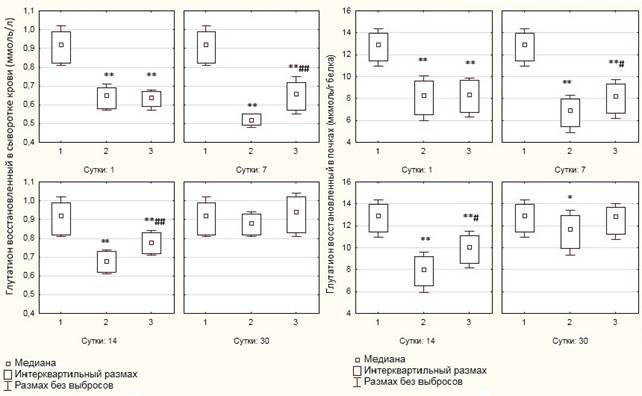
Рис. 1. Динамика уровня восстановленного глутатиона в сыворотке крови и в почечной ткани после 24-часовой иммобилизации и введения МСК
Примечание:
* - p<0,05; ** - p<0,001 – относительно интактных значений;
# - p<0,05; ## - p<0,001 – относительно контрольных значений.
Показатели ферментативного звена антиоксидантной системы также существенно снизились как в сыворотке крови, так и в почечной ткани в ответ на 24-часовой иммобилизационный стресс. В сыворотке крови уровни активности каталазы и супероксиддисмутазы у животных контрольной группы снизились по сравнению с интактными значениями в 1-е сутки наблюдения на 21,4% и 28% соответственно (р<0,001), на 3-и сутки – на 36,4% и 55% соответственно (р<0,001), на 7-е сутки – на 33,5% и 45,6% соответственно (р<0,001), на 14-е сутки – на 26,7% и 33,3% соответственно (р<0,001), на 21-е сутки – 16% и 22,5% соответственно (р<0,001). У крыс, леченных МСК, показатели активности каталазы и СОД достоверно превышали контрольные значения на 7, 14, 21 и 30-е сутки мониторинга соответственно на 9,8% (р<0,001) и 20% (р<0,001), 25,4% (р<0,001) и 21,7% (р<0,001), 16,9% (р<0,001) и 20,5% (р<0,001), 8,3% (р<0,001) и 13,6% (р<0,05). Изменения активности супероксиддисмутазы и каталазы в сыворотке крови после 24-часового иммобилизационного стресса и введения МСК показаны на рисунке 2.
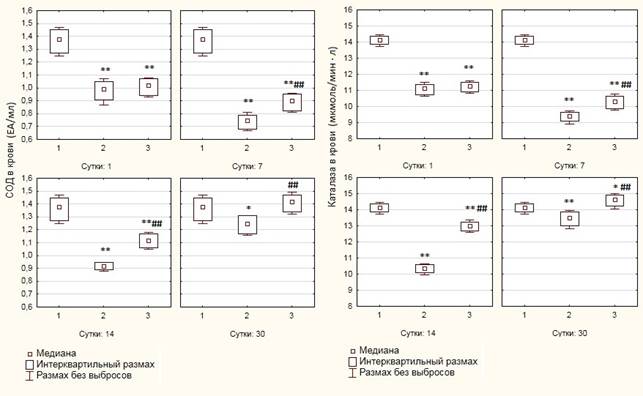
Рис. 2. Изменения активности супероксиддисмутазы и каталазы в сыворотке крови после 24-часового иммобилизационного стресса и введения МСК
Примечание:
* - p<0,05; ** - p<0,001 – относительно интактных значений;
# - p<0,05; ## - p<0,001 – относительно контрольных значений.
Исследованием установлено, что уровни активности СОД и каталазы в гомогенатах почечной ткани после 24-часовой иммобилизации в группе контроля в 1-е сутки снизились по сравнению с интактными значениями на 27% (р<0,001) и 46,2% (р<0,001) соответственно, на 3-и сутки – на 49,7% (р<0,001) и 58,3% (р<0,001) соответственно, на 7-е сутки – на 41,6% (р<0,001) и 43,9% (р<0,001) соответственно, на 14-е сутки – на 18,3% (р<0,001) и 32,6% (р<0,001) соответственно, на 21-е сутки – на 9,8% (р<0,01) и 14,8% (р<0,001) соответственно. К 30-м суткам наблюдения показатели активности каталазы и супероксиддисмутазы в контрольной группе статистически не отличались от интактных значений. У животных, получавших клеточную терапию, показатели активности каталазы достоверно превышали значения группы контроля на 7, 14, 21 и 30-е сутки соответственно на 15,6% (р<0,001), 14 26,3% (р<0,001), 22,8% (р<0,001) и 6,64% (р<0,001). Значения активности СОД у животных опытной группы на 7, 14, 21 и 30-е сутки наблюдения возросли относительно контрольных на 29,9% (р<0,001), 6,4% (р<0,05), 7,3% (р<0,001) и 8,2% (р<0,01) соответственно. Изменения активности супероксиддисмутазы и каталазы в почечной ткани после 24-часового иммобилизационного стресса и введения МСК показаны на рисунке 3.
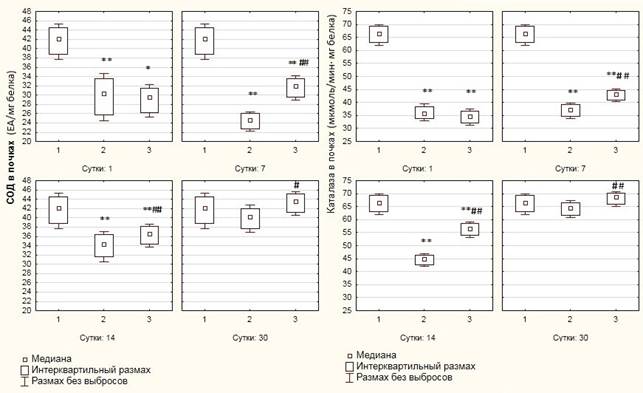
Рис. 3. Изменения активности супероксиддисмутазы и каталазы в почечной ткани после 24-часового иммобилизационного стресса и введения МСК
Примечание:
* - p<0,05; ** - p<0,001 – относительно интактной группы;
# - p<0,05; ## - p<0,001 – относительно группы контроля.
Полученные результаты свидетельствуют о значительном угнетении системы антиоксидантной защиты сыворотки крови и паренхимы почек в условиях острого стресса, что подтверждается снижением активности каталазы и СОД. Более быстрые темпы восстановления исследуемых показателей могут указывать на подавление мезенхимальными стволовыми клетками процессов перекисного окисления липидов и повышение антиоксидантных свойств клеток [8-10].
Выводы. Острая иммобилизация приводит к интенсификации перекисного окисления липидов, угнетению активности как ферментативных, так и неферментных компонентов антиоксидантной системы, о чем свидетельствуют повышение концентрации малонового диальдегида, снижение уровня восстановленного глутатиона, угнетение активности супероксиддисмутазы и каталазы в сыворотке крови и в ткани почек. Применение аллогенных МСК в качестве средства коррекции при острой иммобилизации способствует более быстрому восстановлению показателей антиоксидантной системы, а, следовательно, функционального состояния почек опытных крыс по сравнению с контролем. Полученные данные указывают на целесообразность дальнейших экспериментальных исследований применения клеточной терапии с целью активации процессов регенерации органов и тканей при состояниях, в патогенезе которых лежат явления гипоксии.
Библиографическая ссылка
Демьяненко Е.В. ВЛИЯНИЕ МЕЗЕНХИМАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК НА ПОКАЗАТЕЛИ ПЕРЕКИСНОГО ОКИСЛЕНИЯ ЛИПИДОВ И АНТИОКСИДАНТНОЙ ЗАЩИТЫ СЫВОРОТКИ КРОВИ И ПОЧЕЧНОЙ ТКАНИ КРЫС ПРИ ОСТРОМ ИММОБИЛИЗАЦИОННОМ СТРЕССЕ // Современные проблемы науки и образования. – 2018. – № 6. ;URL: https://science-education.ru/ru/article/view?id=28307 (дата обращения: 26.04.2024).



