Актуальность. Актуальность работы обусловлена тем, что успех восстановления повреждений кости челюстей, образующихся вследствие роста одонтогенных кист, доброкачественных опухолей, травм, остеомиелитических процессов и т.д., во многом определяется процессами репаративной регенерации костной ткани. Исследования, связанные с изучением этиологии и патогенеза и комплексным лечением пациентов с дефектами и деформациями, в настоящее время среди всех патологий костной системы челюстно-лицевой области в Российской Федерации занимают первое место. В связи с этим многообразие существующих хирургических методов говорит о сложности устранения такой патологии. В силу актуальности проблемы возникает острая необходимость в систематизации и анализе накопленного клинического опыта и поиска рациональных методов комплексного лечения таких больных с использованием инновационных технологий. Полное и быстрое восстановление костных тканей является проблемным, поскольку большие дефекты не могут восстанавливаться спонтанно, несмотря на попытки усиления регенерации кости препаратами, повышающими остеогенез. Наличие дефектов в области верхней и нижней челюсти препятствует проведению дентальной имплантации в течение длительного времени, которая порой и вообще становится невозможной, так как отсутствие костной ткани не позволяет ее осуществить [1-3]. В настоящее время проводится интенсивный поиск новых материалов, которые можно было бы применить в замещении костных дефектов. Разрабатываются и апробируются имплантаты из различных сплавов металлов, пластмасс, керамики, углерода, имеющих монолитную основу, что снижает их остеоинтеграционные свойства – это их главный недостаток. Мы предлагаем применение имплантационных материалов, которые значительно отличаются от моноблочных изделий и даже пористо-углеродных материалов и пористого титана. На наш взгляд, заполнение костных дефектов имплантационными биосовместимыми материалами, имеющими структуру гранецентрированной кубической решетки кристалла, соответствующими размерам образовавшейся полости и повторяющими анатомическую форму челюсти с внедренным опорным элементом под коронку зуба, является актуальным направлением в челюстно-лицевой хирургии [4; 5].
Цель: изучить в эксперименте регенерацию костной ткани в условиях имплантационных материалов, состоящих из гранецентрированных кубических решеток кристалла, в различные сроки. Сравнить процессы репаративной регенерации костной ткани в титановых решетках, а также при использовании углекона-М и пористого титана.
Материал и методы исследования. Создание усовершенствованной конструкции титанового имплантационного материала, способного обеспечить доставку клеточных элементов, образующих кость, в сегменты кубических решеток, было одной из важных задач нашего исследования. По нашему мнению, это будет достигнуто за счет того, что имплантационный материал выполнен в виде гранецентрированных кубических решеток кристалла, образованных тонкими перемычками (0,2 мм), пронизанными микроканальцами, которые, соединяясь, образуют конструкцию правильной геометрической формы (рис. 1). Жестко соединенные между собой, они образуют в начале модель, в последующем титановый имплантационный материал для замещения костного дефекта.
В работе использованы образцы титановых имплантационных материалов, образованных гранецентрированной кубической решеткой кристалла, имеющих размеры кубических решеток 250, 550 и 850 мкм, изготовленных методом прототипирования на основе технологии визуализации трехмерных систем компьютерного моделирования.

Рис. 1. Имплантационный материал, состоящий из гранецентрированных кубических решеток кристалла (1). Ув. х100
Изделия изготовлены на кафедре конструирования машин и сопротивлений материалов (зав. кафедрой, д.т.н., профессор А.М. Ханов) и на кафедре информационных технологий и автоматических систем (зав. кафедрой, д.т.н., профессор Р.А. Файзрахманов) Пермского государственного технического университета. В эксперименте использовали образцы, состоящие из гранецентрированных кубических решеток кристалла с гладкими краями, максимальным диаметром 5 мм, минимальным 2 мм, толщиной 1,5 мм; поверхность их была подвергнута пескоструйной обработке. Полученные имплантационные изделия из титана с кубической решеткой вводили в искусственно созданный костный дефект нижней челюсти беспородных крыс и морских свинок, используя базу ЦНИЛа ПГМУ. Работы выполнены в соответствии с Приказом Министерства здравоохранения СССР от 12.08.1977 г. № 755 и «Европейской конвенцией о защите позвоночных животных, используемых для экспериментов или в иных научных целях» от 18.03.1986 г. Текст изменен в соответствии с положениями протокола (ETS № 170), после его вступления в силу 2 декабря 2005 года. Исследования включали 3 этапа: 2 недели, 4 и 9 месяцев.
Внедрение имплантатов осуществляли следующим способом: животное вводили в наркотическое состояние с помощью Северана, местно - раствор лидокаина 0,5 от 1,0 до 1,5 мл. После антисептической обработки рассекали кожу, подкожную клетчатку длиной до 1,5 см в поднижнечелюстной области, а также надкостницу и отслаивали ее от кости челюсти. Осторожно с помощью бора формировали дефект в кости челюсти, соответствующий размерам имплантата. Имплантат помещали в костный дефект, фиксировали с помощью тонкой танталовой проволоки по типу костного шва. Мягкими тканями закрывали имплантат и ушивали Проленом 0,3 мм. Линию швов покрывали марлевой повязкой с мазью «Левомеколь». Животным вводили цептриаксон – 100 млг один раз в сутки в течение 7 суток. (Удостоверение на рационализаторское предложение № 2586, 17.05.2012 г.) Подопытных животных выводили из эксперимента в соответствии со сроками (2 недели, 4 мес. и 9 мес.), после чего осуществляли забор мягких тканей и костную структуру вместе с имплантатом. В первом случае выделен 21 макропрепарат, во втором - 43 макропрепарата, а в третьем – 18. Взятый материал погружали в «Трилон-В» на 3 месяца для проведения декальцинации костной ткани. После заливки материала в парафин-целлоидин изготавливали срезы. Окраска гематоксилин-эозином. Из 82 макропрепаратов нами приготовлено 109 микропрепаратов, которые подвергли морфологическому исследованию.
Результаты исследования и обсуждение. В 2-недельный срок выявлено, что произошло образование соединительной ткани, которая заполнила кубические решетки имплантационного материала в 250 мкм на 2/3 и 550 мкм полностью, переходила непосредственно в капсулу вокруг имплантата и была представлена грануляционной или незрелой фиброзной тканью (рис. 2), в которой частично отмечалась мононуклеарная инфильтрация различной плотности; в инфильтратах преобладали лимфоциты и макрофаги. В кубических решетках в 850 мкм обнаружена остаточная макрофагальная реакция.
Новообразованная костная ткань представлена незрелой, ретикулофиброзной тканью, которая врастала от края дефекта к центру, циркулярно, охватывая периферические перемычки кубических решеток. В глубине фиброзной ткани по периферии дефекта встречались небольшие очаги оссификата с признаками активного остеогенеза.
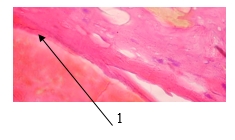
Рис. 2. Соединительнотканная капсула вокруг образца вокруг ячеек (1), срок имплантации - 12 дней. Капсула тонкая, без воспалительной реакции. Окраска гематоксилин-эозином.
Ув. х200
Через 2 недели после пластики дефекта нижней челюсти накостным углеродным имплантатом «Углекон-М» при морфологическом исследовании выявлено полнокровие сосудов, умеренная макрофагальная инфильтрация вокруг имплантата. В цитоплазме макрофагов – наличие инородных частиц углерода. Отмечается также пролиферация фибробластов. При исследовании имплантата из пористого титана в 24 недели выявлено: вокруг пористого титанового образца интимно прилегает грубоволокнистая костная ткань, которая представлена множеством костных балок и костным мозгом.
Микроскопический анализ тканей, полученных из имплантатов, состоящих из кубических решеток 250 мкм в сроки 4 мес., показал, что замещение их незрелым костно-фиброзным регенератом в основном наблюдается по периферии ячеек. Однако в центре имплантатов содержится незрелая фиброзная ткань. Иногда выявляются островки гиалинового хряща.
В кубических решетках 550 мкм в те же сроки обнаружены отростки пластинчатой костной ткани, окруженные соединительной тканью. В кубических решетках имплантационного материала, размером 850 мкм, сформировалась соединительная ткань, а на периферии - грубоволокнистая и пластинчатая костная ткань с прослойками соединительной ткани. Наблюдается большое количество сосудов без наличия тромбов. В целом в имплантационных материалах с гранецентрированных кубических решеток кристалла, размером 850 мкм, выявлено, что относительный объем костной части регенерата, заполняющего ячейки, больше, чем в вышеизложенных случаях. В искусственно созданном дефекте кости нижней челюсти имеется некоторое увеличение объема периостального костного регенерата по краям имплантатов.
Таким образом, через 4 месяца экспериментального исследования можно заметить, что с увеличением размеров гранецентрированных кубических решеток увеличивается иинтеграция имплантата с костью. Остеоинтеграция образцов обусловлена также непосредственным контактом минерализованных костных структур с поверхностью металла снаружи и в перемычках имплантата. Через 4 месяца после пластики дефекта нижней челюсти накостным углеродным имплантатом «Углекон-М» при гистологическом исследовании выявлено обилие частиц черного цвета, окруженных соединительными структурами, содержащих большое количество плотно расположенных коллагеновых волокон. При исследовании имплантата из пористого титана в 24 недели выявлено: вокруг пористого титанового образца интимно прилегает грубоволокнистая костная ткань, которая представлена множеством костных балок и костным мозгом.
Через 9 месяцев в имплантационных материалах с гранецентрированной кубической решеткой кристалла с размером 250 мкм выявляется незрелая ретикулофиброзная ткань, которая уже распространяется от края к центру ячеек, циркулярно, охватывая одновременно края костного дефекта. Встречались небольшие оссификаты в глубине фиброзной ткани. По краям дефекта и интерстициального регенерата наблюдались признаки активного остеогенеза.
В имплантационных материалах с гранецентрированной кубической решеткой кристалла с размером 550 мкм, и особенно 850 мкм, сформировались разнонаправленные костные пластинки, окруженные по границе с металлом соединительной тканью. В центрально расположенных ячейках пластинчатая костная ткань утолщена с наличием костных трабекул с образованием костномозговых полостей с расположенными здесь сосудами и развивающимися клетками крови. Образуются подобия остеонов (рис. 3).
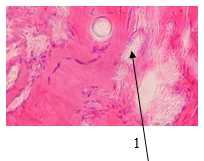
Рис. 3. Нижняя челюсть крысы, срок 9 мес. после имплантации. Имплантат с ячейками 850 мкм с костными пластинками (1) и широкими пространствами между ними с кровеносными сосудами и клетками крови. Окраска гематоксилин-эозином. Ув. 200
Соединительнотканная капсула вокруг имплантационного материала с гранецентрированной кубической решеткой кристалла была представлена зрелой фиброзной тканью с незначительно выраженной мононуклеарной воспалительной инфильтрацией и увеличенным количеством лимфоцитов и макрофагов (рис. 4). С одной стороны к капсуле (1) примыкают волокна мышечной ткани (2), с другой – зрелые костные пластинки (3).
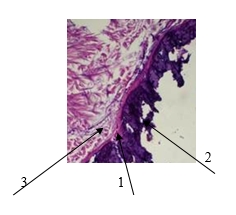
Рис. 4. Плотная соединительнотканная капсула по краю имплантата, срок имплантации - 9 мес. Мышечная ткань (1), соединительнотканная капсула (2), зрелые костные пластинки (3). Окраска гематоксилин-эозином. Ув. х200
Анализ образцов, полученных через 9 месяцев, показал, что интеграция костных структур в имплантационных материалах с гранецентрированной кубической решеткой кристалла увеличилась незначительно. Однако костный компонент в решетках размером 850 мк более выражен, чем в других случаях, что обусловлено образованием зрелых костных пластинок, обеспечивающих жесткость и стабильность конструкции.
Через 9 мес. гистологическое исследование кости имплантационного ложа с имплантатом из «Углекона-М» показало: утолщение надкостницы; видны широкие прослойки соединительной ткани с прилежащими к ним единичными костными трабекулами. При исследовании имплантата из пористого титана в 36 недель выявлена в основном грубоволокнистая костная ткань, которая лишь окружает конструкцию и частично замещается пластинчатой костной тканью. В участках грубоволокнистой костной ткани, интимно прилегающей к пористому имплантату, обнаружены процессы минерализации и поверхностных очагов прорастания в поры имплантата в виде «бахромы».
Таким образом, исследования показали, что остеоинтеграция при использовании имплантационных материалов с гранецентрированной кубической решеткой кристалла протекает активнее в решетках разных размеров в ранние и поздние сроки и завершается образованием полноценной пластинчатой кости, обеспечивающей высокую прочность, по отношению к «Углекону-М» и пористому титану, при использовании которых остеосинтез происходит замедленно.
Выводы
1. В 2-недельный срок образовавшаяся соединительная ткань заполняла кубические решетки в 250 и 550 мкм, переходила непосредственно в капсулу вокруг имплантата и была представлена грануляционной или незрелой фиброзной тканью, однако в решетках в 850 мкм обнаружена ретикуло-фиброзная ткань с признаками активного остеогенеза.
2. С увеличением срока эксперимента с 4 до 9 месяцев увеличивается интеграция костных структур во всех трех видах имплантатов, особенно в имплантатах с кубическими решетками в 850 мкм и более.
3. Сравнительный анализ данных, полученных через 9 месяцев, показал, что имеются еще слабовыраженные признаки костно-фиброзной интеграции в имплантационных материалах с решетками 250 и 550 мкм. Минерализованные костные структуры имеются лишь в имплантационных материалах с кубической решеткой в 850 мкм, где процессы оссификации начинаются значительно раньше.
4. Процессы остеорегенерации различны и активнее протекают с использованием имплантационных материалов с решетками разных размеров в ранние и поздние сроки и завершаются образованием полноценной пластинчатой кости, обеспечивающей высокую прочность образованной конструкции по отношению к «Углекону-М», при котором остеосинтез происходит замедленно. В имплантатах из пористого титана в те же сроки выявлены широкие прослойки соединительной ткани и участки грубоволокнистой кости лишь интимно прилегающей к имплантату.
Библиографическая ссылка
Василюк В.П., Штраубе Г.И., Четвертных В.А. МОРФОЛОГИЯ КОСТНОЙ ТКАНИ В УСЛОВИЯХ ГРАНЕЦЕНТРИРОВАННЫХ КУБИЧЕСКИХ РЕШЕТОК КРИСТАЛЛА ТИТАНОВЫХ ИМПЛАНТАТОВ В ЭКСПЕРИМЕНТЕ // Современные проблемы науки и образования. – 2018. – № 4. ;URL: https://science-education.ru/ru/article/view?id=27764 (дата обращения: 26.04.2024).



