Анализ проведенных эпидемиологических исследований, проведенных в последнее время, в том числе и в Нижегородской области, свидетельствует о том, что одними из распространенных заболеваний слизистой оболочки ртa (СОР) и красной каймы губ (ККГ) являются заболевания, сопровождающиеся гипер- и дискератозом, а именно красный плоский лишай, лейкоплакия, различные формы хейлита. Как известно, эти состояния относятся к факультативным предракам, с частотой озлокачествления от 1,5 до 20-40%. В то время как абразивный преканцерозный хейлит Манганотти относят к облигатным формам предрака с высокой потенциальной злокачественностью (от 9 до 42%). С клинической и патоморфологической точки зрения к предраковым состояниям относят любые хронические заболевания, сопровождающиеся образованием в тканях очагов избыточной пролиферации клеток, на фоне которых может развиться рак. Это требует от врачей – стоматологов, в первую очередь, онкологической настороженности, диагностической точности, знания клинической картины заболеваний, организации онкологической помощи населению, стратегии и тактики ведения данной категории больных [1; 2].
В настоящее время существуют противоречивые взгляды на проблему диагностики и лечения предраковых заболеваний, о чем свидетельствует увеличивающееся количество онкобольных. Это связано с поздним обращением пациентов к специалисту, «смазанностью» клинической картины на начальных стадиях заболевания, неиспользованием дополнительных методов диагностики и неадекватной терапией [3]. Проведенные исследования показали, что только 42,8% врачей-стоматологов дифференцируют ранние проявления рака тканей и органов ротовой полости, 4,2% респондентов могут правильно провести первичные диагностические мероприятия по выявлению патологии данной локализации [4]. По данным Гилевой О.С. (2012), только в 46,1% случаев первичная диагностика КПЛ СОПР соответствовала первому и второму диагностическим уровням. Прямые затруднения в постановке диагноза при заболеваниях СОР были зафиксированы у 48,9% врачей-стоматологов, при этом корректный диагноз был сформулирован только в 5,0% направлений. Низкое качество диагностики отражало высокое количество недостаточно обследованных пациентов (74,6%), также в 9,8% случаев имела место гипердиагностика, когда доброкачественные изменения интерпретировались как «рак СОПР» [5].
Несмотря на кажущуюся простоту клинической визуализации предраковых изменений СОР и ККГ в связи с наружной локализацией, определение нозологической формы заболевания только на основе данных осмотра и пальпации нередко ведет к диагностическим ошибкам, так как различная степень ороговения или изъязвления патологических элементов делает их сложно дифференцируемыми. Особенно актуальной является ранняя диагностика злокачественной трансформации, поскольку ее клинические признаки появляются позднее реально возникшего процесса [6]. Поэтому необходимо проведение организационно-методической работы и повышения уровня знаний стоматологов о ранних клинических проявлениях предраковых заболеваний тканей и органов полости рта, широкое внедрение быстрых скрининговых методов диагностики заболеваний СОР и ККГ на первичном приеме.
В настоящее время известны такие методики, как стоматоскопия, фотостоматоскопия, люминесцентное исследование при воздействии ультрафиолетовых лучей (лучей Вуда), флюоресцентная диагностика [7]. В последние годы высокую чувствительность в обнаружении предикторных изменений и ранних форм рака слизистых оболочек полых органов показал метод аутофлюоресцентной диагностики (АФД), основанный на различиях в интенсивности и спектральном составе аутофлюоресцентного излучения нормальной и патологической ткани. Физический принцип способа основан на возбуждении собственной флюоресценции (аутофлюоресценции) слизистой оболочки посредством света из синей зоны оптического спектра (375-440 нм). С этой целью используют специальные источники света, такие как ксеноновая лампа или полупроводниковый лазер. Известно, что аутофлюоресценция здоровых тканей наблюдается в зеленой части спектра в диапазоне от 470 до 800 нм, разница в длине волны между светом возбуждения (синим) и эмитируемым светом позволяет выявить флюоресценцию [8; 9]. Согласно клиническим исследованиям последних лет в месте перерождения эпителия наблюдается резкое уменьшение интенсивности излучения на фоне окружающей здоровой ткани. Данный эффект получил название «темного пятна», так как эпителий предраковых и злокачественных образований излучает свечение меньшей интенсивности, чем эпителий нормальной слизистой оболочки. Разница между аутофлюоресценцией новообразований и нормального эпителия вызвана изменениями в физическом строении ткани, изменениями в объеме циркулирующей крови, содержания в ткани флюоресцирующих веществ [10].
В доступных литературных источниках имеется ряд публикаций, касающихся АФС-диагностики заболеваний СОР, при этом вопросы оценки эффективности лечения предикторных изменений СОР и ККГ с помощью данной методики недостаточно освещены.
В связи с этим целью настоящего исследования явилась оценка эффективности комплексной терапии предраковых заболеваний СОР при помощи аутофлюоресцентной диагностики.
Материал и методы. На базе кафедры пропедевтической стоматологии за 2015-2017 годы обследовано 300 пациентов с заболеваниями в возрасте 31-82 лет. Из них у 94 человек (31,3%) выявлены различные формы предраковой патологии СОР и ККГ: эрозивно-язвенная форма плоского лишая (ПЛ) – у 47 человек (50%), эрозивная форма лейкоплакии – у 20 больных (21,3%), веррукозная лейкоплакия – у 12 человек (12,8%); декубитальная язва – у 12 человек (12,8%), хейлит Манганотти – у 3 пациентов (3,1%).
Обследование больных включало традиционные методы: опрос, сбор анамнеза, визуальный осмотр, пальпацию регионарных лимфатических узлов, осмотр зубных рядов. Особое внимание уделялось исследованию ортопедических конструкций, острых краев зубов, коронок, зубных протезов. Для определения площади патологических очагов проводилось их фотодокументирование и измерение продольного (a) и поперечного размера (b) при помощи пародонтального зонда. Площадь одиночной язвы, эрозии вычислялась по формуле S=a×b, при наличии нескольких патологических элементов рассчитывалась суммарная площадь пораженной поверхности по формуле S= S1+S2+S3+n.
Для первичной диагностики заболеваний слизистой оболочки рта был использован комплект АФС-Д («Полироник»). Все пациенты были обследованы при обращении, на 7, 10, 14, 21-й день, 1 месяц и каждые 3-6-12 месяцев диспансерного наблюдения. По результатам онкоскрининга больные с длительностью заболевания более 1 месяца были направлены на цито- и гистологическое исследование, которое проводилось на базе поликлиники ГБУЗ «Нижегородский областной клинический онкологический диспансер».
Комплексное лечение больных с предраковыми заболеваниями СОР и ККГ на первом этапе включало устранение местных травмирующих факторов (острых краев зубов, снятие некачественных ортопедических конструкций, в первую очередь из разнородных металлов), профессиональную гигиену, санацию полости рта, временное протезирование с использованием безакриловой пластмассы. Медикаментозная терапия включала назначение следующих препаратов: атаракс, нейромультивит, кестин, аевит, аппликации мази «Целестодерм», «Солкосерил дентальной адгезивной пасты», масла шиповника. Больные с веррукозной формой лейкоплакии были направлены на хирургическое лечение.
Критериями эффективности комплексной терапии являлись повышение качества жизни больных, а именно уменьшение и отсутствие болевого синдрома в покое, при разговоре и приеме пищи, нормализация цвета и увлажненности слизистой оболочки, эпителизация эрозий и язв в сроки до 1 месяца. Изменения со стороны СОР и ККГ на этапах лечения верифицировались при помощи повторной АФС-диагностики и считались эффективными при уменьшении или исчезновении аномального свечения («эффекта темного пятна»), а также увеличении площади нормального зеленого свечения.
Анализ полученных результатов производился при помощи пакета прикладных программ STATISTICA версия 6.0 (StatSoft, USA) и Microsoft Excel с использованием методов одномерной статистики. Результаты представлялись в виде M±m, где M – среднее арифметическое, m – стандартное отклонение. Различия и связи между показателями считались достоверными и определялись по t–критерию Стьюдента, используя поправку Бонферрони, если уровень значимости р для соответствующего статистического критерия не превышал 0,05.
Результаты
Большинство обследованных больных предъявляли жалобы на боли при приеме пищи, чистке зубов, перманентное наличие эрозий и язв во рту, нарушение вкуса и чувствительности, повышение либо, напротив, снижение слюноотделения. Начало заболевания 45% пациентов связывали с неудачным протезированием либо с удалением зубов, в остальных случаях пусковым механизмом являлся сильный стресс. По данным анамнеза было выявлено, что 76% больных ранее обращались за стоматологической помощью, но лечение не принесло желаемых результатов. При опросе было выяснено, что при постановке диагноза практикующие врачи других медицинских учреждений в 97,9% проводили только визуальный осмотр. Дополнительные методы исследования, такие как стоматоскопия, флюоресцентная диагностика, ранее не использовались. У 12 (12,5%) больных были ранее обследованы на грибы рода Candida, морфологическое исследование при давности заболевания от нескольких месяцев до нескольких лет было проведено только 2 (2,1%) пациентам.
При анализе сопутствующей патологии у пациентов с факультативными предраковыми поражениями органов и тканей полости рта получены следующие результаты: гипертоническая болезнь служила фоном у 27 человек (71,3%), заболевания желудочно-кишечного тракта – у 48 человек (51,1%), сахарный диабет – 15 человек (15,9%), ревматоидный артрит – 10 (10,6%), заболевания крови имели 2 человека (2,1%). При этом у 84 больных (89,3%) выявлена коморбидная патология, то есть сочетание двух и более заболеваний внутренних органов, чаще всего сердечно-сосудистой и пищеварительной систем. Психоэмоциональное напряжение, канцерофобию и низкую эффективность предшествующей терапии отмечало более половины обследованных.
При объективном осмотре 90 больных с дискератозами имели частичную потерю зубов, средние значения индекса КПУ составили 18,4±0,02. Из них у 59 пациентов (61,5%) имелись некачественные ортопедические конструкции: у 20 человек - штампованно-паянные из нержавеющей стали без напыления, у 10 - те же конструкции с напылением, у 29 пациентов – металлокерамические коронки и мостовидные протезы. Острые края зубов или коронок являлись причиной декубитальной язвы у 12 больных (12,8%). Выявленные нарушения были устранены врачом стоматологом-ортопедом и включали снятие конструкций, временное и постоянное протезирование, а также совместное со стоматологом-терапевтом динамическое наблюдение. Заболевания пародонта в виде хронического гингивита и пародонтита обнаружены в 100% случаев. Синдром Гриншпана, т.е. сочетание плоского лишая СОР, гипертонической болезни и сахарного диабета имело место у 17 человек. Все они были проконсультированы врачами терапевтом и эндокринологом и находились на поддерживающей терапии.
В результате АФС-исследования у трети обратившихся выявлено нарушение аутофлюоресценции мягких тканей полости рта в виде усиления или, напротив, снижения его интенсивности. Так, у 94 человек (31,3%) эндогенное флюоресцентное свечение отличалось от свечения здоровой слизистой оболочки. Из них у 79 больных (84%) с эрозивно-язвенными заболеваниями СОР и ККГ выявлено гашение флюоресценции, которое визуализировало в виде темных участков без видимого свечения. В очагах гиперкератоза, напротив, отмечено усиление флюоресценции в виде ярко-белого свечения. По результатам онкоскрининга у 3 больных выявлено неоднородное ярко-красное или бурое свечение патологических элементов, впоследствии у них был морфологически верифицирован плоскоклеточный рак СОР.
На этапах комплексного лечения проводилась повторная АФС-диагностика и измерение площади патологических элементов на 7, 10, 14, 21-е сутки (рис. 2), что позволило визуализировать динамику эпителизации патологических элементов и оценить эффективность комплексной терапии (табл.).
Динамика эпителизации патологических элементов на этапах комплексного лечения предраковых заболеваний СОР и ККГ при помощи АФС-диагностики
|
Сроки терапии Диагноз |
Площадь эрозивной поверхности, мм2 |
|||||
|
До лечения |
7 сут. |
10 сут. |
14 сут. |
21 сут. |
1 мес. |
|
|
Эрозивно-язвенная форма ПЛ СОР (n=47) |
3,94±0,2 |
3,12±0,2 |
2,21±0,3* |
1,63±0,1* |
0,45±0,1* |
0,21±0,03* |
|
Эрозивная форма лейкоплакии СОР (n=20) |
3,12±0,01 |
2,71±0,02 |
1,92±0,03* |
1,46±0,02* |
0,63±0,01* |
0,11±0,02* |
|
Декубитальная язва СОР (n=12) |
1,34±0,01 |
0,79±0,02 |
0,53±0,03* |
0,24±0,02* |
0,11±0,01* |
0,01±0,02* |
* достоверность при значениях р≤0,05.
По результатам мониторинга пациентов с эрозивно-язвенной формой ПЛ (рис. 1) выявлено, что на 7-е сутки лечения наблюдалась эпителизация 41,2% эрозивной поверхности, на 14-е - отмечено заживление у 63,4% и на 21-е сутки – 71,3%. На 28-е сутки наблюдалось заживление 93,6% эрозивной поверхности (рис. 2). У 3 пациентов (6,4%) на фоне проводимой терапии появились новые элементы поражения на СО и к завершению курса лечения не наблюдалось полной эпителизации.
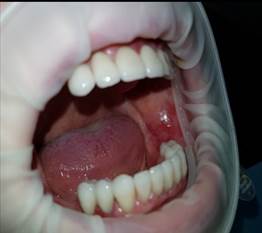
Рис. 1. Пациентка К., 1948 г.р. Диагноз: плоский лишай слизистой оболочки рта, эрозивно-язвенная форма. Визуальный осмотр
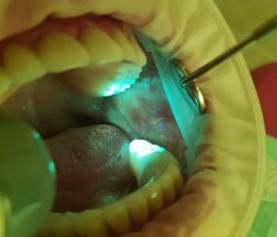
Рис. 2. Пациентка К., 1948 г.р. Плоский лишай слизистой оболочки рта, эрозивно-язвенная форма. Аутофлюоресцентная диагностика
По результатам контрольных осмотров пациентов с эрозивной формой лейкоплакии на 7-е сутки отмечена эпителизация 23,3% эрозивной поверхности; на 14-е – 43,4%; на 21-е – 66,7%, на 28-е - 80,1%. При оценке результатов лечения хронической травматической язвы СО щек и языка посредством АФС-диагностики выявлена эффективность в 91,6% случаев, у 1 больного отмечен рецидив заболевания через 12 месяцев после лечения в связи с неадекватным протезированием.
Следует отметить, что более половины больных с хроническими дискератотическими процессами полости рта отмечали уменьшение болевого синдрома и улучшение качества жизни уже через 7 дней от начала комплексной терапии, а к его окончанию 93,6% и 80,1% пациентов соответственно.
Выводы
Таким образом, в настоящее время существует проблема четкого алгоритма диагностики, стратегии и тактики ведения больных с предраковой патологией слизистой оболочки рта.
В свою очередь, использование аутофлюоресцентной диагностики на первичном приеме в стоматологии позволяет обнаруживать различия в свечении здоровой и патологически измененной ткани, а также позволяет улучшить визуализацию и объективно определить площадь пораженной поверхности.
Кроме того, прибор «АФС-Д» может быть рекомендован и для оценки эффективности результатов лечения и динамического наблюдения больных с дискератозами слизистой оболочки ротовой полости. При этом комплексное лечение этой категории больных должно включать санацию полости рта, устранение травмирующих факторов, конструкций из разнородных металлических сплавов, оптимальную медикаментозную терапию и рациональный подход к ортопедическому лечению.
Библиографическая ссылка
Пурсанова А.Е., Казарина Л.Н., Гулян У.Г., Серхель Е.В. ОЦЕНКА ЭФФЕКТИВНОСТИ ТЕРАПИИ ПРЕДРАКОВЫХ ЗАБОЛЕВАНИЙ СЛИЗИСТОЙ ОБОЛОЧКИ РТА ПРИ ПОМОЩИ АУТОФЛЮОРЕСЦЕНТНОЙ ДИАГНОСТИКИ // Современные проблемы науки и образования. 2018. № 4. ;URL: https://science-education.ru/ru/article/view?id=27754 (дата обращения: 18.06.2025).



