Регуляция кислородтранспортной функции (КТФ) крови при возрастании уровня двигательной активности (ДА) обеспечивается механизмами разного уровня: от количественной и качественной перестройки эритрона до изменения сродства к кислороду и гетерогенной структуры гемоглобина (Hb) [1]. Индивидуальные особенности организма длительно выполнять физические нагрузки, в свою очередь, во многом определяются генетическими факторами, обусловливающими фенотипические проявления адаптационных изменений [2-4].
Особый интерес представляют гены, белковые продукты которых могут прямо или косвенно участвовать в проявлении физических качеств. К их числу относят гены, отвечающие за работу сердечно-сосудистой системы, сокращение мышц, определяющие эффективность использования углеводных и липидных ресурсов и т.д. [5; 6]. Данными маркерами могут служить полиморфизмы генов ангиотензин-превращающего фермента (АCE) и химазы сердца (CMA1).
AСЕ является важным гуморальным регулятором артериального давления за счет синтеза ангиотензина 2 - активного сосудосуживающего вещества [7]. Наиболее значимым в отношении влияния на физические качества считается инсерционно-делеционный полиморфизм (I/D) гена ACE. У носителей *D аллеля отмечена высокая экспрессия гена [3; 6; 7].
Ген CMA1 кодирует фермент химазу, ответственный за альтернативный путь биосинтеза ангиотензина 2. Химаза обладает даже большей ферментативной активностью, чем АСЕ. В 5’-нетранслируемой области гена CMA1 обнаружена точечная замена остатка A на G в положении –1903. У представителей аллеля *А CMA1 наблюдается повышенный синтез фермента [8].
На сегодняшний день известны факты о связи полиморфизмов генов с физической работоспособностью и выносливостью, тогда как ассоциация полиморфизмов генов АСЕ и CMA1 с показателями кислородтранспортной системы крови в зависимости от уровня физической активности остается малоизученной. В связи с этим целью данного исследования явилось исследование влияния I/D аллельных вариантов гена АСЕ и A(–1903)G гена CMA1 на показатели красной крови и гемоглобинового профиля в зависимости от уровня ДА.
Материалы и методы
В исследовании приняло участие 245 юношей - студентов в возрасте 21±2 года, клинически здоровых по результатам ежегодного диспансерного осмотра, давших письменное согласие на участие в эксперименте. Контингент обследуемых по уровню ДА, в соответствии с рекомендациями ВОЗ [9], был разбит на три группы. Группу с низкой ДА (НДА) составили студенты (151 чел.), которые, согласно данным анкет, проявляли физическую активность менее 150 минут в неделю; с умеренной ДА (УДА) – 44 юноши, занимающиеся аэробикой, плаванием или быстрой ходьбой средней интенсивности 150–300 минут в неделю. Группу с высокой ДА представляли студенты факультета физической культуры, имеющие на момент обследования первый взрослый спортивный разряд по легкой атлетике (50 чел.), в данной группе тренировки проходили 4 раза в неделю по 2 часа, это 480 минут в неделю.
Материалом для генетического исследования послужила венозная кровь, взятая из локтевой вены индивида. Выделение ДНК осуществляли из лейкоцитов периферической крови с использованием стандартной фенол-хлороформной методики. Определение полиморфизмов I/D гена AСЕ и A(-1903) G гена CMA1 осуществлялось методом полимеразной цепной реакции (ПЦР). Для определения нуклеотидной замены в гене CMA1 использовали метод ПДРФ-анализа, ПЦР–продукты расщепляли рестриктазой BstXI. Генетический анализ проводили на кафедре генетики БГПУ им. Акмуллы.
Измерения содержания эритроцитов (RBC), гемоглобина (Hb), среднего объема эритроцита (MCV), средней концентрации гемоглобина в клетке (MCHC), гематокрита (Ht) проводились с помощью автоматического гематологического анализатора ADVIA 60 производства BAYER (Германия). В капиллярной крови на аппарате RAPIDLAB865 фирмы BAYER (Германия) анализировали показатели гемоглобинового профиля крови (оксигенированного Hb – HbO2, фетального Hb – FetHb).
Статистический анализ производили с помощью программ Microsoft Office Excel и Statistics 10.0, значимость различий между показателями в сравниваемых группах определяли с помощью t-критерия Стьюдента и двухфакторного дисперсионного анализа ANOVA. Различия считались статистически значимыми при p<0.05.
Результаты и обсуждения
По результатам исследования для носителей разных вариантов гена CMA1 установлены общие закономерности варьирования показателей красной крови при возрастании интенсивности физических нагрузок. Они выражаются в более высоком уровне суммарных показателей у спортсменов по сравнению с физически малоактивными юношами: общего количества эритроцитов (RBC) (достоверно при генотипах A/A и A/G) и гематокрита (достоверно при G/G генотипе) на фоне снижения объема отдельных эритроцитов (MCV) (достоверно при А/А генотипе), содержания (MCH) и концентрации (MCHC) гемоглобина в клетках (достоверно при A/A и G/G генотипах). Отмеченные тенденции в наибольшей степени проявляются у обладателей генотипов А/А, G/G и в меньшей - при гетерозиготном генотипе.
Сравнение средних значений при одинаковом уровне ДА в зависимости от генотипов полиморфизма А(1903)G гена СМА1 продемонстрировало наличие различий только в группе НДА по показателю MCV. У юношей с G/G вариантом размеры эритроцитов были меньше, чем при А/А генотипе (p<0,05) (табл. 1).
Что касается показателей фракционного состава гемоглобина, то здесь существенных различий у носителей разных генотипов гена CMA1 при разном уровне ДА не обнаружено.
Таблица 1
Количественные и морфофункциональные параметры красной крови и фракций гемоглобина у юношей с разным уровнем ДА в зависимости от генотипов гена CMA1 (M±m)
|
НДА |
УДА |
ВДА |
|||||||
|
A/A |
A/G |
G/G |
A/A |
A/G |
G/G |
A/A |
A/G |
G/G |
|
|
n(46) |
n (82) |
n(23) |
n(10) |
n(30) |
n(4) |
n(26) |
n(4) |
n(20) |
|
|
Группа 1 |
Группа 2 |
Группа 3 |
Группа 4 |
Группа 5 |
Группа 6 |
Группа 7 |
Группа 8 |
Группа 9 |
|
|
HGB, г/л |
152 (3,1) |
146 (1,6) |
143 (4,3) |
149 (4,1) |
142 (4,3) |
145 (3,3) |
144 (3,7) |
150 (3,2) |
142 (2,1) |
|
RBC, 1012 |
4,9 (0,1)7 |
4,8 (0,09)8 |
4,6 (0,2) |
4,8 (0,2) |
4,8 (0,14) |
5,22 (0,2) |
5,2 (0,1)1 |
5,31 (0,2)2 |
4,9 (0,05) |
|
HTC,% |
43 (0,8)3 |
41 (0,7) |
39 (1,3)1,9 |
41,0 (1,6) |
41,7 (1,1) |
41,4 (1,3) |
43,3 (0,9) |
45,2 (1,4) |
42 (0,4)3 |
|
MCV,fl |
86,8 (0,8)7 |
86,1 (0,6) |
86,1 (1,1) |
84,4 (0,3) |
86,6 (0,62) |
79,4 (1,0) |
82 (1,5)1 |
85,3 (1,2) |
85,2 (0,7) |
|
MCH, Pg |
30,6 (0,7)7 |
30,3 (0,7) |
31,1 (0,9)9 |
30,7 (1,5) |
29,4 (0,54) |
27,7 (0,8) |
27,5 (0,6)1 |
28,2 (0,5) |
28,8 (0,4)3 |
|
MCHC,g/l |
352,9 (6,8)7 |
353 (8,2) |
361 (9,1)9 |
364 (17,6) |
340 (5,3) |
350 (5,3) |
332 (3,2)1 |
331 (4,2) |
338 (2,6)3 |
|
HbO2,% |
93,0 (0,1) |
92,9 (0,5) |
93,5 (0,3) |
93,1 (0,6) |
94,4 (0,9) |
93,7 (0,4) |
93,6 (0,9) |
95,3 (1,2) |
94 (0,7) |
|
FetHb,% |
3,4 (1,0) |
3,7 (0,3) |
3,9 (0,6) |
3,2 (0,6) |
2,9 (1,2) |
3,7 (0,3) |
2,9 (0,5) |
3,1 (1,0) |
4,1 (0,8) |
Обозначения: группа 1 – носители генотипа A/A с НДА; группа 2 – носители генотипа A/G с НДА; группа 3 – носители генотипа G/G с НДА; группа 4 – носители генотипа A/A с УДА; группа 5 – носители генотипа A/G с УДА; группа 6 – носители генотипа G/G с УДА; 7 – носители генотипа A/Ac ВДА; 8 – носители генотипа A/G с ВДА; 9 – носители генотипа G/G с ВДА. Индексы 1, 2, 3, 4, 5, 6 означают достоверные отличия от соответствующих групп при р <0,05.
При сравнении среднегрупповых значений показателей в группах с разным уровнем ДА в зависимости от генотипов гена АСЕ выявлена противоположная картина. У обладателей I/D аллельных вариантов гена АСЕ базовые показатели красной крови варьируют в зависимости от интенсивности физических нагрузок незначительно, тогда как гемоглобиновый профиль – статистически значимо. Возрастание физической активности сопровождается снижением среднего объема эритроцитов у носителей D/D генотипа. Кроме того, в этой группе размеры эритроцитов оказались ниже, чем у юношей с генотипами I/D и I/I (табл. 2).
Таблица 2
Количественные и морфофункциональные параметры красной крови и фракции гемоглобина у юношей с разным уровнем ДА в зависимости от генотипов гена АCE (M±m)
|
НДА |
УДА |
ВДА |
|||||||
|
D/D |
I/D |
I/I |
D/D |
I/D |
I/I |
D/D |
I/D |
I/I |
|
|
Гр. 1 n(64) |
Гр.2 n(62) |
Гр.3 n(25) |
Гр. 4 n(15) |
Гр. 5 n(23) |
Гр.6 n(6) |
Гр. 7 n(22) |
Гр.8 n(12) |
Гр.9 n(15) |
|
|
Hb g/l |
138 (3,4) |
140,8 (2,9) |
133 (5,2) |
147 (3,6) |
147 (1,9) |
146 (3,1) |
140 (7,2) |
149,4 (2,6) |
151 (7,6) |
|
Ht, % |
41 (1,3) |
41,8 (0,9) |
39 (1,6) |
42 (1,0) |
43 (0,7) |
42 (0,8) |
42,0 (2,1) |
44,5 (0,7) |
45 (2,0) |
|
MCV, fl |
87 (0,9)7 |
87,8 (0,4) |
86 (0,8) |
84 (1,1) |
86 (1,2) |
87 (1,3) |
82 (1,0)1,9 |
85,8 (1,4) |
88 (0,3)7 |
|
MCHC, g/l |
33 (0,2) |
33,7 (0,1) |
33 (0,2) |
34 (0,2) |
34 (0,2) |
34 (0,2) |
33 (0,2) |
33,5 (0,2) |
33 (0,3) |
|
HbO2,% |
94 (0,4)2 |
92,9 (0,3)1,8 |
93 (0,6) |
93 (0,7)7 |
92 (0,7)8 |
92 (1,1) |
95 (0,5)4 |
96(0,3)2,5,9 |
92 (1,9)8 |
|
FetHb,% |
3 (0,2)2 |
4(0,3)1,3,5,8 |
3,0 (0,5)2 |
3,3 (0,4) |
2 (0,4)2,8 |
3,7 (0,7) |
2,7 (0,5) |
1,7(0,1)2,5,9 |
4,4 (1,0)8 |
Обозначения: группа 1 – юноши с генотипом D/D с НДА; 2 – генотип I/D с НДА; 3 – генотип I/I с НДА; 4 - юноши с генотипом D/D с УДА; 5 – генотип I/D с УДА; 6 - генотип I/I с УДА; 7 - юноши с генотипом D/D с ВДА; 8 – генотип I/D с ВДА; 9 –генотип I/I с ВДА. Индексы 1, 2, 3, 4, 5, 6, 7, 8, 9 означают достоверные отличия от соответствующих групп при р ≤ 0,05.
В то же время как варианты генотипов полиморфизма I/D гена АCE, так и ДА существенно влияют на содержание фракций гемоглобина. Уровень оксигенации гемоглобина (HbO2) у спортсменов, имеющих в своем генотипе аллель *D, достоверно выше по сравнению с аналогичными генотипами в группах с более низкой ДА. У юношей с генотипом I/I содержание HbO2 по мере роста физической активности существенно не меняется. Более того, его доля у спортсменов ниже, чем у носителей аллеля *D. Уровень плодного гемоглобина также зависит от интенсивности ДА и полиморфизма гена АCE. Так, у носителей I/D генотипа при НДА содержание FetHb достоверно выше, чем при других генотипах в данной группе (p<0,05). Однако по мере роста физической активности у юношей с гетерозиготным вариантом гена АСЕ доля FetHb достоверно снижается, при ВДА наблюдался самый низкий уровень показателя. У спортсменов с генотипом I/I по мере роста ДА уровень FetHb повышается (достоверно по отношению к I/D генотипу) (p<0,05).
Поскольку FetHb обеспечивает длительную и стабильную адаптацию к кислородному дисбалансу [10], более высокий уровень FetHb у юношей с генотипом I/I при высоких физических нагрузках может рассматриваться как результат адаптации организма к возросшим потребностям клеток к кислороду. Согласно многочисленным исследованиям [2; 5; 6], генотип I/I гена АСЕ ассоциируется с преимущественно аэробным метаболизмом, что способствует носителям данного генотипа более длительно выполнять физические нагрузки.
Представленные результаты подтверждают данные дисперсионного анализа. На базовые показатели красной крови оказывает влияние только интенсивность ДА (RBC: p=0,018; Hb: p=0,02), тогда как на гемоглобиновый профиль достоверно влияет также и ген АСЕ (HbO2: p=0,04; FetHb: p=0,04), совместно с ДА на FetHb и MCV (p=0,001 и p=0,04 соответственно) (рис. 1 и 2).
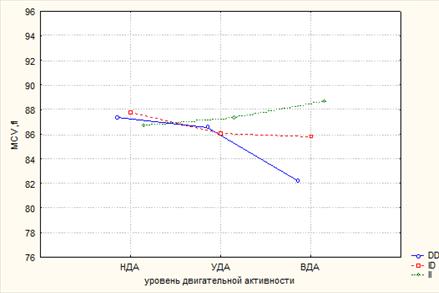
Рис. 1. Совместное влияние факторов ДА и полиморфизма I/D гена АСЕ на MCV, по данным дисперсионного анализа
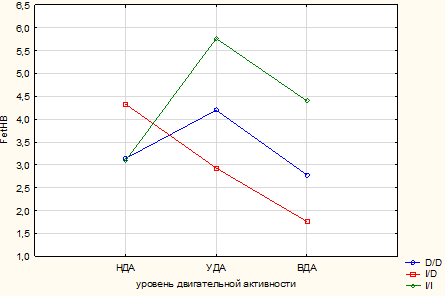
Рис. 2. Совместное влияние факторов ДА и полиморфизма I/D гена АСЕ на FetHb, по данным дисперсионного анализа
Заключение
Проведенное исследование показало, что адаптация КТФ крови к возрастанию двигательной активности реализуется через разные звенья в зависимости от полиморфизмов генов АСЕ и CMA1. Так, у юношей с разными генотипами гена CMA1 под влиянием интенсивных физических нагрузок активируется эритропоэтическая функция, направленная на увеличение численности клеток красной крови. В то же время участие гена АСЕ в адаптации организма к физической деятельности выражается у носителей аллеля *D в возрастании оксигенации гемоглобина, а генотипа I/I – увеличении доли плодного гемоглобина, обладающего повышенным сродством к кислороду.
Вместе с тем у спортсменов - носителей генотипа A/A гена CMA1 и D/D гена АСЕ обнаружено выраженное снижение размеров эритроцитов. Этот факт можно рассматривать как компенсаторную реакцию на повышение у обладателей данных генотипов сосудистого тонуса, ассоциированного с более высокой интенсивностью синтеза ангиотензина 2. Известно, что уменьшение размеров эритроцитов способствует улучшению реологических свойств крови в микроциркуляторном русле и у спортсменов расценивается как результат адаптации к систематическому выполнению физических нагрузок [11]. Можно предположить, что увеличение суммарной дыхательной поверхности крови у лиц с генотипом А/А гена СМА1, необходимое для адекватного нагрузкам обеспечения деятельности мышц, сочетается с оптимизацией реологических свойств крови.
Полученные данные свидетельствуют о том, что интенсификация двигательной активности обеспечивается при разных генотипах полиморфизмов генов СМА1 и АСЕ включением различных адаптационных механизмов функционирования КТФ крови. Этот факт говорит о необходимости учитывать индивидуальные особенности адаптации системы крови юношей при занятиях физической культурой, а также индивидуализации тренировочного процесса в зависимости от наследственного фактора.
Библиографическая ссылка
Даутова А.З., Хажиева Е.А., Шамратова В.Г. КИСЛОРОДТРАНСПОРТНАЯ ФУНКЦИЯ КРОВИ ПРИ РАЗНОМ УРОВНЕ ДВИГАТЕЛЬНОЙ АКТИВНОСТИ В ЗАВИСИМОСТИ ОТ ПОЛИМОРФИЗМОВ ГЕНОВ CMA1 И АСЕ // Современные проблемы науки и образования. 2018. № 2. ;URL: https://science-education.ru/ru/article/view?id=27496 (дата обращения: 16.05.2026).



