Российская Федерация занимает одно из первых мест в мире по распространенности курения и сердечно-сосудистых заболеваний. Глобальный опрос взрослого населения РФ о потреблении табака (Global dult Tobacco Survey), проведенный в России в 2009 году, показал, что 39,1% (43,9 млн человек) в нашей стране являются постоянными курильщиками табака. Среди мужчин оказались постоянными курильщиками 60,2% (30,6 млн), среди женщин - 21,7% (13,3 млн). В ходе исследования была выявлена высокая интенсивность этой пагубной привычки в России (в среднем мужчины выкуривают 18 сигарет в день, женщины - 13 сигарет) [1]. Распространенность курения в российской популяции, по результатам исследования ЭССЕ-РФ, проведенного в 2012-2013 гг., составила 43,5% среди мужчин и 14,2% среди женщин, причем максимальный пик курения (47,8% и 19,9% среди мужчин и женщин соответственно) приходится на самый активный возраст 25-34 года [2].
Курение представляет собой серьезную опасность для здоровья и в значительной степени способствует развитию сердечно-сосудистой заболеваемости и смертности, оказывает влияние на все стадии атеросклероза от эндотелиальной дисфункции до острых клинических событий [3]. Длительное курение является общепризнанным фактором риска развития ишемической болезни сердца (ИБС), хронической сердечной недостаточности (ХСН) [4; 5].
Широко исследована патофизиология воздействия курения на сердечно-сосудистую систему опосредованно через механизмы вазомоторной и эндотелиальной дисфункции, сосудистого воспаления, микротромбозов, перекислого окисления липидов [6; 7]. В отечественном исследовании в группе курящих пациентов с декомпенсированной ХСН (IIб и III стадии) показатель относительного риска по курению значимо преобладал в сравнении с группой, компенсированной по ХСН (I и IIа стадии) - ОР=1,7 (р=0,017) [8].
Однако структурно-функциональные изменения миокарда на фоне курения исследованы в настоящее время недостаточно. В связи с высокой распространенностью курения и его значительным влиянием на развитие и прогрессирование сердечно-сосудистых заболеваний интерес к исследованию механизмов патологического воздействия курения на миокард и сосуды, а также к поиску способов лечебного воздействия на эти механизмы остается достаточно высоким.
Цель исследования
Оценка влияния курения на структурно-функциональное состояние миокарда у пациентов с ишемической болезнью сердца.
Материалы и методы
Нами было обследовано и на условиях письменного добровольного информированного согласия в исследование включено 56 пациентов с ИБС, стабильной стенокардией напряжения I-III функционального класса (ФК), хронической сердечной недостаточностью I-III ФК, из них 24 мужчины (28,57%) и 32 женщины (71,43%).
Критерии исключения: нестабильная стенокардия, сердечная недостаточность в стадии декомпенсации, инфаркт миокарда и острое нарушение мозгового кровообращения в течение последних 3 месяцев, пароксизмальные нарушения ритма сердца, ранее диагностированная хроническая обструктивная болезнь легких, бронхиальная астма и эмфизема, тяжелые сопутствующие заболевания, в т.ч. психические, злоупотребление алкоголем, злокачественные новообразования.
Всем больным проводилось общеклиническое обследование, антропометрическое обследование, определение «офисного» артериального давления, определение показателей клинического и биохимического исследования крови, расчет скорости клубочковой фильтрации (СКФ) с помощью формул CKD-EPI и SANAKA для пациентов старше 70 лет, определение ФК ХСН при помощи теста 6-минутной ходьбы, ЭКГ, обзорная рентгенография органов грудной клетки.
Общий анализ крови выполнялся на автоматическом гематологическом анализаторе Coulter-Becman Diff 5 (США) и включал в себя определение концентрации гемоглобина, количества эритроцитов, лейкоцитов и тромбоцитов, величины гематокрита и эритроцитарных индексов (средний объём эритроцитов (MCV), среднее корпускулярное содержание гемоглобина в эритроцитах (MCH), средняя концентрация гемоглобина в эритроцитах (MCHC)), исследование лейкоцитарной формулы и скорости оседания эритроцитов.
Биохимический анализ крови выполнялся для всех пациентов централизованно с помощью автоматического биохимического анализатора CA-400 (Япония) и включал в себя определение: глюкозы крови натощак, мочевины, креатинина, электролитов (калий, натрий, хлор), общего холестерина и его фракций, общего билирубина, общего белка, аланинаминотрансферазы, аспартатаминотрансферазы, а также коагулограммы.
Электрокардиография (ЭКГ) выполнялась с помощью портативного шестиканального электрокардиографа SCHILLER CARDIOVIT AT-1 по общепринятой методике. По результатам ЭКГ оценивались сердечный ритм и проводимость, наличие или отсутствие ишемических и рубцовых изменений и гипертрофии миокарда.
Трансторакальное ультразвуковое исследование сердца проводилось c помощью аппарата Medison Sonoace 8000 EX (Южная Корея) ультрасонографическим датчиком c частотой колебания 3,5-5,0 МГц. Визуализацию структур сердца и определение размеров полостей сердца и его структур, необходимых для исследования, производили в положении больного лежа на спине и на левом боку в условиях M-режима. Анализировали не менее пяти сердечных циклов. B данном режиме измеряли конечный диастолический размер (КДР), конечный систолический размер (КСР) ЛЖ, толщину межжелудочковой перегородки (ТМЖП) и задней стенки (ТЗС) ЛЖ.
Величину конечно-диастолического объема (КДО), конечного систолического объёма (КСО) и ударного объёма (УО) сердца определяли по формуле L.E.Teicholtz (1976).
Все включенные в исследование пациенты были разделены на 2 группы: в первую группу были включены курящие пациенты в количестве 29 человек (11 мужчин и 18 женщин), средний возраст 65,3±2,37 года; во вторую группу - некурящие 27 человек (10 мужчин и 17 женщин), средний возраст 72,9±3,02 года. Группы больных были паритетны по полу, индексу массы тела, уровню гликемии, величине «офисного» артериального давления, скорости клубочковой фильтрации, показателям электролитного состава. Характеристика групп приведена в таблице 1.
Таблица 1
Характеристика групп обследованных пациентов
|
Показатель |
Группа 1 (курящие), M±m |
Группа 2 (некурящие), M±m |
|
Количество, чел. |
29 |
27 |
|
Мужчины |
18 |
10 |
|
Женщины |
11 |
17 |
|
Средний возраст, лет |
65,3±2,37* |
72,9±3,02 |
|
ИМТ, кг/ м2 |
30,2±3,4 |
31,4±2,6 |
|
СКФ, мл/мин/1,73 м2 |
||
|
Общий холестерин, ммоль/л |
5,7±1,62 |
5,4±1,84 |
|
Триглицериды, ммоль/л |
3,1±1,26 |
2,8±1,84 |
|
Глюкоза, ммоль/л |
4,4±2,24 |
4,1±1,93 |
|
Калий, ммоль/л |
4,8±2,15 |
3,7±2,62 |
|
Натрий, ммоль/л |
136,1±2,84 |
139,4±2,97 |
|
Хлор, ммоль/л |
102,5±1,56 |
108,6±2,1 |
|
Фибриноген, г/л |
3,7±1,41 |
3,4±2,0 |
|
Креатинин, мкмоль/л |
89±3,44 |
94±2,81 |
|
АД систолическое, мм рт. ст. |
146±3,51 |
146±2,88 |
|
АД диастолическое, мм рт. ст. |
98±2,21 |
96±1,98 |
|
Гемоглобин, г/л |
135±3,12 |
131±3,20 |
|
Гематокрит, % |
34±2,22 |
31±2,41 |
Примечание: * - p<0,05, ИМТ – индекс массы тела, АД – артериальное давление, СКФ – скорость клубочковой фильтрации.
Статистическая обработка результатов исследования проводилась на персональном компьютере с использованием пакета программ Microsoft Office Excel 2007 (Microsoft, США) и Statistica 6.0 (StatSoft Inc, США), а также Biostat 4.03 (McGraw Hill, США) на персональном ноутбуке с операционной системой Windows 7 Home Basic (США). Определяли значения среднего арифметического (M), стандартного отклонения (SD). Для оценки соответствия распределения наблюдаемых переменных в выборке нормальному закону использовали критерий Шапиро-Уилка, что позволило выявить отклонение от нормального закона распределения большинства показателей. В связи с этим для статистической оценки данных применялись непараметрические методы. Сравнение выборок для разных групп проводилось с использованием критериев Манна-Уитни с установлением уровня значимости р ≤ 0,05.
Полученные данные представлены в виде средних величин и среднеквадратического отклонения (M±m).
Результаты и обсуждение
В результате обследования больных не было выявлено достоверных отличий между группами по сопутствующей патологии (артериальная гипертензия, сахарный диабет, перенесенный инфаркт миокарда, постоянная форма фибрилляции предсердий) (рис. 1, 2).
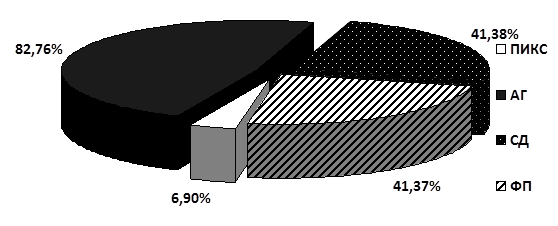
Рис. 1. Распределение сопутствующей патологии в группе курящих
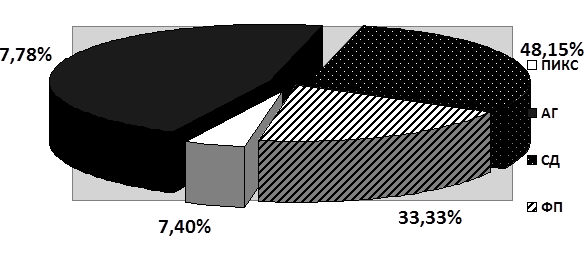
Рис. 2. Распределение сопутствующей патологии в группе некурящих
Примечание: ПИКС – постинфарктный кардиосклероз, АГ – артериальная гипертензия, СД – сахарный диабет, ФП – фибрилляция предсердий.
Однако средний возраст пациентов первой группы был достоверно меньше, чем пациентов второй группы (65,3±2,37 и 72,9±3,02 года соответственно, р<0,05), что может быть обусловлено ускорением естественных инволюционных процессов в организме на фоне активного курения [9].
При оценке показателей ЭХО-КС в группе курящих пациентов по сравнению с группой некурящих выявили достоверно больший конечно-диастолический размер левого желудочка (51,4±7,63 и 46,8±7,22 мм соответственно, р<0,05) и полости левого предсердия (42,0±4,33 и 39,13±3,98 мм соответственно, р<0,05), что соотносится с данными исследования В.В. Сыволап и др. [10]. Кроме того, в первой группе имелась тенденция к увеличению массы миокарда левого желудочка, хотя эти изменения достоверности не достигли (табл. 2).
Таблица 2
Основные показатели ЭХО-КС у обследованных пациентов
|
Показатель |
Группа 1 (курящие), M±m |
Группа 2 (некурящие), M±m |
|
КДР, мм |
51,4±7,63* |
46,8±7,22 |
|
ТМЖП, мм |
13,87±1,46 |
13,47±1,51 |
|
ТЗСЛЖ, мм |
11,93±1,49 |
11,33±1,59 |
|
ЛП, мм |
42,0±4,33* |
39,13±3,98 |
|
ММЛЖ, г |
343,11±98,15 |
293,9±115,36 |
|
ФВ, % |
51,93±7,17 |
53,27±9,01 |
Примечание: * - p<0,05, КДР - конечно-диастолический размер, ТМЖП – толщина межжелудочковой перегородки, ТЗСЛЖ – толщина задней стенки левого желудочка, ЛП – левое предсердие, ММДЖ – масса миокарда левого желудочка, ФВ – фракция выброса.
По данным ряда исследований можно отметить противоречивые результаты в отношении структурно-функциональных изменений миокарда у курящих и некурящих пациентов. В нашем исследовании не отмечено статистически значимого различия в толщине стенок миокарда левого желудочка и массы миокарда левого желудочка между группами, тогда как в исследовании В.В. Сыволап и др. [10] эти показатели достигли статистической значимости. При оценке типа ремоделирования миокарда ЛЖ также отмечалась тенденция к превалированию эксцентрического типа гипертрофии миокарда левого желудочка в группе курящих пациентов по сравнению с некурящими (51,72% и 37,04% соответственно), хотя изменения статистической значимости не достигли. Аналогичные данные были получены и в других исследованиях [9; 11]. Полученные результаты позволяют предположить значительное влияние курения на структурные изменения миокарда левого желудочка, что в дальнейшем может способствовать прогрессированию и утяжелению течения кардиоваскулярной патологии.
Фракция выброса левого желудочка в группах практически не отличалась, однако у курящих пациентов этот показатель был чуть ниже, несмотря на достоверно более молодой возраст, что может свидетельствовать о тенденции к более ранним нарушениям функции миокарда левого желудочка. Эти данные соотносимы с результатами других исследований [11].
При оценке результатов теста 6-минутной ходьбы выявлено статистически значимое преобладание более высокого ФК ХСН в группе курящих пациентов, несмотря на более молодой возраст (табл. 3).
Таблица 3
Функциональный класс ХСН у обследованных пациентов
|
ФК ХСН |
Группа 1 (курящие), количество пациентов |
Группа 2 (некурящие), количество пациентов |
|
I |
6 |
8 |
|
II |
4 |
5 |
|
III |
19* |
9 |
Примечание: * - p<0,05.
Заключение
В результате исследования выявлены более выраженные структурно-функциональные изменения миокарда левого желудочка у курящих пациентов. Патологическое ремоделирование миокарда левого желудочка на фоне табакокурения наблюдалось в более молодом возрасте. Все это позволяет расценивать курение как фактор кардиоваскулярного риска, ускоряющий развитие структурной перестройки сердца и нарушение его функций, что способствует более раннему прогрессированию хронической сердечной недостаточности.
Библиографическая ссылка
Крючкова И.В., Адамчик А.С., Панченко Д.И., Солодова Ю.А., Шульга Д.В. ВЛИЯНИЕ КУРЕНИЯ НА СТРУКТУРНО-ФУНКЦИОНАЛЬНОЕ СОСТОЯНИЕ МИОКАРДА И ПРОГРЕССИРОВАНИЕ КАРДИОВАСКУЛЯРНОЙ ПАТОЛОГИИ // Современные проблемы науки и образования. 2017. № 6. ;URL: https://science-education.ru/ru/article/view?id=27152 (дата обращения: 02.07.2025).



