Актуальность исследования
В мире отмечается рост операций первичного и ревизионного эндопротезирования крупных суставов. По данным регистра эндопротезирования тазобедренного сустава РосНИИТО им. Р.Р. Вредена, в период с 2007 по 2012 г. доля ревизионных операций колебалась с 13,4 % до 18,8 % от общего числа операций по замене тазобедренного сустава и составила 1543 ревизионных вмешательства [1, 2].
Расширения показаний к имплантации первичных эндопротезов у подростков и лиц от 20–30 лет ведет к быстрому истиранию пары трения, прогрессированию остеолиза и возникновению расшатывания компонентов эндопротеза тазобедренного сустава [3-6].
Дефекты бедренной кости приводят не только к расшатыванию внутрикостных конструкций, но и патологическим переломам, рецидивирующим вывихам эндопротеза, глубокой инфекции. Лечение этих больных чрезвычайно сложная задача, потому что помимо устранения дефектов костей образующих тазобедренный сустав, необходимо еще и дать этим больным возможность двигаться, иметь одинаковую длину ног и обслуживать себя без боли [7, 8].
Классификацией дефектов бедренной кости, являющейся на сегодняшний день наиболее удобной, является классификация Valle C.J., Paprosky W.G., предложенная ими в 2003 году. Она удобна для применения в клинической практике для предоперационного планирования и выбора тактики оперативного лечения. Выделяются сегментарные дефекты бедренной кости, приравнивая их к градации с I по IIIA и тотальные дефекты бедренной кости, соответствующие IIIB и IV типам.
При IIIB определяется значительная потеря губчатой и кортикальной кости в области метаэпифиза с потерей опорной функции кости с сохранением менее 4 см, нормальной кости в области нижней трети диафизарного отдела. Опорная функция проксимальной части диафиза бедра серьезно снижена; IV тип – разрушение губчатой и кортикальной кости на большем протяжении диафиза бедра, с образованием сегментарных дефектов. Следы неизмененной костной ткани могут сохранятся в области дистального метаэпифиза бедра.
Использование трупных бедренных костей показало, что даже сохранение от 1,5 до 2,5 см неизмененной костной ткани дистального отдела диафиза бедренной кости является достаточным условием для стабильной первичной фиксации конического бедренного компонента эндопротеза [9, 10].
Современный дизайн ревизионных бедренных компонентов подразделяется на конические [11, 12, 13], при внедрении которых производится заклинивание их в дистальном отделе за счет своих граней (прямоугольное, звездчатое сечение), расположенных на конусе, и цилиндрические компоненты с пористой структурой, которые придают значительное сопротивление при ротационных движениях [14-17].
Как конические, так цилиндрические ревизионные бедренные компоненты бывают модульными или моноблоковыми. Использование модульных имплантатов позволяет хирургу вносить более точные интраоперационные корректировки в смещении и калибровке, что позволяет регулировать натяжение мягких тканей, длину ноги и офсет, снижая в дальнейшем вероятность вывиха [18-22].
Использование ревизионных ножек Цваймюллера целесообразно при сохранении опорной кортикальной кости толщиной не менее 2 мм ниже уровня малого вертела на протяжении как минимум 6 см и при тотальных дефектах бедренной кости приводит к большому количеству неудач в среднесрочной перспективе [23].
В клинической практике наибольшую популярность получили использования конических ножек Wagner. Böhm P. с соавт. (2001) имплантировали бедренный компонент Wagner S.L. в 129 случаях при значительных дефектах бедренной кости. Кумулятивная выживаемость за 11,1 лет составила 93,9 %. Средний значение Merled'Aubigné улучшился с 7,7 баллов до операции до 14,8 баллов при последнем контрольном осмотре. Рентгенологическое обследование на момент написания статьи показало хорошее или отличное восстановление проксимальной части бедра в 113 (88 %) случаях [8].
Выживаемость цилиндрического бедренного сустава S-ROM при Paprosky III через 15 лет с пересмотром по любой причине в качестве конечной точки составила 90,5 % (95 % доверительный интервал (ДИ) 85,7 до 93,8) и с пересмотром асептического ослабления в качестве конечной точки 99,3 % (95 % ДИ 97,2–99,8) [24]. March G.M, с соавт. (2014) в ретроспективном обзоре сообщают о рентгенологических и клинических исходах одиннадцати пациентов с ХПН, подвергшихся ревизионной артропластике с использованием длинно-пористого цилиндрического бедренного компонента. Бедренная кость у всех пациентов на фоне ХПН имела дефекты (Paprosky IIIB и IV). При среднем сроке наблюдения 8 лет (от 2 до 14) не было выявлено переломов бедренной кости. Расшатывания бедренного компонента не наблюдалось [10].
Клинические методики имплантации бедренных компонентов эндопротеза при Paprosky IV дефектах бедренной кости
Первичная фиксация ревизионного бедренного компонента эндопротеза тазобедренного сустава в условиях отсутствия неизмененной кости в дистальном отделе бедренной кости обеспечивается ограниченным набором методик.
1. Производится проведение поперечных винтов через дистальный отдел бедренной кости и поперечные отверстия в дистальном отделе ревизионного бедренного компонента (Brand S. etall., 2015). Отмечено, что такой метод стабильной фиксации бедренного компонента эндопротеза приводит к разрушению винтов и миграции ножки эндопротеза в среднем у 4,8 % оперированных за 15 летний период [11, 25], рекомендуют использовать подобную методику при наличии не менее 3 см неизмененной бедренной кости в дистальном отделе.
2. Использование ПММА цемента при подобной фиксации как альтернатива дистальной фиксации винтами рекомендована для больных пожилого и старческого возраста [15,18, 21, 34].
3. Исследования доказывают, что восстановление опорной функции бедра, путем придания первичной стабильности беcцементному бедренному компоненту при тотальных костных дефектах, можно обеспечить, использовав от 1 до 3 костных кортикальных аллотрансплантатов, уложив их по всей длине вокруг ревизионного бедренного компонента эндопротеза без дополнительной фиксации винтами. Они мотивируют это тем, что остеолиз кортикальных аллотрансплантатов начинает происходить через 1 год после ревизионной хирургии, идет медленно и утихает через 3 года. Использование такой технологии первичной фиксации демонстрирует выживание бедренного компонента эндопротеза в течение 16 лет у 91 % оперированных [16].
4. Широкую популярность имеет АРС (allograft-prosthesiscomposite) эндопротезирование (см. рисунок). Соразмерный ревизионный бедренный компонент эндопротеза фиксируется в межвертельной зоне и верхней трети диафиза цельной бедренной аллокости с помощью ПММА цемента. Рассчитав длину отсутствующего проксимального отдела бедра в аллокости, удаляют внутреннюю полуокружность продольно, а оставшуюся наружную полуокружность аллокости совместно с бедренным компонентом эндопротеза имплантируют интрамедуллярно в дистальный отдел кости больного. Поперечник внутренней полуокружности аллокости опирается на внутреннюю полуокружность кости больного, а дистальный отдел ревизионного эндопротеза совместно с наружной полуокружностью бедренной кости устанавливается интрамедуллярно в диафизарно-мыщелковый «стакан» сохранившейся кости больного. Дополнительно с помощью серкляжных швов укладываются кортикальные аллотрансплантаты по типу вязанки хвороста, перекрывая зону аллокости и кости больного [24].
В диафизарно-мыщелковом «стакане» кости больного вокруг ревизионного бедренного компонента и наружного отдела структурной бедренной аллокости осуществляется импакционная костная пластика губчатыми аллотрансплантатами. Для придания стабильности производится дистальная чрезкостная фиксация винтами. Учитывая, что именно винты,
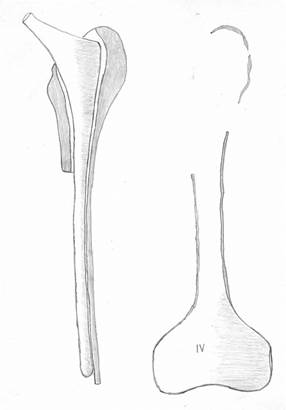
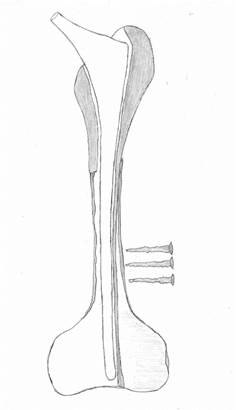
АРС (allograft-prosthesis composite) эндопротезирование
проведенные поперечно, будут испытывать основную осевую нагрузку, их рекомендуют проводить не менее 3, толщиной до 5 мм [26-29].
Интерпретация многих клинических исследований не объективна, потому что они не систематизированы в зависимости от классификации потери костной ткани бедра и используют различные хирургические методы фиксации аллотрансплантата. Общая выживаемость реконструкции бедренной кости протезом APC варьируется по литературным данным от 72 % до 90 % через пять лет и от 64 % до 86 % через десять лет [24, 30, 31, 32]. Повторная ревизия APC бедренного компонента на новый АРС у 21 (асептическое расшатывание у 18 и глубокая инфекция у 3 больных) больного демонстрируют 83,5 % общей выживаемости спустя 10 лет после операции [33].
5. Одно из популярных направлений является применение онкологических бедренных компонентов эндопротезов с фиксацией дистального отдела на костном цементе. Отсутствие осложнений при этом обратно пропорционально активности больного, что соответствует больным старшей возрастной группы [26-29,34,35]. С учетом этого общая выживаемость первичных онкологических мегапротезов составляет в среднем 81 % за 11 лет наблюдения [35], а ревизионных 57 % в течение 5-ти лет [36]. Использование онкологических имплантатов (Modular Universal Tumour And Revision System (MUTARS®) в ревизионном эндопротезировании тазобедренного сустава при тяжелых дефектах бедренной кости при среднем наблюдении 40 месяцев показало преимущество хороших результатов. Использование мега имплантатов ведет к увеличению частоты развития глубокой инфекции [37], и рекомендованы они в крайнем случае, когда другие операции выполнить невозможно [38].
6. При неоднократных ревизионных вмешательствах применяется тотальное замещение бедренной кости мега протезом с формированием тазобедренного и коленного суставов [39].
Большинство авторов предпочитают в условиях массивного проксимального остеолиза бедренной кости использовать модульные ревизионные бедренные компоненты, подтверждая их преимущества клиническими данными [17]. Использование модульного конусного эндопротеза LINK MP у 470 пациентов с IV типом остеолитических дефектов по классификации Paprosky W.G. показало, что основными осложнениями интраоперационно и ближайшем послеоперационном периоде был перипротезной перелом (интраоперационно 21 случаев и после операции 8 случаев). Структура осложнений в среднем через 5,7 лет после ревизионного вмешательства включала инфекции (7 случаев), вывих (5 случаев), онемение, вызванное тракционной нейропатией седалищного нерва (6 случаев) и отек бедра (3 случая). Динамическое рентгенологическое наблюдение выявило миграцию бедренного компонента эндопротеза в 4-х случаях [40].
По данным литературы при дефектах бедренной кости Paprosky IV преимущественно необходимо использовать цилиндрические бедренные компоненты. Во-первых, они тупые на конце и не могут перфорировать передне-нижнюю стенку межмыщелковой борозды коленного сустава при вертикальной миграции, во-вторых, та часть кости, которая все еще сохранилась в дистальном отделе метафиза, способна создать шероховатость и сохранить торсионную стабильность на всем протяжении, а не только на верхней трети конуса при использовании конусных имплантатов, и, в-третьих, чем толще слой металла в дистальном отделе от отверстия для винтов дистального заклинивания до поверхности имплантата, тем дольше не наступит усталость металла при нагрузке на винты.
Обсуждение
Неизбежно встает вопрос, почему у разных авторов при имплантации бедренных ревизионных компонентов при наличии тотальных дефектов бедренной кости частота развития осложнений значительно отличается? Для ответа на этот вопрос необходимо обратиться к истории создания классификации дефектов бедренной кости Valle C.J., Paprosky W.G., (2003). Эта классификация описывает остеолизные дефекты бедренной кости. При этом нестабильный бедренный компонент представляет собой инородный секвестр, находящийся в своем «склерозированном доме». Сохраненный дистальный промежуток диафиза бедренной кости по своей структуре представляет собой склерозированную (стеклянную), хрупкую костную ткань.
Большинство авторов предпочитают в условиях массивного проксимального остеолиза бедренной кости использовать модульные ревизионные бедренные компоненты, подтверждая их преимущества клиническими данными. Использование модульного конусного эндопротеза LINK MP у 470 пациентов с IV типом остеолитических дефектов по классификации Paprosky W.G. показало, что основными осложнениями интраоперационно и ближайшем послеоперационном периоде был перипротезной перелом (интраоперационно 21 случаев и после операции 8 случаев). Структура осложнений в среднем через 5,7 лет после ревизионного вмешательства включала инфекции (7 случаев), вывих (5 случаев), онемение, вызванное тракционной нейропатией седалищного нерва (6 случаев) и отек бедра (3 случая). Динамическое рентгенологическое наблюдение выявило миграцию бедренного компонента эндопротеза в 4-х случаях.
Таким образом, у больных пожилого возраста рационально применение дистальной фиксации цилиндрического бедренного компонента, а у более молодых АРС эндопротезирование или дистальное заклинивание бедренного компонента эндопротеза полосками аллокости по методике Kim Y.H. У пациентов старше 70 лет рационально использовать ПММА цементной фиксацию бедренного компонента эндопротеза в дистальном, сохраненном отделе или применять мега и онкопротезы.
Библиографическая ссылка
Гуацаев М.С., Плиев Д.Г., Михайлов К.С., Булатов А.А., Синеокий А.Д. ДИЗАЙН И ХИРУРГИЧЕСКИЕ МЕТОДИКИ ИМПЛАНТАЦИИ РЕВИЗИОННЫХ БЕДРЕННЫХ КОМПОНЕНТОВ ЭНДОПРОТЕЗА ТАЗОБЕДРЕННОГО СУСТАВА ПРИ ТОТАЛЬНЫХ ДЕФЕКТАХ БЕДРЕННОЙ КОСТИ // Современные проблемы науки и образования. 2017. № 6. ;URL: https://science-education.ru/ru/article/view?id=27147 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.27147



